Clear Sky Science · ru
Модуляция иммунитета, обусловленная ротовой микробиотой, вдоль оси «рот–кишечник»: от локальных сигналов до системного воспаления
Почему ваш рот важен для всего организма
Бактерии, живущие в полости рта, делают гораздо больше, чем просто вызывают кариес или неприятный запах. В этом обзорном материале объясняется, как ротовые микробы могут попадать в кишечник, нарушать его тонкие защитные механизмы и запускать воспалительные процессы, достигающие таких органов, как печень и мозг. Понимание этой скрытой «оси рот–кишечник» даёт новые подсказки о распространённых проблемах — от неалкогольной жировой болезни печени до болезни Альцгеймера — и указывает на удивительно простые меры, такие как улучшение стоматологического ухода и корректировка питания, которые могут защитить наше общее здоровье.
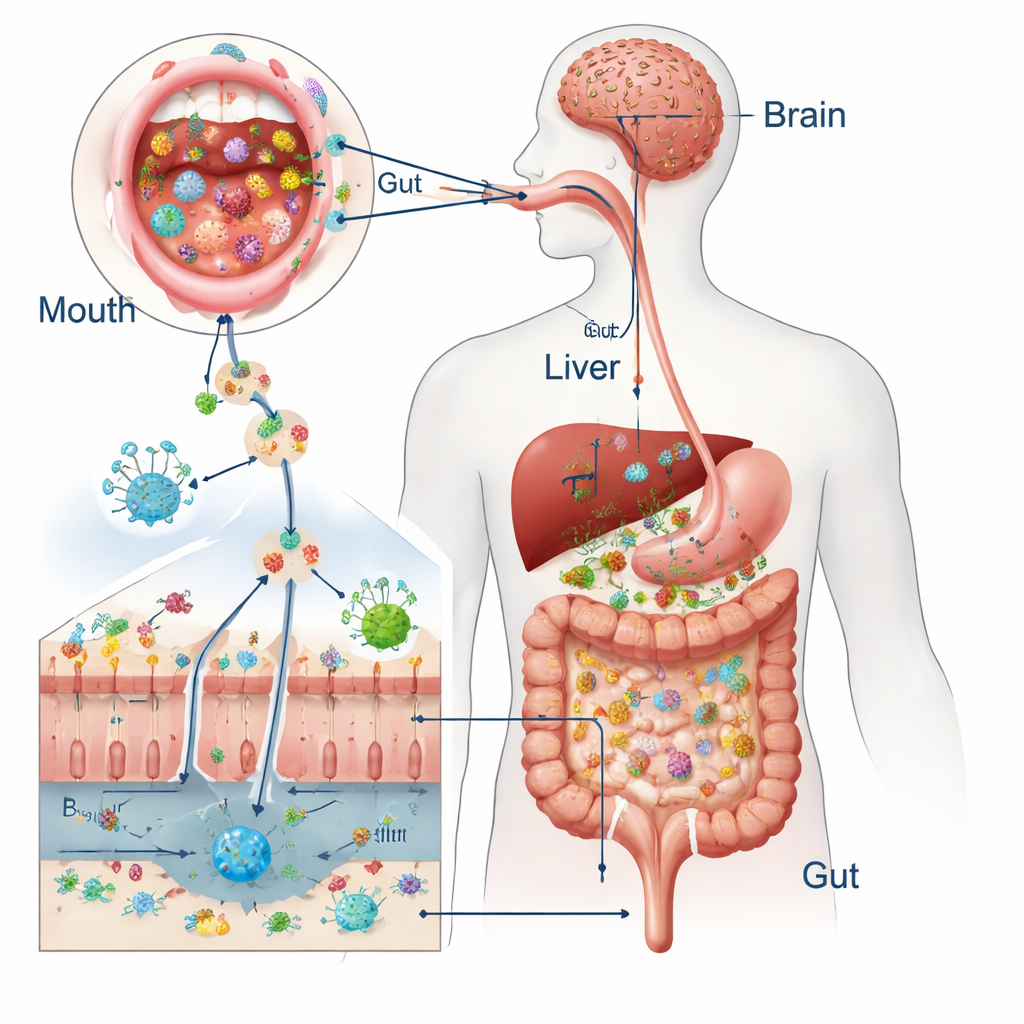
От проглатывания до системных эффектов
Каждый день мы проглатываем примерно полтора литра слюны, содержащей миллиарды микробов полости рта. У здоровых людей сильные барьеры — природные антимикробные факторы слюны, соляная кислота желудка, желчные кислоты, вязкая слизь и плотные межклеточные контакты кишечника — не дают большинству этих «гостей» осесть. Сравнения микробиоты рта и стула показывают, что при нормальном состоянии только крошечная доля кишечных микроорганизмов поступает прямо из рта. Тем не менее экосистемы перекрываются в достаточной мере, что ротовые виды, такие как Streptococcus и Veillonella, иногда обнаруживают в кишечнике, что ставит вопрос: когда они перестают быть безвредными прохожими?
Когда барьеры дают сбой
Картина меняется под влиянием стресса. Старение, сухость во рту, плохая гигиена полости рта и хронические заболевания дёсен могут привести к избытку вредных бактерий в ротовой полости. Лекарства — например антибиотики и блокаторы желудочной кислоты — ослабляют защиту кишечника, истончая слизистую, ослабляя межклеточные связи и позволяя большему числу микробов пережить путь через желудок. Ротовые инфекции и стоматологические процедуры могут даже способствовать попаданию бактерий в кровоток. В обзоре также выделяются внеклеточные везикулы бактерий — наномасштабные «посылки», которые микробы сбрасывают и которые могут проникать через ткани, неся воспалительные сигналы далеко от источника. Некоторые ротовые бактерии, например Porphyromonas gingivalis и Fusobacterium nucleatum, даже скрываются внутри иммунных клеток и перемещаются по организму как микробные «троянские кони».
Как ротовые бактерии учатся выживать в кишечнике
Не каждый ротовой микроб, достигший кишечника, может там закрепиться. Те, кому это удаётся, обычно обладают особыми стратегиями выживания. Некоторые штаммы перестраивают свои клеточные оболочки, чтобы выдерживать высокую кислотность или действие желчи; другие питаются сахарами из слизи, покрывающей стенку кишечника, или объединяются с местными бактериями, формируя прочно прилипшие биоплёнки. Одновременно они учатся оставаться незаметными для иммунной системы. Некоторые блокируют способность естественных киллеров и Т-клеток убивать патогены; другие вмешиваются в ранние датчики, которые обычно обнаруживают микробные компоненты и запускают защитные ответы. Сдвигая баланс иммунных клеток в сторону более провоспалительных типов и уменьшая количество регуляторных «тормозов», они создают нишу, в которой возможно длительное, низкоуровневое колонизирование.
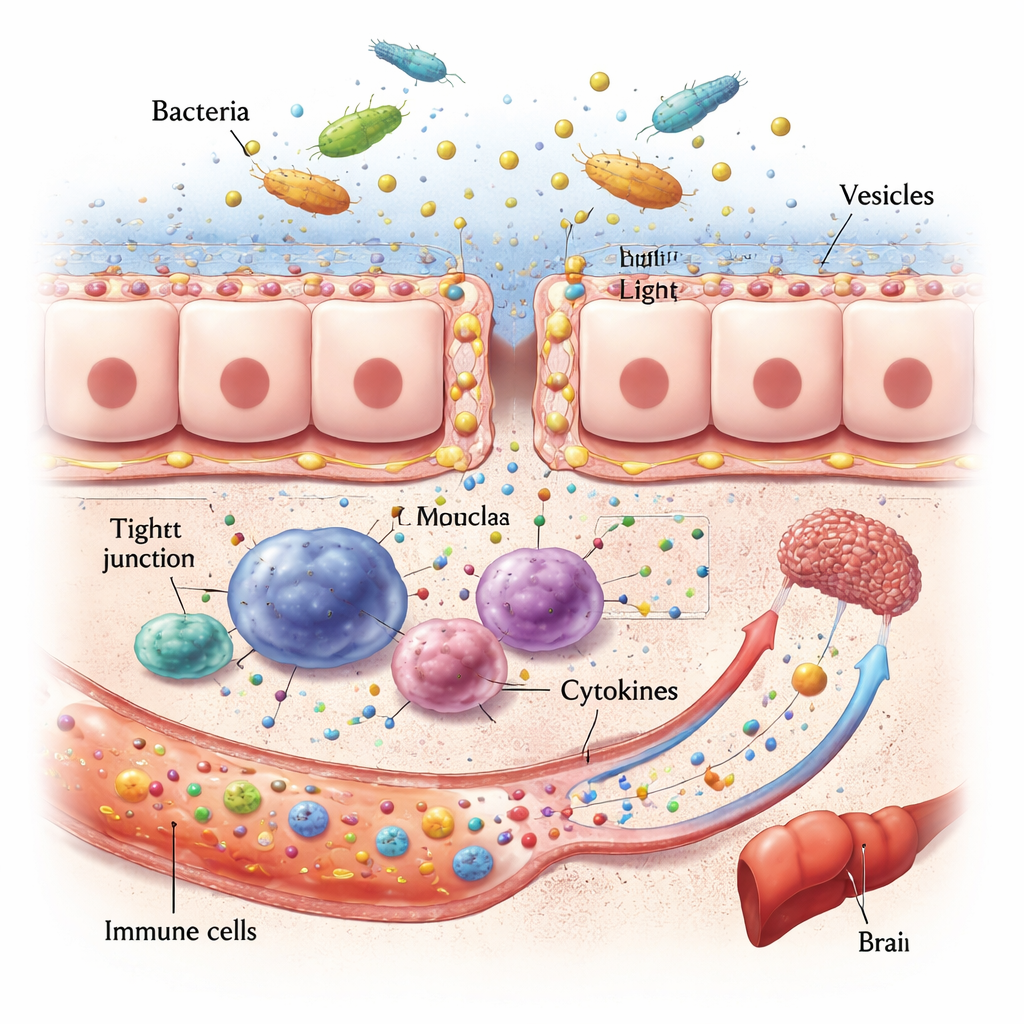
От «дырявого» кишечника до больных органов
После закрепления инвазивные ротовые микробы и их везикулы могут повредить передовую линию защиты кишечника. Они разрушают белки, которые герметично соединяют соседние клетки, истощают слизистую пленку и могут даже напрямую убивать клетки кишечника. Это повышает проницаемость стенки кишечника, позволяя фрагментам бактерий и токсинам просачиваться в кровоток. Там они активируют иммунные клетки и вызывают выброс сигнальных молекул — цитокинов. Поскольку кровь от кишечника направляется прямо в печень, этот орган особенно уязвим: данные на животных и людях связывают ротовые патогены с жировой дистрофией печени, фиброзом и усилением воспаления. Аналогичные пути связывают дисбиоз рта и нарушение кишечника с мозгом, где хроническое воспаление и изменения в микробных метаболитах, по-видимому, усиливают накопление белков, связанных с болезнью Альцгеймера, и нарушают настроение и когнитивные функции.
Новые подходы для вмешательства
Осознание оси «рот–кишечник» открывает многоуровневые стратегии профилактики и терапии. В ротовой полости рутинное лечение пародонта, методы на основе света и природные антимикробные пептиды могут снизить количество вредных бактерий и уменьшить число микробов, попадающих в кишечник. В кишечнике пробиотики, рационы, богатые клетчаткой, и добавки, восстанавливающие уровень короткоцепочечных жирных кислот, помогают восстановить барьер и успокоить чрезмерно активную иммунную систему. В перспективе сложные «орган-на-чипе» устройства, связывающие миниатюрные ткани рта, кишечника, печени и мозга, вместе с крупномасштабными картами того, какие микробы вызывают какие иммунные реакции, могут позволить персонализированные подходы к предотвращению хронических воспалительных заболеваний.
Что это значит для вас
Для неспециалиста основная мысль такова: рот — это не изолированное пространство; его микробы могут формировать здоровье кишечника и через кишечник влиять на весь организм. Когда ротовые бактерии обходят или разрушают естественные барьеры, они могут способствовать длительному воспалению в отдалённых органах, таких как печень и мозг. Авторы приходят к выводу, что защита здоровья полости рта, сохранение кишечного барьера и мягкое управление нашими микробными сообществами с помощью целевых мер могут стать важными инструментами в борьбе с современными хроническими заболеваниями.
Цитирование: Li, C., Fan, Y. & Chen, X. Oral microbiota–driven immune modulation along the oral–gut axis: from local signals to systemic inflammation. npj Biofilms Microbiomes 12, 46 (2026). https://doi.org/10.1038/s41522-026-00912-0
Ключевые слова: ротовой микробиом, кишечный барьер, системное воспаление, заболевания печени, здоровье мозга