Clear Sky Science · ru
Антибиотикотерапия с усилением ферментами снижает количество биопленок до неопределяемого уровня в модели инфекции, связанной с имплантатом
Почему стойкие инфекции имплантатов имеют значение
Замена тазобедренного или коленного сустава меняет жизнь людей к лучшему, но когда бактерии колонизуют металлические имплантаты, они могут образовать слизистые сообщества, называемые биопленками. Эти биопленки действуют как бронированные города, которые защищают микробы и от иммунной системы, и от антибиотиков, что приводит к болезненным, длительным инфекциям, которые очень трудно вылечить. В данном исследовании рассматривается новый двухэтапный подход: сначала ослабляют защиту биопленки, а затем обильно насыщают область высокими дозами антибиотиков — стратегия, которая в будущем может помочь спасти больше имплантатов вместо их замены.
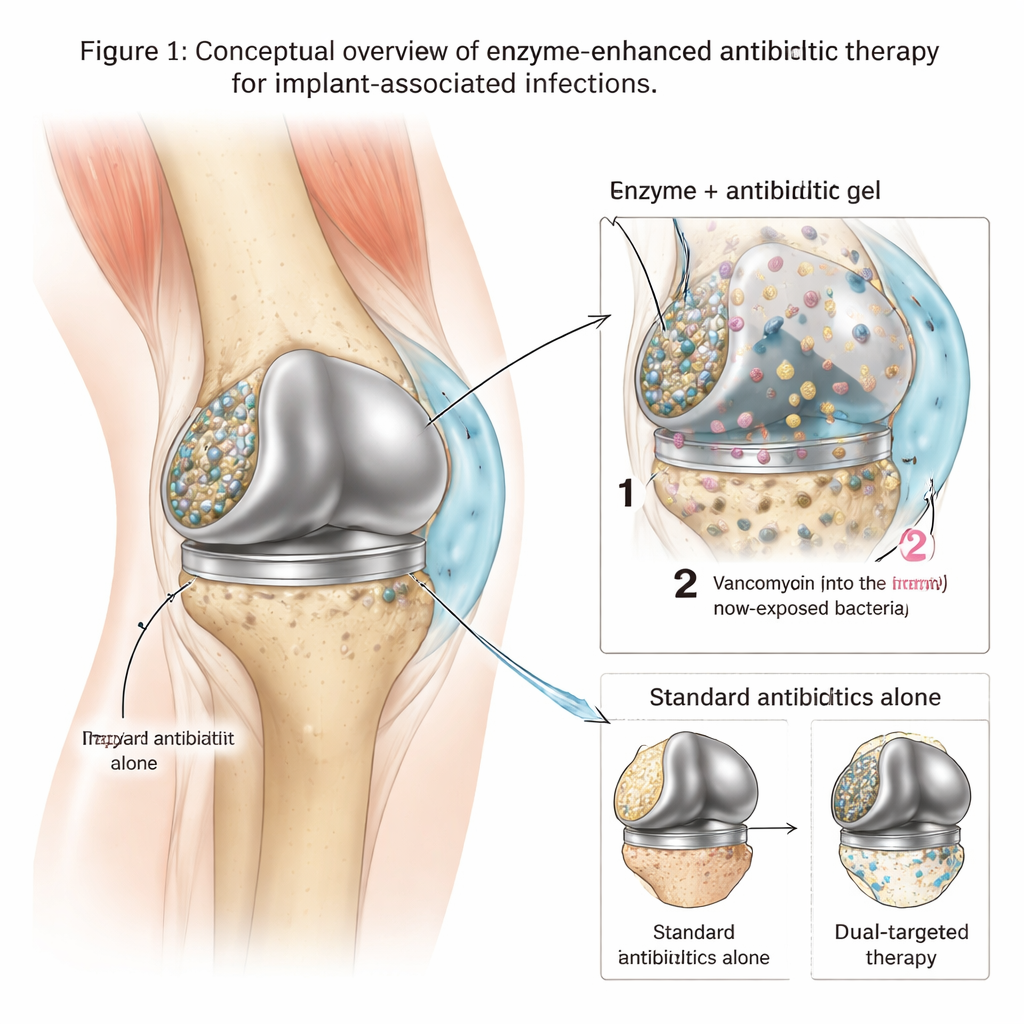
Скрытые укрепления на металлических имплантатах
Когда такие бактерии, как метициллин‑резистентный Staphylococcus aureus (MRSA), прикрепляются к искусственному суставу, они быстро формируют липкую матрицу из ДНК, сахаров и других молекул на металлической поверхности. Внутри этой защищенной биопленки бактерии медленно растут, меняют поведение и могут переносить концентрации антибиотиков в сотни или тысячи раз выше тех, которые убивают свободноплавающие микробы. В результате стандартные методы лечения — даже сильные препараты, такие как ванкомицин — часто не справляются с полной очисткой инфекции, вынуждая пациентов проходить повторные операции или полностью заменять имплантат. Врачам нужны инструменты, которые не только уничтожают бактерии, но и разрушают их защитную крепость, чтобы лекарства могли до них добраться.
Умный гель, доставляющий ферменты и антибиотики
Исследователи разработали локальное средство на основе термочувствительного гидрогеля из полоксамера 407. Этот гель жидкий в холодном состоянии, что облегчает его инъекцию вокруг имплантата, но быстро превращается в мягкое твердое состояние при температуре тела, что помогает ему оставаться на месте. В гель команда загрузила два ключевых компонента: мощный антибиотик (ванкомицин) и коктейль из трех ферментов, разрушающих основные составляющие матрикса биопленки. В лабораторных испытаниях они настроили гель так, чтобы ферменты высвобождались в первую очередь — ослабляя и истончая биопленку, — тогда как ванкомицин высвобождался медленнее в течение нескольких дней, поддерживая очень высокие локальные концентрации препарата прямо там, где живут бактерии.
От чашек Петри до морских свинок
Чтобы проверить, действительно ли стратегия работает, команда сначала протестировала её на биопленках, выращенных на кусочках титана в лаборатории, а затем в модели с морскими свинками, имитирующей инфицированные имплантаты. In vitro два применения геля с ферментами и антибиотиком с интервалом 48 часов уменьшили количество живых бактерий на металлических поверхностях более чем в 100 000 раз и почти полностью уничтожили массу биопленки. В опытах на животных исследователи хирургически разместили перфорированные камеры с титановые шариками под кожей, инфицировали их MRSA, а затем лечили разными комбинациями системных антибиотиков и локальных гелей. Наиболее эффективный режим сочетал: (1) локальный гель, содержащий и ферменты, и ванкомицин, примененный дважды, и (2) системное лечение ванкомицином в комбинации со вторым антибиотиком — рифампицином, который особенно хорошо проникает в биопленки.
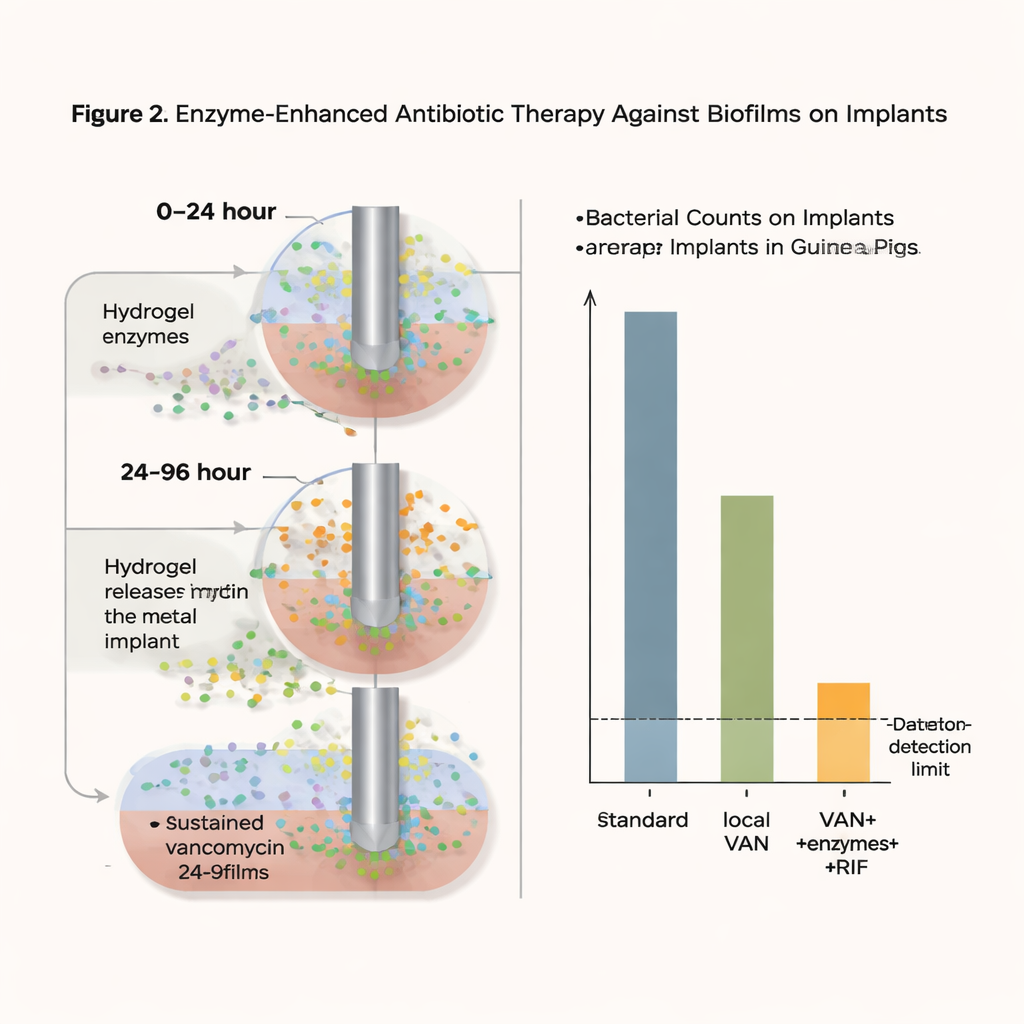
Чего добился новый подход
С этой интенсивной, но локализованной стратегией число бактерий на материале имплантата снизилось до предела обнаружения — фактически «необнаруживаемые бактерии» в этой модели — в 75 процентов обработанных камер через день после окончания терапии и в 37,5 процента даже через пять дней. Важно, что не наблюдалось увеличения устойчивости к ванкомицину, а высокие локальные уровни ванкомицина, по-видимому, препятствовали появлению штаммов, устойчивых к рифампицину. Тесты безопасности на культурах клеток и в реконструированной модели человеческой кожи не выявили признаков токсичности или раздражения от формул геля. Хотя в некоторых случаях всё же отмечался слабый повторный рост бактерий и период лечения был короче, чем обычно у пациентов, результаты показывают, что сочетание ферментов, разрушающих биопленку, и длительной локальной доставки антибиотика может значительно сократить иначе стойкие инфекции.
Что это может означать для пациентов
Для людей, столкнувшихся с инфекциями, связанными с имплантатами, эта работа указывает на будущее, в котором хирурги могли бы вводить умный гель вокруг инфицированного сустава, а не немедленно удалять или заменять конструкцию. Сначала ослабив щит биопленки, а затем затопив область высокими, длительно поддерживаемыми дозами антибиотиков — при поддержке системного лечения — эта двухцелевaя стратегия нацелена на снижение числа бактерий до неопределяемого уровня и уменьшение риска возникновения резистентности. Хотя требуются дополнительные исследования, более длительные курсы лечения и клинические испытания на людях, подход предлагает перспективную модель превращения некоторых из самых упорных ортопедических инфекций в более управляемые и, возможно, излечимые проблемы.
Цитирование: Buzisa Mbuku, R., Poilvache, H., Maigret, L. et al. Enzymes-enhanced antibiotic therapy reduces biofilms to undetectable levels in an implant-associated infection model. npj Biofilms Microbiomes 12, 44 (2026). https://doi.org/10.1038/s41522-026-00910-2
Ключевые слова: инфекция биоплени, ортопедические имплантаты, ванкомицин, ферментная терапия, рифампицин