Clear Sky Science · ru
Теоретическое исследование протоколов лечения инфекций протезированных суставов комбинациями антибиотиков и бактериофагов
Почему инфекции имплантатов суставов важны
Замена тазобедренного или коленного сустава изменила жизнь миллионов людей, вернув им возможность ходить без боли. Но когда бактерии заселяют искусственные суставы, они могут образовывать слизистые сообщества — биопленки, которые крепко прилипают к металлу и пластику. Как только биопленка формируется, обычные дозы антибиотиков и иммунная система часто не справляются с её уничтожением, иногда вынуждая пациента переносить повторные операции. В этом исследовании спрашивают, может ли добавление вирусов, специфически атакующих бактерии — бактериофагов или фагов — к стандартным антибиотикам предложить лучший способ лечения этих упорных инфекций.
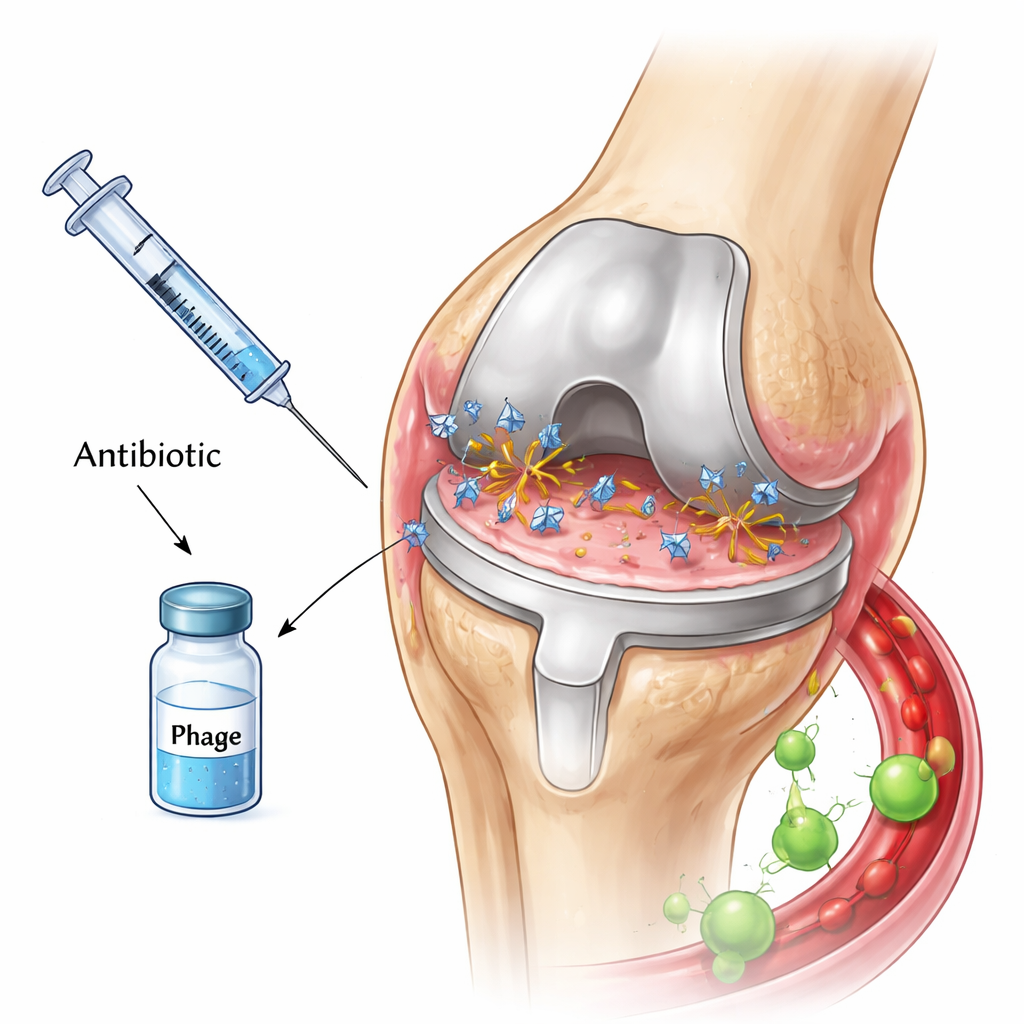
Крошечные вирусы, охотящиеся на бактерии
Фаги — естественные хищники бактерий. Они прикрепляются к бактериальной клетке, вводят в неё свой генетический материал, превращают клетку в «фабрику» вирусов и в конце концов разрывают её, выпуская рой новых фагов. Некоторые фаги также несут ферменты, способные расщеплять липкое вещество, окружающее биопленки, потенциально разрушая защитные слои, которые оберегают бактерии от препаратов. Благодаря этим свойствам многие исследователи надеются, что сочетание фагов с антибиотиками сможет дать мощный комбинированный эффект против инфекций протезов, особенно когда бактерии становятся устойчивыми к антибиотикам.
Создание инфекций внутри компьютера
Вместо того чтобы сразу переходить к опытам на животных или клиническим испытаниям, авторы сначала построили подробную математическую и компьютерную модель инфекции протезированного сустава. Их виртуальная система имела две основные зоны: свободноплавающие бактерии в жидкостях организма и бактерии, встроенные в биопленку на поверхности имплантата. Модель также отслеживала иммунные клетки, питательные вещества для роста бактерий, антибиотики и фаги, все перемещающиеся внутрь и наружу сустава. Меняя такие условия, как доза препарата, время введения и наличие антибиотикорезистентных бактерий, они могли исследовать множество схем лечения, которые было бы трудно, дорого или долго проверять на реальных пациентах.
Когда лекарства действуют по‑одиночке и вместе
Симуляции показали, что ни иммунная система, ни одни только антибиотики не справляются легко с биопленочными инфекциями. Антибиотики сильно снижали число свободноплавающих бактерий, но едва затрагивали популяцию в биопленке. Фаги могли сначала эффективнее сдерживать инфекцию, но вызывали циклы бума и падения: когда фаги убивали бактерии, их жертвы становились слишком редкими, что приводило к снижению числа фагов и восстановлению бактериальной популяции. Когда антибиотики и фаги вводили одновременно, исход, как правило, определялся антибиотиком, и добавление фагов часто давало лишь немного дополнительного эффекта по сравнению с антибиотиком в одиночку.
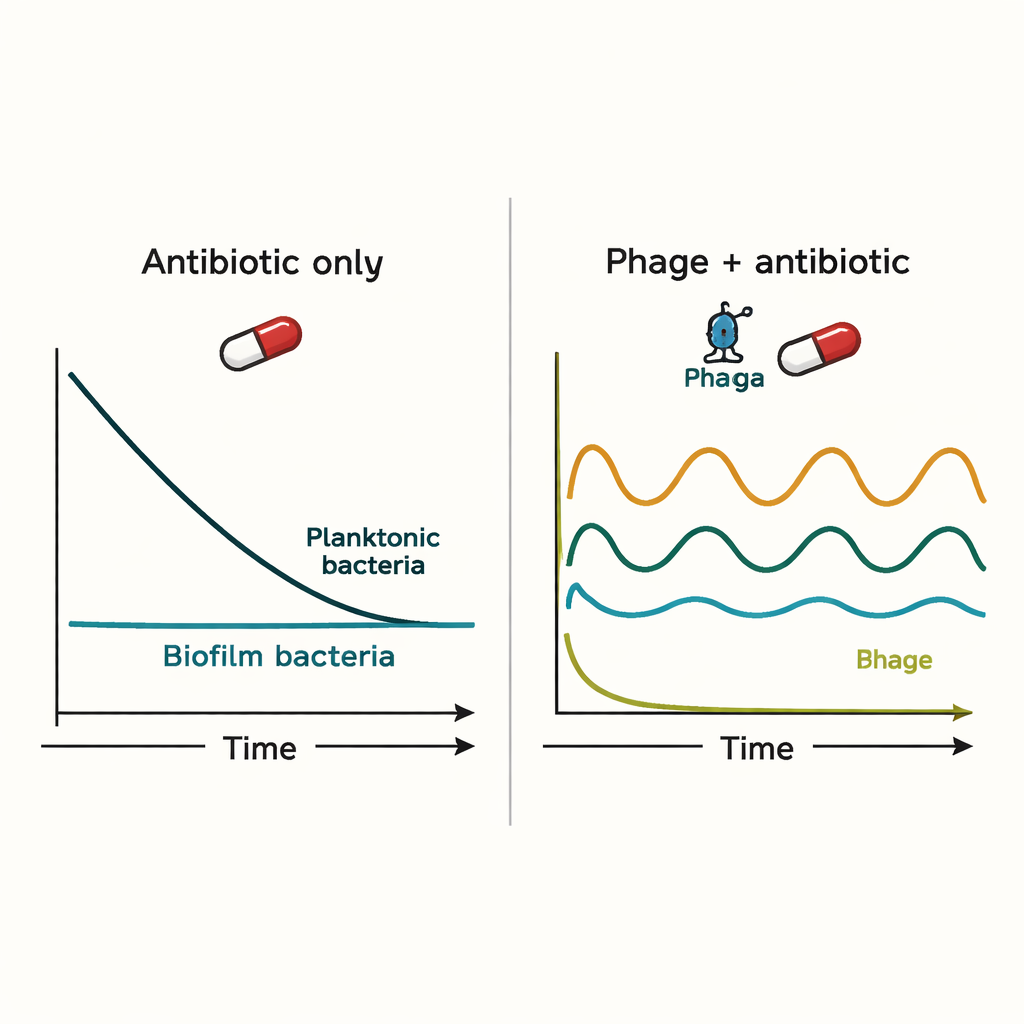
Особая роль времени и резистентности
Модель выглядела более обнадеживающей при включении антибиотикорезистентных бактерий. Фаги могли атаковать эти резистентные клетки и иногда полностью их устранять. Если лечение фагами начинали первым, а антибиотики добавляли спустя несколько часов, комбинированная стратегия снижала количество свободноплавающих бактерий на несколько порядков и устраняла резистентные субпопуляции в симуляциях. Тем не менее бактерии, ассоциированные с биопленкой, полностью не исчезали; их численность удерживалась на более низком уровне, с которым иммунной системе могло быть легче справиться. Это указывает на то, что фаги скорее служат вспомогательным средством — не волшебной пулями, а инструментом для предотвращения резистентности и контроля инфекции.
Что это значит для пациентов и врачей
Для людей с инфицированным имплантатом эта работа несёт и предостережение, и надежду. Модель указывает, что простое добавление фагов к стандартным антибиотикам вряд ли само по себе вылечит глубокие биопленочные инфекции. Тем не менее фаги могут быть ценными: они способны уничтожать антибиотикорезистентные бактерии и сокращать общее число возбудителей до уровня, с которым организм может справиться, особенно если их вводить до или с продуманной синхронизацией с антибиотиками. Авторы подчеркивают, что это теоретические предсказания, а не клинические доказательства. Главная их мысль — что необходимы вдумчивые эксперименты, направляемые такими моделями, чтобы выявить, когда фаговая терапия действительно может улучшить исходы для пациентов с инфекциями протезированных суставов.
Цитирование: Levin, B.R., Gil-Gil, T., Berryhill, B.A. et al. A theoretical exploration of protocols for treating prosthetic joint infections with combinations of antibiotics and bacteriophage. npj Biofilms Microbiomes 12, 51 (2026). https://doi.org/10.1038/s41522-025-00908-2
Ключевые слова: инфекция протеза сустава, биопленка, терапия бактериофагами, антибиотикорезистентность, математическое моделирование