Clear Sky Science · ru
Стадии образования биомолекулярных конденсатов при сборке про‑β‑карбоксисомы
Почему крошечные углеродные фабрики имеют значение
Цепи питания на Земле зависят от фотосинтеза, однако ключевой фермент, который извлекает диоксид углерода (CO2) из воздуха, Rubisco, работает медленно и легко путает CO2 с кислородом. Цианобактерии — микроскопические фотосинтезирующие микроорганизмы — давно решили эту проблему, собирая белковые «микрофабрики», называемые карбоксисомами, которые концентрируют CO2 вокруг Rubisco. В этом исследовании раскрывается, как один важный адаптерный комплекс, состоящий из белков ApN и CM, самоорганизуется по этапам, чтобы помочь построить рабочую карбоксисому. Понимание этой хореографии может направить усилия по внедрению похожих систем повышения CO2 в сельскохозяйственные растения и повышению урожайности.
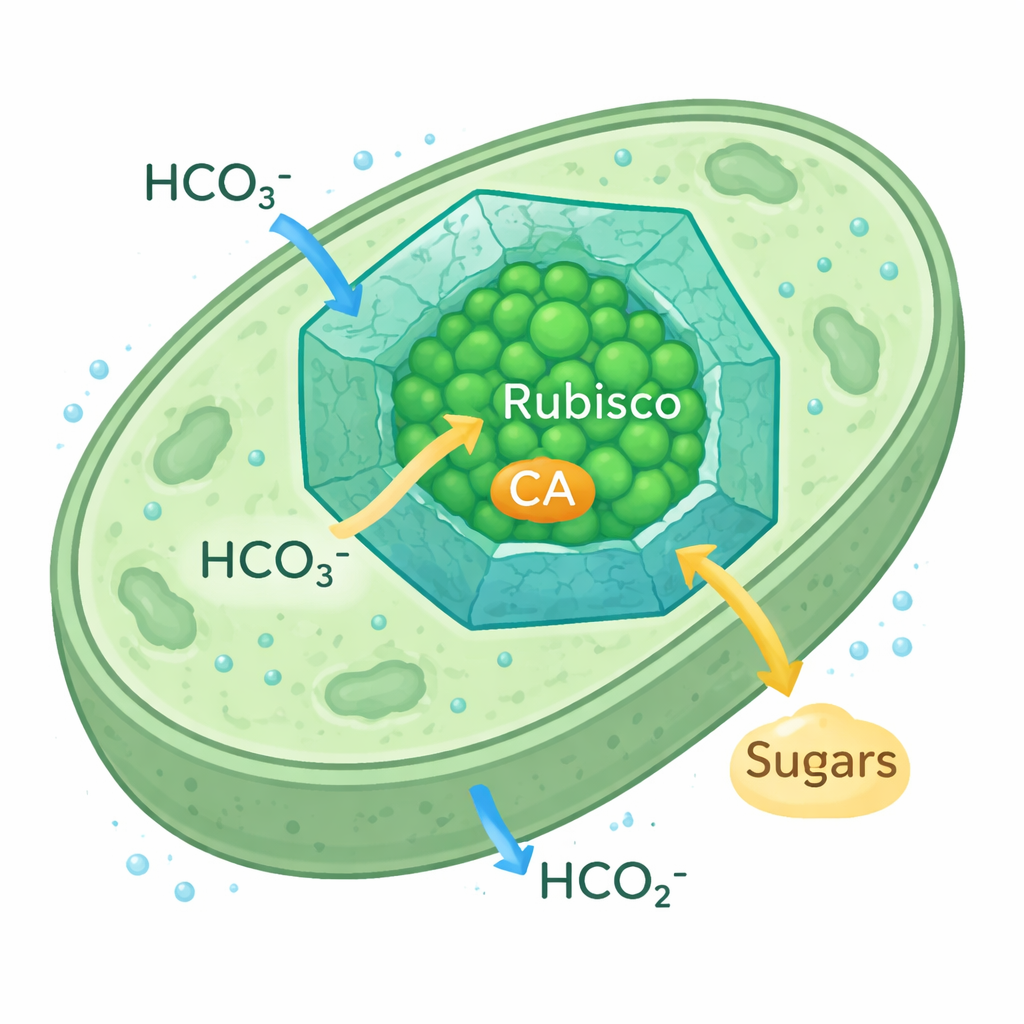
Как микробы усиливают улавливание углерода
Карбоксисомы цианобактерий — это крошечные икосаэдрические белковые компартменты, расположенные внутри клетки. Их белковая оболочка пропускает ионы гидрокарбоната, одновременно замедляя утечку CO2, создавая вокруг Rubisco и его партнёра карбоангидразы (CA) зону с высокой концентрацией CO2. Этот механизм концентрирования CO2 позволяет цианобактериям процветать даже при низком содержании CO2 в окружающей среде. Поскольку форма Rubisco, используемая в этих карбоксисомах, напоминает растительный Rubisco, исследователи рассматривают их как реалистичную модель для перепроектирования хлоропластов растений с целью более эффективного захвата углерода.
Фрагмент головоломки, который связывается с оболочкой
Прежде чем образуется твёрдая белковая оболочка, цианобактерии сначала формируют мягкий, похожий на каплю «про‑карбоксисомный» конденсат. Предыдущие работы показали, что каркасный белок CM собирает Rubisco и CA в этой капле. Недоставал звено: как адаптерный белок оболочки ApN вступает в эту структуру и затем соединяется с оболочечными белками. Авторы обнаружили, что когда ApN синтезируется в одиночку, он образует четырёхчастный пучок, который не взаимодействует с другими компонентами карбоксисомы. В таком состоянии ApN не втягивается в капли с Rubisco, CM и CA, что указывает на то, что при реальной сборке карбоксисомы используется другая форма ApN.
Совместно собранные адаптеры и редокс‑переключатель
Рассматривая генетическую организацию в цианобактериях, команда заметила, что apn расположен сразу за cm в одном опероне, поэтому оба белка чаще всего синтезируются одновременно. Имитируя это в бактериях, они ко‑экспрессировали ApN и CM с общей ДНК. При таких условиях ApN перестал образовывать самостоятельный тетрамер. Вместо этого три субъединицы ApN и одна субъединица CM собрали специфический четырёхчастный адаптерный комплекс, обозначенный (ApN)3:CM. Этот гетеро‑комплекс легко связывался с Rubisco, CA и CM и мог входить в конденсаты. Структурное моделирование и крио‑электронная микроскопия показали, что ApN и CM связываются через точно настроенный «язычок‑впадина» интерфейс; при мутациях ключевых остатков ApN в этом интерфейсе адаптер не формировался, и клетки не могли построить правильные карбоксисомы.
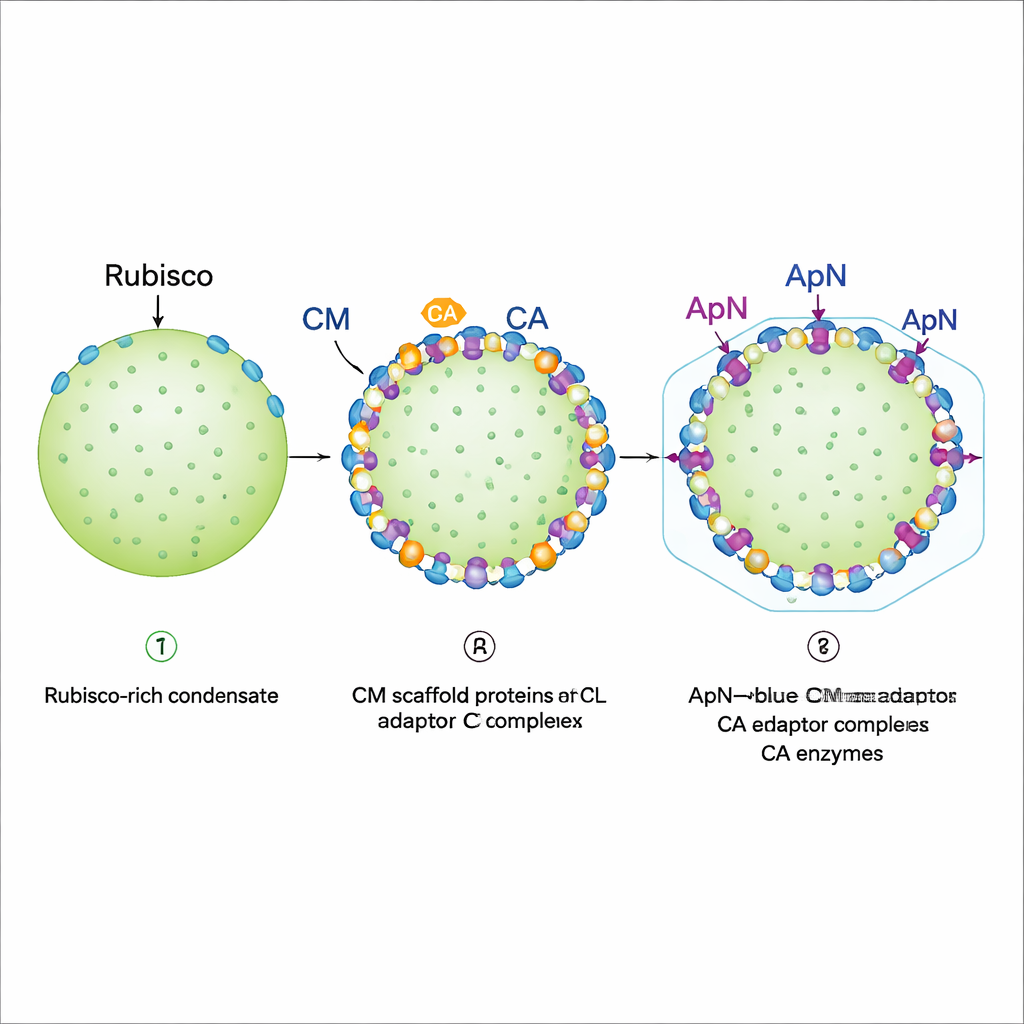
Позиционирование на краю и подготовка к оболочке
Флуоресцентная визуализация реконституированных капель выявила ступенчатую программу сборки. Сначала Rubisco, полноразмерный CM и более короткий вариант CM формируют плотный конденсат, который ведёт себя как гель: Rubisco по сути зафиксирован. Затем добавляют CA и комплекс (ApN)3:CM. Оба преимущественно оседают на внешнем ободе существующей капли, при условии что CA поступает раньше или одновременно с (ApN)3:CM. Такая локализация по краю критична, потому что хвост ApN несёт «пептид инкапсуляции», который связывает оболочечные белки. Авторы также обнаружили встроенный редокс‑переключатель: по мере того как внутренность созревающей карбоксисомы становится более окисляющей, две консервативные цистеиновые остатка в ApN могут окисляться, смещая адаптер от тетрамера (ApN)3:CM к тримеру (ApN)2:CM. В живых цианобактериальных клетках изменение этих цистеинов замедляло рост и приводило к образованию увеличенных по размеру, но всё ещё функциональных карбоксисом, что подчёркивает их роль в точной настройке созревания.
Уроки для создания лучших культур
Для неспециалиста эти молекулярные детали могут показаться архаичными, но их суть проста: важны время и партнёрство. Работа показывает, что ApN должен синтезироваться совместно с CM, чтобы избежать образования бесполезных самосборок и вместо этого стать адаптером, который располагается на поверхности про‑карбоксисомы, готовым рекрутировать оболочку. Затем чувствительный к редокс‑состоянию шаг помогает перестроить этот адаптер по мере закрывания компартмента и изменения его внутренней химии. Для инженеров растений, стремящихся пересадить цианобактериальную систему концентрирования CO2 в культуры, исследование подчёркивает: недостаточно перенести отдельные части; необходимо также уважать порядок, соотношения и химические триггеры, которые в природе направляют сборку карбоксисомы.
Цитирование: Zang, K., Hong, X., Nguyen, N.D. et al. Stages of biomolecular condensate formation in pro-β-carboxysome assembly. Nat. Plants 12, 447–464 (2026). https://doi.org/10.1038/s41477-026-02227-6
Ключевые слова: сборка карбоксисомы, цианобактериальный механизм концентрирования CO2, конденсаты Rubisco, биомолекулярные конденсаты, синтетическое фотосинтезирование