Clear Sky Science · ru
Многоуровневый молекулярный профиль помогает в диагностике и таргетной терапии десмопластической мелкой круглоклеточной опухоли
Редкая опухоль, нуждающаяся в лучших ответах
Десмопластическая мелкая круглоклеточная опухоль (DSRCT) — исключительно редкая и агрессивная злокачественная опухоль, которая преимущественно поражает детей, подростков и молодых взрослых. Из‑за своей редкости и способности микроописательно имитировать другие опухоли врачам нередко бывает трудно поставить точный диагноз и подобрать эффективное лечение. В этом исследовании задают простой, но важный вопрос: если всесторонне проанализировать опухоли DSRCT на нескольких молекулярных уровнях — не только ДНК, но и РНК, белковых паттернов и химических меток на ДНК — можно ли точнее диагностировать заболевание и выявить новые, более точные варианты терапии для пациентов, у которых исчерпаны стандартные методы лечения?
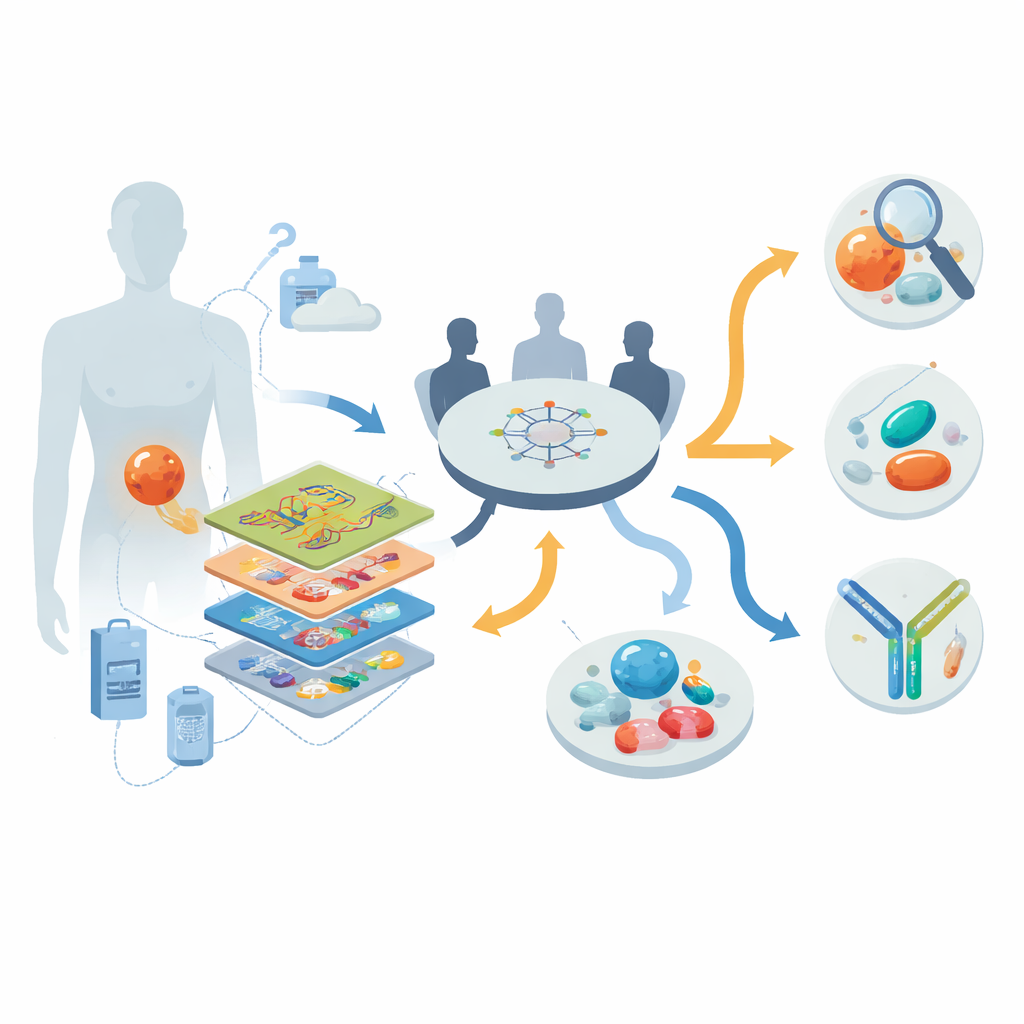
Заглядывая в опухоль слой за слоем
Исследователи работали в рамках национальной программы прецизионной онкологии в Германии, набрав 30 человек с распространённой, в основном рефрактерной DSRCT в период с 2013 по 2022 год. Для каждого пациента они применили «мультиомный» набор методов: секвенирование всего генома или экзома для изучения ДНК; секвенирование РНК, чтобы увидеть, какие гены активно включены; профилирование метилирования ДНК для фиксации эпигенетических отпечатков; и у девяти пациентов — детальные измерения белков и фосфопротеинов, которые показывают, какие сигнальные пути реально активны. Мультидисциплинарный опухолевой консилиум затем совместно рассматривал эти данные вместе с клинической историей каждого пациента, чтобы выработать индивидуальные рекомендации по уточнению диагноза, таргетным препаратам и клиническим исследованиям.
Исправление ошибочных диагнозов и обнаружение скрытых мишеней
Одним из ярких результатов было то, насколько часто глубокое профилирование корректировало первоначальный диагноз. У восьми из 30 пациентов опухоли, первоначально обозначенные как другие образования — например, рак неустановленного происхождения или нечетко определённые саркомы — были переклассифицированы как DSRCT после выявления характерной генной слияния (EWSR1::WT1) и типичного паттерна метилирования. В то же время ДНК этих опухолей оказалась относительно «тихой»: мутаций было мало, а изменения числа копий встречались лишь эпизодически, поэтому классический подход «мутация гена = лечебная мишень» давал мало результатов. Самые ценные подсказки поступали от уровней РНК и белков. Сравнивая активность генов в DSRCT с сотнями других сарком, команда выявила повторяющееся сверхэкспрессирование нескольких поверхностных молекул и сигнальных ферментов, на которые теоретически можно воздействовать существующими или развивающимися препаратами.
От молекулярных сигналов к индивидуальным лечениям
Опираясь на эти паттерны, консилиум вынес 107 молекулярно обоснованных управленческих рекомендаций для 28 из 30 пациентов. Большинство рекомендаций касалось препаратов, блокирующих тирозинкиназы — ключевые ферменты, драйвящие рост клеток и ангиогенез — либо более новых стратегий, нацеленных на высокоэкспрессируемые поверхностные белки. Примерами были ингибиторы киназ малых молекул, такие как пазопаниб; пептидная радиотерапия, нацеленная на рецепторы соматостатина; экспериментальные CAR‑T‑клетки против адгезионного молекулы CLDN6; и конъюгаты антител с цитотоксинами, доставляющие токсины в клетки, несущие рецептор ERBB2 (HER2). Семнадцати пациентам было рекомендовано участие в клинических исследованиях, соответствующих биомаркерам, что подчёркивает: детальные молекулярные данные могут открыть доступ к исследованиям, которые в противном случае были бы труднодоступны для людей с ультраредким заболеванием.
Реальный эффект у тяжело пролеченных пациентов
Из всех рекомендованных персонализированных стратегий 16 были фактически применены у 13 пациентов, причём решения опирались на сигналы на уровне РНК и иногда уточнялись данными по фосфопротеинам. Несмотря на то что эти пациенты уже прошли через несколько курсов химиотерапии и локальных вмешательств, у восьми из 13 удалось добиться контроля болезни — у пятерых наблюдалось частичное уменьшение опухоли, у трёх — стабилизация. Многоцелевые ингибиторы тирозинкиназ, чаще всего пазопаниб, принесли значимую и порой длительную пользу нескольким пациентам, особенно когда известные мишени препарата были явно гиперактивны в опухоли. Возможно, особенно примечательны два пациента с высокой экспрессией ERBB2, получившие конъюгат антитела с препаратом трастузумаб дерукстекан (T‑DXd). Оба испытали пролонгированные ответы, длящихся до двух лет и более, несмотря на то, что они исчерпали многие предыдущие линии терапии и несмотря на то, что рецептор ERBB2 не демонстрировал типичного сильного паттерна активации, обычно необходимого для классических ERBB2‑блокирующих препаратов.
Что это означает для пациентов и будущей помощи
Для людей с DSRCT исследование даёт осторожно оптимистичное послание. Хотя у этой опухоли мало очевидных ДНК‑мутаций, которые можно было бы эксплуатировать, анализ нескольких молекулярных уровней одновременно способен и корректировать ошибочные диагнозы, и выявлять действующие уязвимости, невидимые при стандартных тестах. Работа показывает, что даже при редком и агрессивном заболевании биология‑ориентированный подход может приносить реальную клиническую пользу, включая длительные ответы на препараты вроде пазопаниба и трастузумаб дерукстекана. В более широком смысле это аргумент в пользу того, что пациенты с DSRCT — и, по аналогии, с другими ультраредкими опухолями — выиграют от рутинного доступа к комплексному молекулярному профилированию и экспертному обзору, что проложит путь к будущим испытаниям, в которых лечение выбирается не только по типу опухоли, но и по уникальному молекулярному отпечатку рака каждого человека.
Цитирование: Renner, M., Oleś, M., Paramasivam, N. et al. Multi-layered molecular profiling informs the diagnosis and targeted therapy of desmoplastic small round cell tumor. Nat Commun 17, 3397 (2026). https://doi.org/10.1038/s41467-026-71636-0
Ключевые слова: десмопластическая мелкая круглоклеточная опухоль, прецизионная онкология, мультиомное профилирование, таргетная терапия, конъюгаты антител с лекарствами