Clear Sky Science · ru
Взаимодействие SLC33A1-зависимой и -независимой O-ацетилирования сиаловой кислоты в аппарате Гольджи при каталозе CASD1
Как крошечные изменения сахаров могут влиять на здоровье и болезни
Клетки покрыты сложными цепочками сахаров, которые действуют как молекулярные удостоверения личности, направляя иммунитет, развитие и даже то, как вирусы прикрепляются к клетке. В этом исследовании рассматривается тонкая, но мощная модификация этих сахаров — добавление небольших химических «шапочек», ацетильных групп, к терминальному сахару, называемому сиаловой кислотой — и выявляется неожиданная двухчастная молекулярная машина, контролирующая этот процесс внутри аппарата Гольджи. Понимание этой скрытой системы помогает объяснить ряд тяжёлых неврологических расстройств и даёт ключи к тому, как клетки тонко настраивают свою поверхность в норме и при болезни. 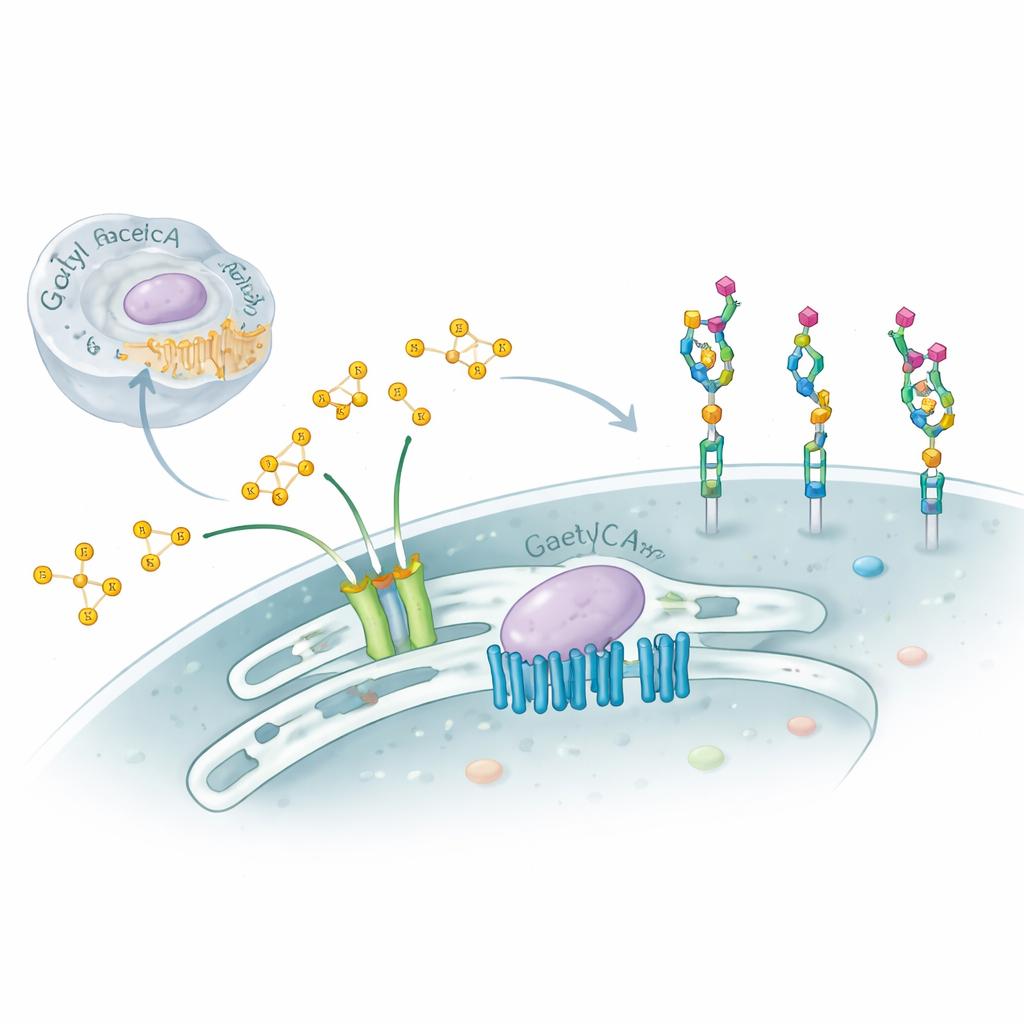
Особые сахара на поверхности клетки
Сиаловые кислоты располагаются на наружных концах многих клеточных сахарных цепочек на белках и липидах, особенно на молекулах, называемых ганглиозидами в мозге. Небольшие изменения сиаловых кислот — например добавление одной или двух ацетильных групп в определённых положениях — позволяют клеткам маскировать существующие сайты распознавания или создавать новые. Вирусы, такие как вирус гриппа типа C и некоторые коронавирусы, специально распознают эти модифицированные сахара, а ацетилированные ганглиозиды могут влиять на выживание нервных клеток и на рост опухолей. Тем не менее внутренние механизмы клеточной машины, которая размещает эти ацетильные группы в аппарате Гольджи, долго оставались слабо понятными.
Транспортер и фермент работают рука об руку
Исследователи сосредоточились на двух белках, локализованных вблизи или внутри аппарата Гольджи: SLC33A1 — транспортере, переносящем ацетил‑CoA (основной донор ацетильных групп в клетке) через мембраны, и CASD1 — ферменте, известном переносом ацетильных групп на сиаловые кислоты. С помощью редактирования генов в клеточных линиях человека и хомяка они удалили SLC33A1 и проследили изменения в определённых ганглиозидах. Клетки без SLC33A1 всё ещё могли синтезировать базовые ганглиозиды GD3 и GD2, но полностью теряли их 9‑O‑ацетилированные формы — характерную модификацию, связанную с раком и нервной функцией. Восстановление человеческого SLC33A1 возвращало эти ацетилированные ганглиозиды, что демонстрирует, что SLC33A1 является ключевым поставщиком ацетил‑CoA для этого пути. 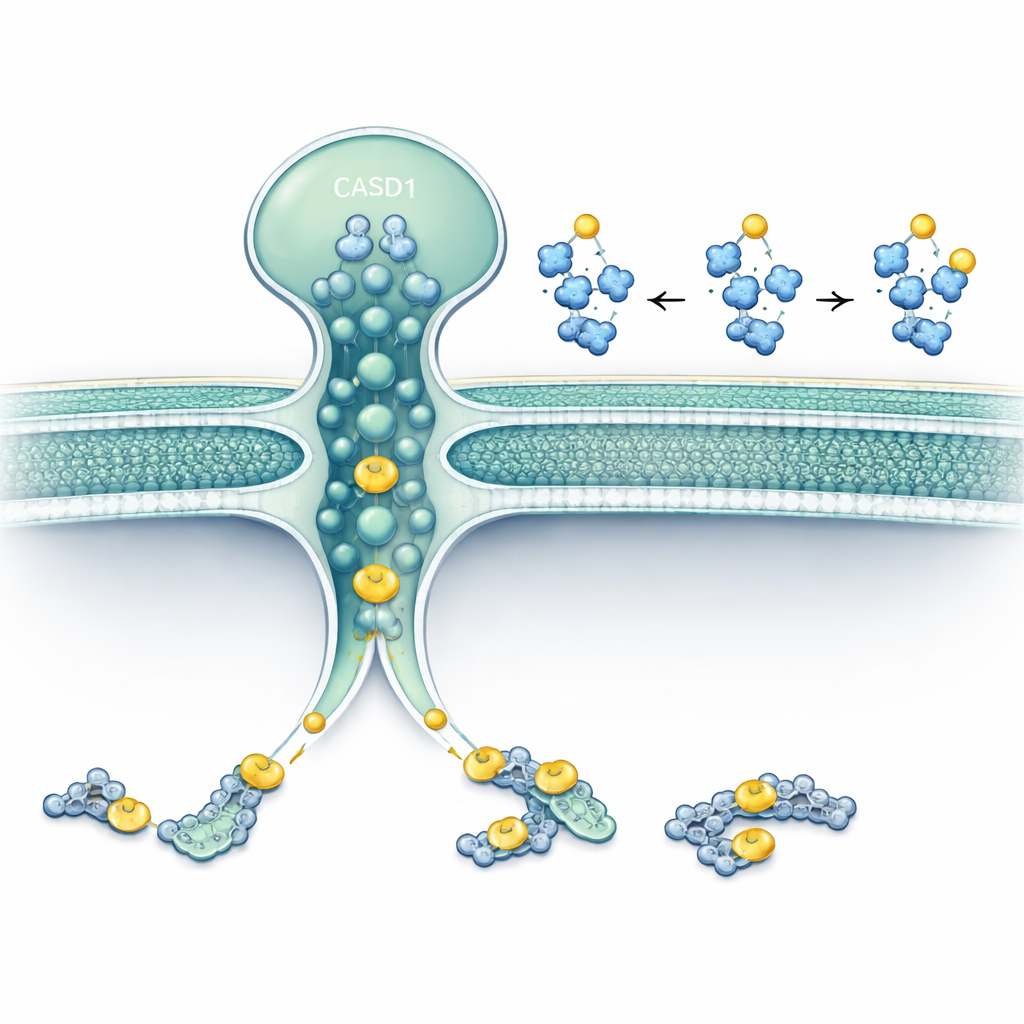
Мутации у пациентов показывают медицинскую значимость
SLC33A1 был вовлечён в несколько редких неврологических состояний, включая тяжёлое детское заболевание (синдром Хуппке–Бренделя), форму наследственной спастической параплегии и поздноначавшуюся церебеллярную атаксию. Команда воспроизвела четыре вариантов SLC33A1, обнаруженных у пациентов, в клетках без нормального транспортера и проверила, могут ли эти изменённые белки восстановить ацетилирование ганглиозидов. Все четыре варианта показали сниженную функцию, а наиболее тяжёлые мутации с детским началом практически не восстанавливали ацетилирование. Опираясь на недавно разрешённую трёхмерную структуру SLC33A1, авторы картировали эти мутации на структуру белка и показали, как они, вероятно, нарушают его архитектуру или способность связывать ацетил‑CoA. Это сильно указывает на то, что нарушенное ацетилирование ганглиозидов вносит вклад в неврологические симптомы у пациентов.
Скрытый второй активный сайт в CASD1
Работа также выявила неожиданный поворот: CASD1 по‑видимому является двухфункциональным ферментом. Его известная часть в люмине Гольджи использует ацетил‑CoA, доставляемый SLC33A1. Но при нокауте SLC33A1 клетки всё же могли в определённых условиях добавить одну ацетильную группу на некоторые сиаловые кислоты, хотя и не могли добавить вторую ацетильную группу, необходимую для более сложных паттернов. С помощью продвинутого предсказания структуры и молекулярных симуляций авторы показали, что трансмембранная часть CASD1 по форме напоминает известный трансмембранный ацетилтрансфераз из лизосом. Они выделили ключевые аминокислоты в этой области, которые связывают ацетил‑CoA на цитозольной стороне и передают его ацетильную группу через мембрану непосредственно на сиаловую кислоту. При мутациях в этих остатках CASD1 терял эту вторую активность как в пробирочных экспериментах, так и в живых клетках.
Два пути — один тонко настроенный сахарный код
В совокупности данные поддерживают модель «двух каталитических сайтов». Один путь зависит от того, что SLC33A1 приносит ацетил‑CoA в люмен Гольджи, где люминальная домен CASD1 добавляет ацетильную группу к сиаловой кислоте, обеспечивая как простые, так и двойные паттерны ацетилирования. Другой путь встроен в трансмембранное ядро CASD1, которое напрямую использует цитозольный ацетил‑CoA и может выполнять базовый уровень ацетилирования даже при отсутствии SLC33A1. Для непрофессионала это означает, что один фермент, подпитываемый двумя разными источниками ацетиля, «ставит» тонкие «знаки пунктуации» на клеточно‑поверхностных сахарах. Когда транспортер или любая из частей фермента дефектна, эти знаки смещены или отсутствуют — что может способствовать объяснению некоторых нейроразвитийных и нейродегенеративных заболеваний и подчёркивает новый уровень регуляции в том, как клетки формируют свою внешнюю идентичность.
Цитирование: Albers, M., Bosse, L., Schröter, L. et al. Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis. Nat Commun 17, 3156 (2026). https://doi.org/10.1038/s41467-026-71333-y
Ключевые слова: сиаловая кислота, ацетилирование в Гольджи, ганглиозиды, SLC33A1, CASD1