Clear Sky Science · ru
Структурная динамика комплекса миднолин–протеасома при утилизации субстратов без участия убиквитина
Как клетки быстро выносят мусор
Внутри каждой клетки белки постоянно синтезируются и разрушаются. Многие из них помечаются небольшой молекулой — убиквитином — прежде чем попадут в основной утилизационный аппарат клетки, протеасому. Но некоторые ядерные белки необходимо удалить настолько быстро, что на маркировку времени нет. В этом исследовании показано, как малоизвестный вспомогательный белок миднолин напрямую встраивается в протеасому, чтобы выводить эти срочные мишени, давая представление о том, как клетки обеспечивают жесткий и быстрый контроль активности генов.
Короткий путь к клеточной «шредерной машине»
26S-протеасома — это бочкообразный комплекс, разрушающий белки на мелкие фрагменты. Традиционно она распознаёт мишени по цепочкам убиквитина, прикреплённым к ним. Последние работы выявили альтернативный маршрут: «короткий путь», при котором миднолин сопровождает определённые ядерные белки — особенно продукты генов мгновенного ответа, быстро включающих и выключающих транскрипцию — прямо к протеасоме без каких-либо убиквитиновых меток. Эти белки, например факторы транскрипции, участвующие в стрессовых и воспалительных ответах, должны появляться и исчезать в течение нескольких минут. Новая статья сочетает высокоразрешающую крио-электронную микроскопию с биохимическими экспериментами, чтобы почти покадрово показать, как миднолин закрепляется на протеасоме и ориентирует свой груз для разрушения.
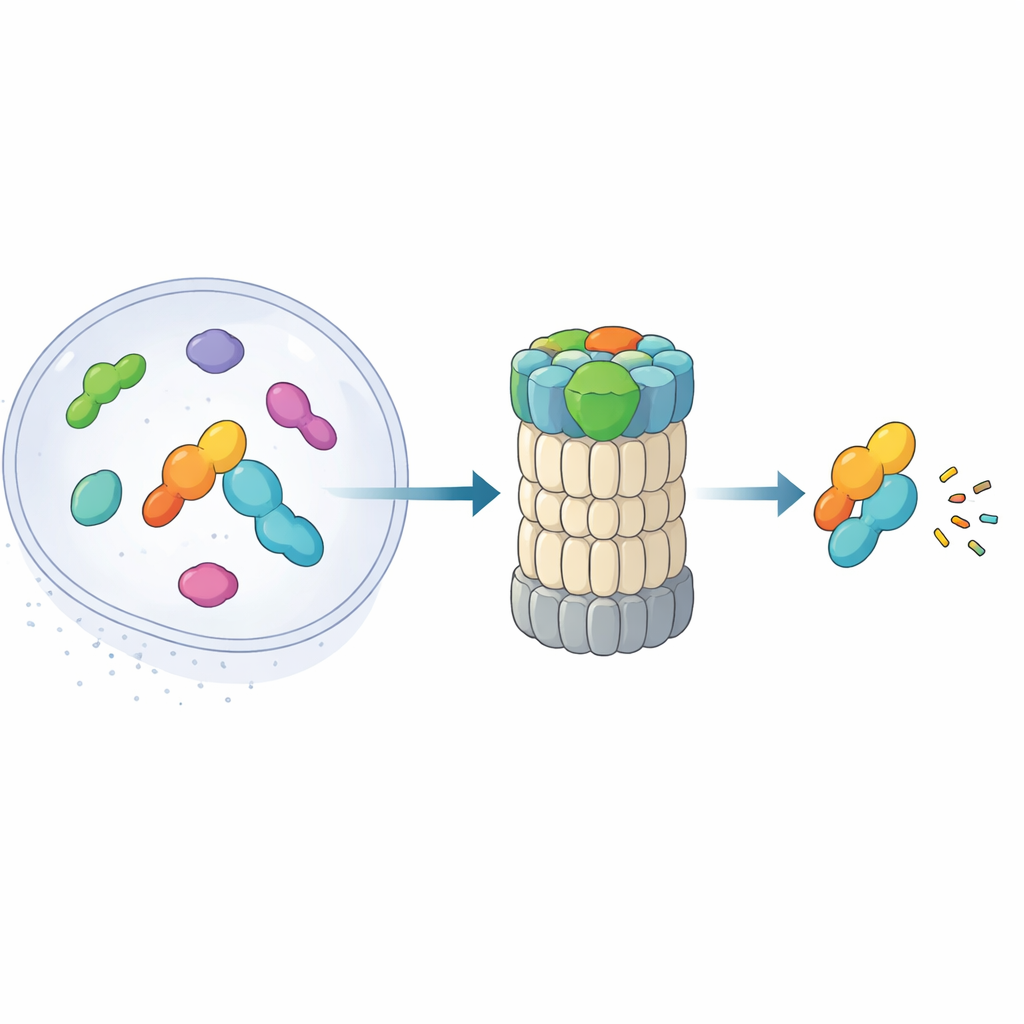
Трёхчастный помощник, который хватаёт и наводит мишени
Миднолин действует как многофункциональный инструмент с тремя ключевыми модулями. Один конец, С-концевой α-спиральный сегмент, вставляется в участок связывания на компоненте протеасомы RPN1, фиксируя миднолин на утилизационной машине. Центральная «ловящая» область распознаёт и удерживает специфичную нитевидную особенность (дегрон) в целевых белках. На противоположном конце расположен домен, подобный убиквитину. Удивительно, но этот домен здесь не служит главным образом для связывания с протеасомой, как это делают подобные домены в других белках-переносчиках. Авторы показывают, что он располагается рядом с RPN11 — ферментом, который обычно срезает убиквитин с субстратов. В данном случае RPN11 скорее выполняет роль каркаса: обхватывая убиквитиноподобный сегмент миднолина, он помогает удерживать область Catch и её связанный груз прямо над узким входным отверстием в протеасому.
Направляя белок в измельчающее ядро
После того как миднолин закреплён, управление переходит к энергозависимому мотору протеасомы — кольцу AAA+ ATPаз. Это кольцо расположено непосредственно под входным отверстием и поэтапно втягивает развернутые полипептидные цепи в ядро. Снимки крио-ЭМ показывают серию позиций в виде «винтовой лестницы», принимаемых шестью субъединицами мотора по мере того как они хватают и передают субстрат через центральный канал. Авторы захватили четыре последовательных стадии этого цикла, все с материалом, связанным с миднолином и протянутым через отверстие, и даже увидели, как выход иона магния из одной субъединицы совпадает с опусканием всего кольца. Это указывает на то, что скоординированное расходование АТФ и высвобождение магния помогают «располагать» белок глубже в камере, где находятся каталитические участки.
Почему важны позиционирование и совместное экспрессирование
Группа проверила, как каждый модуль миднолина влияет на эффективность процесса. Анкерная спираль сама по себе может связываться с RPN1, но не повышает существенно активность протеасомы. Удаление области Catch оставляет многие протеасомы в холостом, не загруженном состоянии, даже если миднолин всё ещё прикреплён; замена Catch на постоянно связанный субстрат также не восстанавливает полную активность. Эти результаты указывают на то, что Catch делает больше, чем просто захват мишени — она должна точно ориентировать белок у входа в пору. Биохимические данные и анализ транскриптомов опухолей дополнительно показывают, что миднолин склонен синтезироваться совместно со своими субстратами. При совместной экспрессии миднолин лучше сворачивается и формирует стабильные комплексы, создавая готовый «пакет: уничтожь меня», который можно быстро доставить к протеасоме, когда клетке нужно перенастроить экспрессию генов.
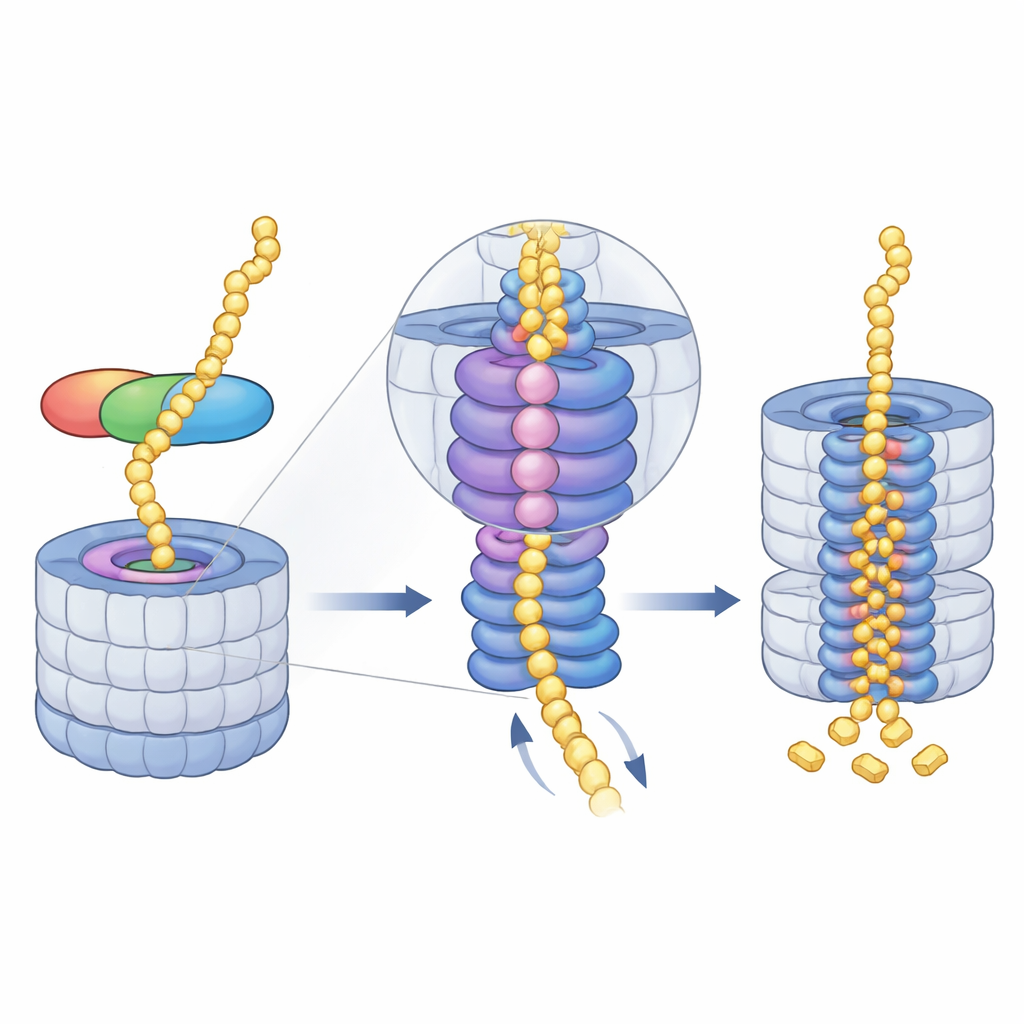
Самоочистка и возможные медицинские перспективы
После того как целевой белок втянут и измельчён, сам миднолин не остаётся в стороне. Его собственные неструктурированные участки могут быть протянуты через мотор и направлены в ту же камеру разрушения, что предотвращает чрезмерное накопление помощника. Осветив этот путь к протеасоме, не требующий убиквитина, исследование расширяет наше понимание того, как клетки управляют временем жизни белков в условиях жестких временных рамок. Оно также наводит на новые терапевтические идеи: путём конструирования молекул на основе миднолина, которые привязывают патогенные ядерные белки напрямую к протеасоме, учёные в будущем могут быстрее и избирательно устранять «неподдающиеся лечению» мишени, включая некоторые онкогены.
Цитирование: Zhu, C., Qin, L., Dai, Z. et al. Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover. Nat Commun 17, 2800 (2026). https://doi.org/10.1038/s41467-026-71002-0
Ключевые слова: протеасома, миднолин, разрушение белков, путь, не зависящий от убиквитина, гены мгновенного ответа