Clear Sky Science · ru
Пространственная гетерогенность МДСК, опосредованная сигналингом ANXA1–FPRs, обеспечивает иммунное подавление при прогрессировании РПСК
Почему защитные силы организма терпят неудачу против некоторых раков полости рта
Плоскоклеточный рак полости рта, распространённая форма рака рта, часто устойчив к самым перспективным ныне методам лечения — иммунотерапии, которая активирует собственные защитные механизмы организма. В этом исследовании ставится простой, но ключевой вопрос: почему мощные иммунные клетки, которые должны распознавать и уничтожать опухоль, так часто оказываются бессильными? Сопоставляя, где располагаются разные клетки в опухоли и как они между собой взаимодействуют, исследователи раскрывают меняющуюся «кошки‑мышки» динамику между раковыми клетками, иммунными супрессорами и киллерами T‑клетками, что помогает объяснить неэффективность лечения — и указывает на способ исправить это. 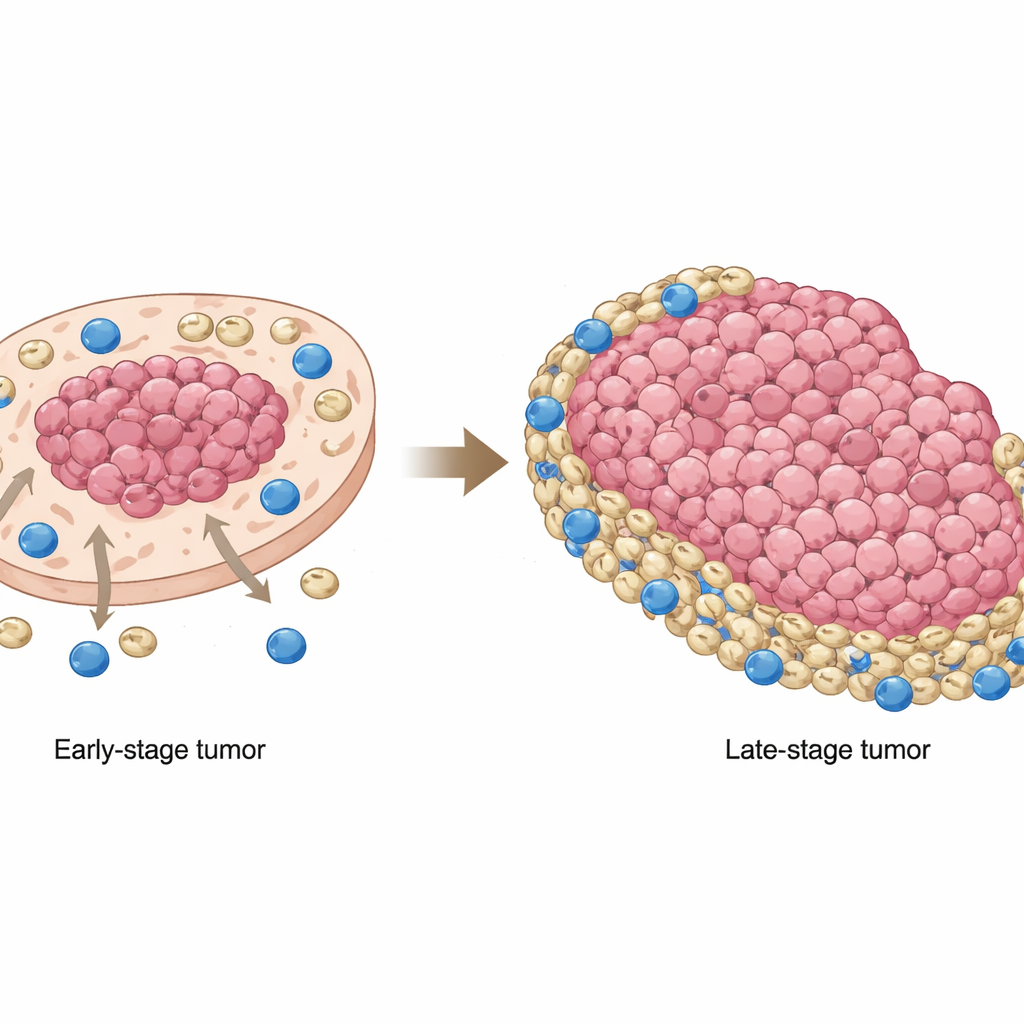
Скрытый ландшафт внутри опухоли
Авторы объединили два передовых подхода: одно‑клеточный РНК‑сиквенсинг, который считывает активность отдельных клеток, и пространственную транскриптомику, показывающую, где эти клетки расположены в тканевых срезах опухоли. Анализируя опухоли пациентов на ранних и поздних стадиях рака полости рта, они выделили ключевых участников: злокачественные эпителиальные клетки, CD8 «киллерные» T‑клетки, другие T‑ и B‑клетки, фибробласты, формирующие структурную поддержку, и специализированные иммунные клетки — миелоидные супрессорные клетки (МДСК). В ранних опухолях было больше активных CD8 T‑клеток, тогда как в поздних стадиях наблюдалось ослабление T‑клеточной сигнализации и усиление иммуносупрессивных сигналов со стороны миелоидных клеток, что указывает на постепенное формирование более враждебной среды для антиопухолевого иммунитета.
Супрессорные клетки в движении
Одно из наиболее заметных наблюдений касалось смещения позиций МДСК по мере прогрессирования опухоли. В ранних стадиях эти супрессорные клетки, как правило, сгущались в областях, богатых опухолевыми клетками, близко к ядру опухоли. На поздних стадиях они смещались наружу, накапливаясь в бедных опухолью зонах и на её краях, где чаще встречались CD8‑клетки. Это означало, что в продвинутых опухолях киллерные T‑клетки в основном оказывались вытесненными на периферию и сталкивались с «поясом» МДСК, который подавлял их способность атаковать раковые клетки. Образцы пациентов и модели на мышах подтвердили, что эта перестройка была не просто любопытным фактом: когда перекрытие МДСК с опухолевыми клетками уменьшалось, а они оседали в не‑опухолевых зонах, у пациентов наблюдалась худшая общая выживаемость. 
Переключение сигналинга между раковыми и супрессорными клетками
Исследование подробно рассмотрело молекулярный «диалог» между раковыми клетками и МДСК, в котором участвует белок аннексин A1 (ANXA1) на опухолевых клетках и семейство рецепторов FPR на миелоидных клетках. На ранних стадиях ANXA1 на раковых клетках активно взаимодействовал с FPR1 и FPR3, особенно на МДСК и опухоле‑ассоциированных макрофагах, способствуя привлечению и удержанию этих супрессорных клеток в ядре опухоли. По мере прогрессирования рака уровень ANXA1 в опухолевых клетках падал, ослабляя эти исходные связи. Одновременно всё больше МДСК начинали экспрессировать другой рецептор, FPR2, и сигналинг ANXA1–FPR2 возник как компенсаторный путь для поддержания МДСК вовлечённости. Определённый подтип опухолевых клеток с высоким уровнем ANXA1, также проявлявший стволоподобные признаки, по‑видимому, выступал в роли «приманки», привлекая МДСК на ранних этапах; когда ANXA1 снижался, МДСК теряли якорение в ядре и смещались в области, богатые CD8 T‑клетками.
Отключение «щита», чтобы иммунотерапия подействовала
Чтобы проверить, может ли разрыв этого диалога улучшить лечение, исследователи использовали модель рака полости рта на мышах и блокировали FPR2 маломолекулярным ингибитором WRW4. Сам по себе ингибитор FPR2 уменьшал присутствие МДСК и увеличивал количество CD8 T‑клеток в опухолевом микроокружении, но этого было недостаточно, чтобы значительно замедлить рост опухоли. Аналогично, лечение антителом против PD‑1 приносило лишь скромную пользу, поскольку МДСК всё ещё формировали супрессивный барьер. Однако при комбинированном применении обоих препаратов рост опухоли был значительно сдержан, а животные жили дольше. В этих животных инфильтрация МДСК резко снизилась, тогда как CD8‑клетки проникали глубже в области, богатые опухолевыми клетками, что говорит о том, что блокада FPR2 устраняет ключевой «щит», который обычно защищает раковые клетки от иммунной атаки.
Что это значит для будущего лечения рака
Вместе взятое, исследование показывает, что важны не только типы клеток, но и их пространственное расположение и сигнальные партнёрства для успеха иммунотерапии при раке полости рта. По мере прогрессирования опухоли МДСК мигрируют из центра к краям, где они перехватывают киллерные T‑клетки, а сигналинг ANXA1–FPR2 помогает поддерживать эту супрессивную конфигурацию. Нарушая этот путь — особенно в сочетании с существующими препаратами блокировки контрольных точек — врачи могут реконфигурировать опухолевое микроокружение так, чтобы собственные иммунные клетки организма снова могли распознавать и уничтожать рак. Это предлагает конкретную стратегию: комбинация блокаторов FPR2 с иммунотерапией может улучшить результаты у пациентов, у которых рак полости рта в настоящее время устойчив к лучшим доступным лечениям.
Цитирование: Li, F., Han, Y., Ou, F. et al. Spatial heterogeneity of MDSCs mediated by ANXA1-FPRs signaling drives immune suppression in OSCC progression. Nat Commun 17, 2535 (2026). https://doi.org/10.1038/s41467-026-70861-x
Ключевые слова: плоскоклеточный рак полости рта, опухолевый микроокружение, миелоидные супрессорные клетки, пространственная транскриптомика, раковая иммунотерапия