Clear Sky Science · ru
Сигнализация FGFR создает пространственные градиенты идентичностей секреторных клеток вдоль проксимо-дистальной оси дыхательных путей
Как наши дыхательные пути тихо сортируют и защищают воздух, которым мы дышим
Каждый вдох обрушивает поток воздуха на миллионы клеток, выстилающих трахею и легкие. Эти клетки выполняют не только роль пассивной поверхности: они детоксицируют загрязняющие вещества, борются с микробами и помогают не дать крошечным альвеолам спадаться. В этом исследовании показано, что секреторные клетки в дыхательных путях мыши далеко не однородны. Они выстроены в плавные градиенты от области, ближе к гортани (проксимальной), к глубоким отделам легкого (дистальным), и ключевой сигнальный путь, называемый FGFR2b, помогает установить и поддерживать эти постепенные изменения в идентичности и функции клеток. Понимание этого скрытого порядка дает представление о том, как легкие сохраняют здоровье и что может пойти не так при хронических заболеваниях легких.
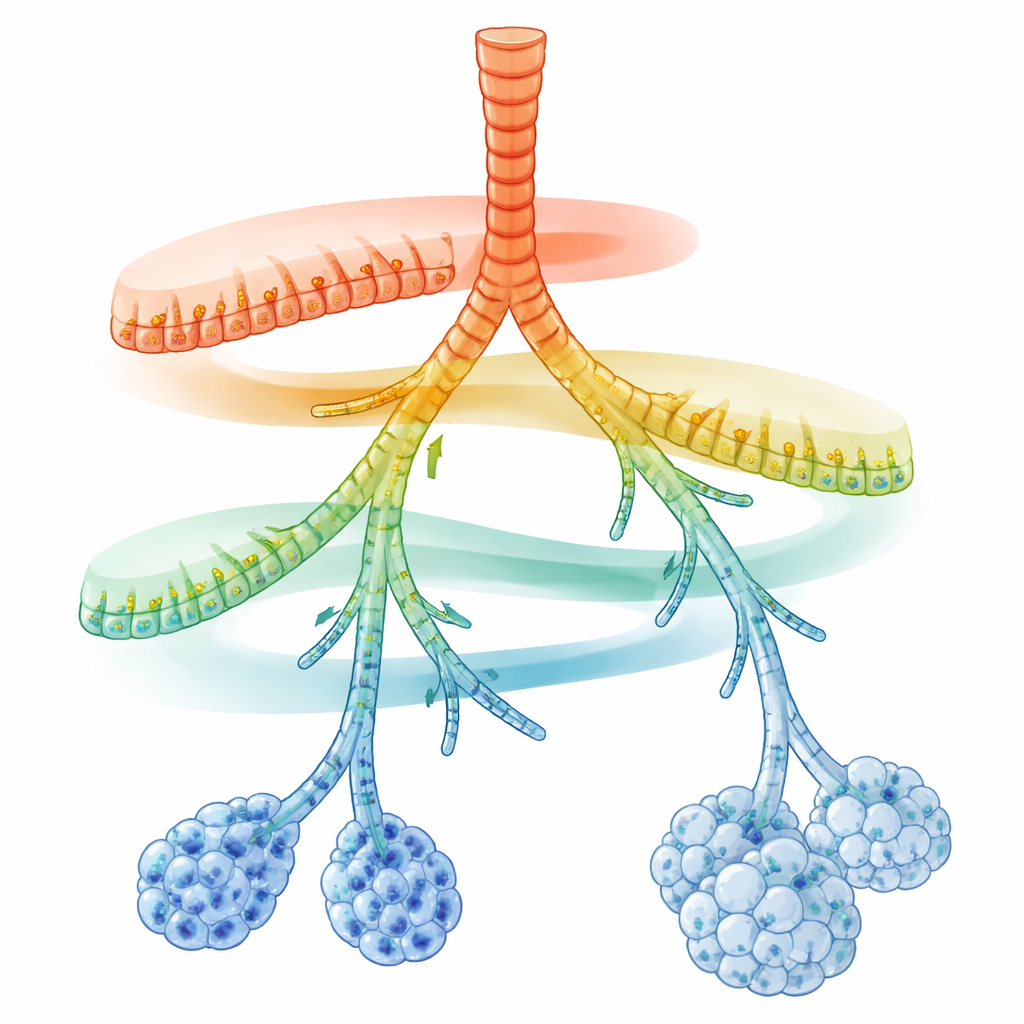
Скрытая карта вдоль дыхательных трубок
Исследователи сосредоточились на секреторных клетках, которые выстилают дыхательные трубки и выделяют слизь, антимикробные пептиды и сурфактант. С помощью одноклеточного РНК-секвенирования они прочитали активные гены в тысячах отдельных клеток из легких взрослых мышей. При проецировании этих клеток на карту молекулярного сходства секреторные клетки не распределялись по нескольким жестким типам. Вместо этого они образовывали непрерывную цепочку состояний, соединяющую крупные дыхательные пути с крошечными альвеолами. Наряду с общим базовым программным набором для детоксикации вдыхаемых химикатов возникли два противоположных градиента активности генов: вблизи больших дыхательных путей были наивысшие уровни генов, связанных с быстрой врожденной иммунной защитой; в направлении самых отдаленных ветвей и альвеол доминировали гены, отвечающие за обращение с липидами, синтез сурфактанта и представление антигенов.
От одной отправной точки — к множеству специализированных клеточных состояний
Чтобы понять, как возникает этот рисунок, команда мечтировала (labeled) секреторные прекурсоры в поздний плодовый период и отслеживала их потомков в ранней жизни с помощью трассировки линий и одноклеточного анализа. Эти меченые клетки первоначально формировали незрелый пул с сильной белоксинтетической машинерией и генами, связанными с построением ткани. После рождения, когда началось дыхание и влияние внешней среды, эти клетки постепенно диверсифицировались в несколько зрелых групп: проксимальные секреторные клетки, богатые генами врожденной защиты; более центральные клетки с развивающими и регуляторными сигнатурами; двухпозитивные клетки, соединяющие признаки дыхательных путей и альвеол; и альвеолярные клетки типа 2, специализированные на сурфактанте. Программа детоксикации включалась рано и широко, тогда как программы врожденного иммунитета и представления антигенов активировались позже и в отдельных областях, что указывает на то, что признаки секреторных клеток приобретаются в определенной последовательности во времени.
Как сигналы роста формируют дистальную идентичность дыхательных путей
Важная подсказка к тому, что управляет этими градиентами, пришла от рецептора FGFR2b — части сигнального пути факторов роста, уже известного как необходимого для альвеолярных клеток типа 2. FGFR2b и его целевые гены были более активны в дистальных клетках дыхательных путей и альвеолярных клетках, чем в проксимальных. Когда исследователи выключили FGFR2b специально в секреторных клетках сразу после рождения, нормальная дистальная программа дала сбой. Снизилась экспрессия генов, необходимых для синтеза сурфактанта и транспортировки везикул, тогда как возросла активность генов, типичных для плоских альвеолярных клеток типа 1, митохондриальных компонентов, ионных каналов и факторов выживания при стрессе. Некоторые промежуточные клетки теперь коэкспрессировали умеренные уровни проксимальных маркеров врожденной защиты и дистальных маркеров, фактически размывая нормальную пространственную схему. В органоидных культурах, выращенных из клеток дыхательных путей, добавление лигандов FGFR подавляло проксимальные маркеры врожденной защиты и усиливало гены, связанные с сурфактантом, в соответствии с результатами in vivo, подтверждая, что активация FGFR2b достаточна, чтобы сместить клетки в сторону дистальной секреторной идентичности.
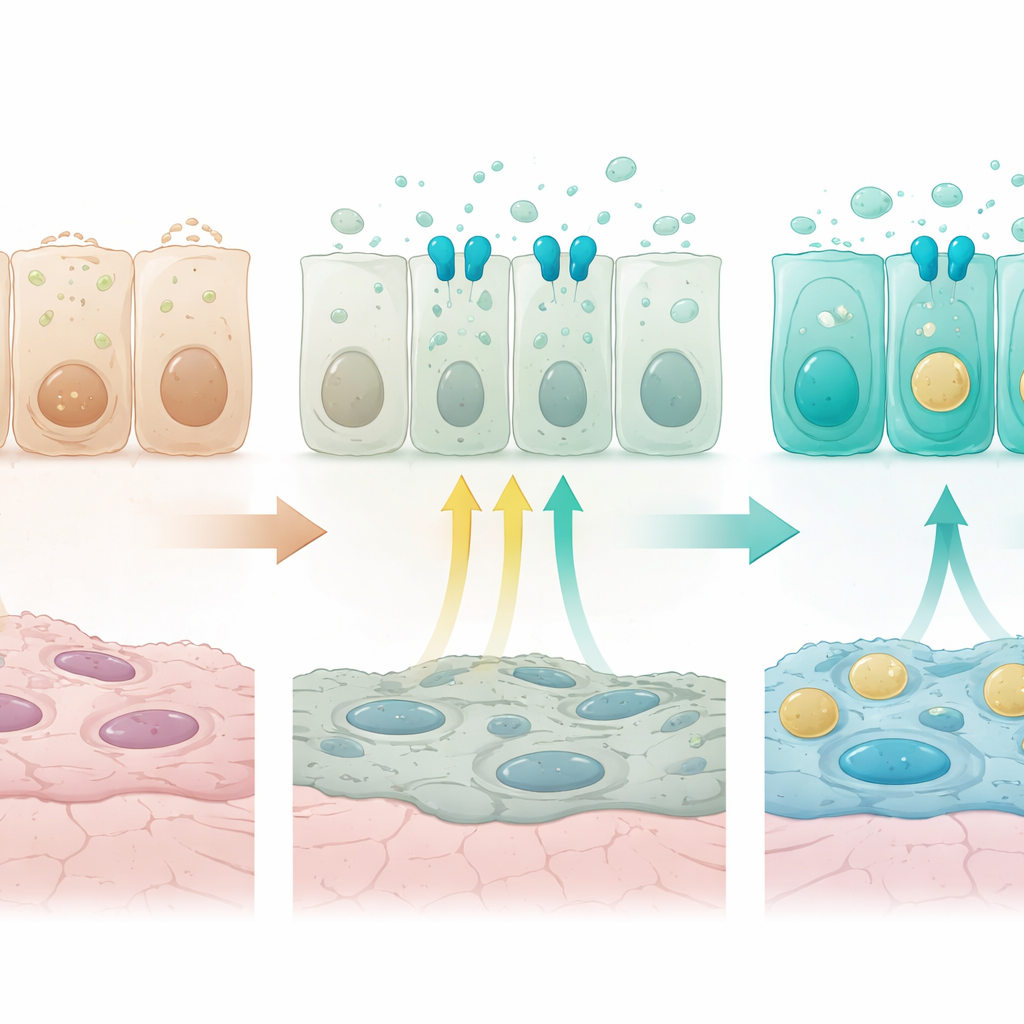
Тонкая настройка через взаимодействие с другими сигналами
Команда также изучила, как сигнализация FGFR2b взаимодействует с другим путем, опосредованным VEGFA, наиболее известным формированием кровеносных сосудов. В органоидах VEGFA самостоятельно могла ослаблять некоторые гены врожденной защиты, а блокирование ее рецептора изменяло определенные дистальные маркеры, но не могло полностью заменить FGFR2b. Фактически, потеря FGFR2b in vivo уменьшила экспрессию Vegfa, а совместная стимуляция обоих путей давала обратную связь, понижающую уровни FGFR2b, что указывает на сложный кросс-ток между этими системами сигналов. У взрослых мышей выключение FGFR2b уже не так драматично перестраивало градиенты врожденного иммунитета, но оставалось необходимым для поддержания экспрессии ключевых дистальных маркеров, таких как ген сурфактанта Sftpb и классический маркер секреторных клеток дыхательных путей Scgb1a1, а также для сохранения гибридных клеток «дыхательные пути–альвеолы».
Почему эти градиенты важны для здоровья легких
Возникающая картина представляет выстилку дыхательных путей как тонко градуированный ландшафт, а не как мозайку из изолированных зон. Проксимальные области настроены на быструю защиту на основе слизи, тогда как дистальные объединяют синтез сурфактанта с более специализированной иммунной коммуникацией. Сигнализация FGFR2b помогает установить и поддерживать эту организацию, особенно в дистальных отделах, стимулируя липидные и везикулярные программы и сдерживая неподходящие проксимальные черты. Нарушение этих градиентов, будь то по генетическим причинам, под влиянием окружающей среды или при болезни, может сместить баланс между защитой, детоксикацией и поддержкой газообмена, способствуя состояниям, когда дистальные дыхательные пути приобретают более проксимальные свойства. Эта концепция предлагает новый способ осмысления заболеваний легких, сопровождающихся «перепаттернированием» ветвления дыхательных путей, и может направить будущие стратегии по восстановлению правильной клеточной организации.
Цитирование: Sountoulidis, A., Theelke, J., Liontos, A. et al. FGFR signaling establishes spatial gradients of secretory cell identities along the airway proximal-distal axis. Nat Commun 17, 2651 (2026). https://doi.org/10.1038/s41467-026-70842-0
Ключевые слова: эпителий дыхательных путей, секреторные клетки, сигнализация FGFR2b, развитие легких, пространственные градиенты