Clear Sky Science · ru
Синтетические аптамерные механорецепторы обеспечивают селективное измерение силы клеток и временной контроль с помощью ДНК-схем
Прислушиваясь к клеткам через нежные рывки
Наши тела наполнены клетками, которые постоянно тянут и тискают окружение, применяя крошечные силы, чтобы решить, когда расти, двигаться или трансформироваться. В этом исследовании описан новый способ подслушивать такие силы с помощью устройств на основе ДНК, которые можно настраивать под конкретные типы клеток и включать или выключать во времени. Такая технология однажды может помочь инженерам управлять ростом тканей, лучше понять поведение опухолей или создать «умные» материалы, реагирующие на живые клетки в реальном времени.
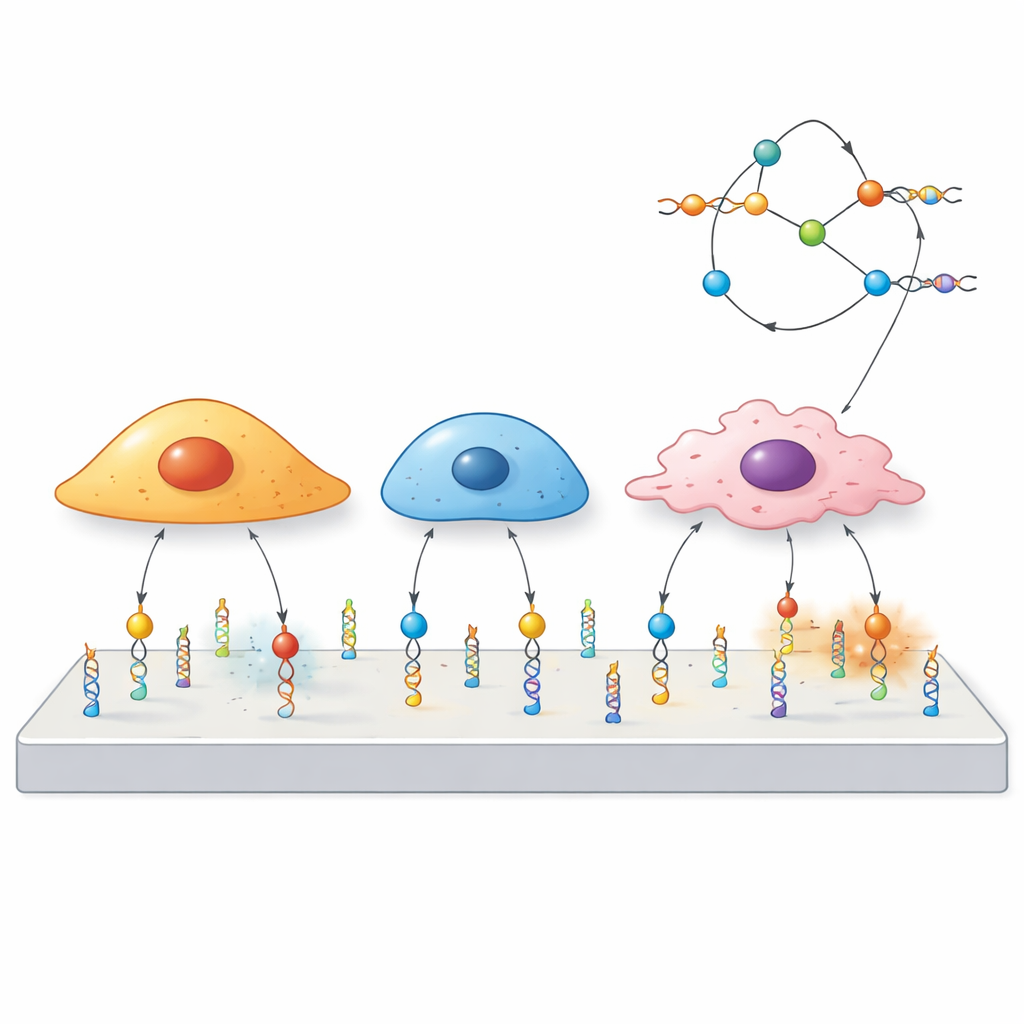
Использование ДНК как крошечного механического переключателя
Исследователи сконструировали «механозонды» из ДНК, той же молекулы, что несет генетическую информацию. Каждый зонд состоит из трёх частей: короткой последовательности ДНК — аптамера, который связывается с выбранным белком на поверхности клетки; парного сегмента ДНК, действующего как пружина, настроенная разрываться при определённой силе; и флюоресцентного красителя, который загорается, когда эта пружина «щелкает». Когда клетка тянет за рецептор, к которому прикреплён аптамер, с достаточной силой, дуплекс ДНК раскрывается и сигнал включается. Поскольку разные аптамеры захватывают разные рецепторы, команда может заранее выбрать, какие клетки или белки смогут активировать зонд.
Обнаружение скрытых путей передачи силы на поверхности клетки
Большинство существующих датчиков силы фокусируются на интегринах — известных белках, которые помогают клеткам удерживаться за окружающую среду, но распространены во многих типах клеток, что ограничивает селективность. В этой работе команда нацелилась на «неканонические» рецепторы, которые обычно не считаются механическими. Они показали, что аптамер AS1411, связывающий белок нуклеолин, характерный для раковых клеток, давал сигнал только при специфическом распознавании своей мишени. Проектируя зонды с требованием либо более слабой, либо более сильной силы для раскрытия, исследователи обнаружили, что нуклеолин передаёт умеренные силы по сравнению с интегринами и сам по себе не способствует распространению клетки по поверхности. Напротив, другой аптамер, Sgc8, распознающий рецептор PTK7, мог регистрировать силы даже при слабом прикреплении клеток, формируя кольцевые паттерны, что указывало на иной источник движения.
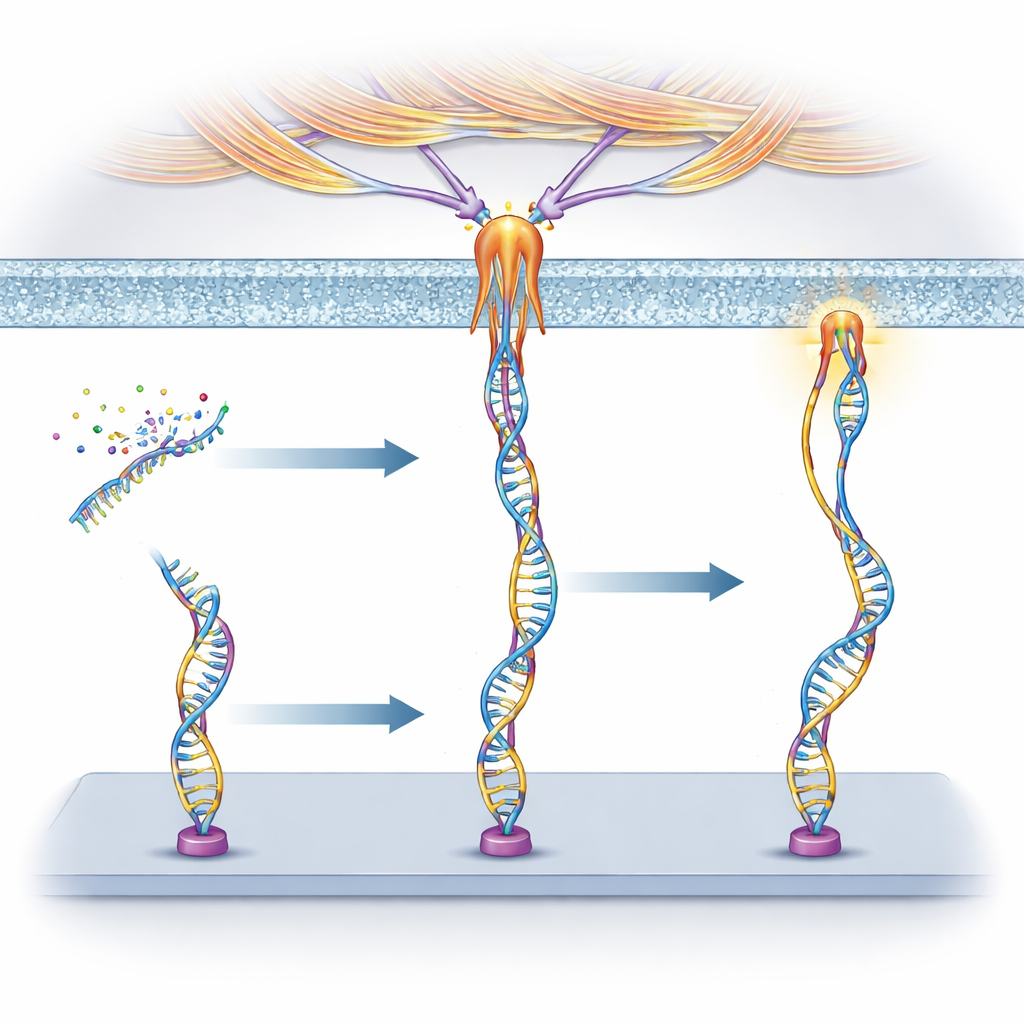
Прослеживание источников этих сил
Чтобы понять, что тянет за эти ДНК‑устройства, исследователи использовали препараты, избирательно блокирующие разные клеточные процессы. Для нуклеолина они обнаружили, что его силы сильно зависят от миозина — моторного белка, участвующего в сокращении мышц — и проявляются в местах формирования фокальных контактов, специальных точек соприкосновения, используемых для сцепления и восприятия жёсткости. Это указывает на то, что нуклеолин опосредованно связан с внутриклеточным актин‑миозиновым аппаратом и может разделять его сократительные усилия. Для PTK7 же блокирование макропиноцитоза — процесса, при котором клетка собирает мембранные складки и заглатывает жидкость — значительно уменьшало сигналы. Силы возникали главным образом из ранних этапов растрёпывания мембраны, управляемых ростом актина, а не из поздних шагов запечатывания везикулы, что выявляет отличную механическую траекторию.
Настройка селективности по клеткам с молекулярной точностью
Поскольку каждый аптамер распознаёт определённый поверхностный рецептор, ту же ДНК‑основу можно перепрограммировать простым обменом одного аптамера на другой. Команда продемонстрировала это с зондами для трёх различных мишеней — PTK7, mucin‑1 и EpCAM — на панели раковых клеточных линий с высоким или низким уровнем каждого белка. Клетки, богатые данным рецептором, давали сильные сигналы, тогда как клетки с малым количеством рецептора едва реагировали, даже при смешении в одной чашке. Поразительно, что клетки с одним и тем же рецептором всё равно могли демонстрировать разные пространственные паттерны силы, подчёркивая, что поток силы через рецептор зависит не только от его наличия, но и от внутриклеточной «проводки» каждого типа клетки.
Программирование времени, когда клетки могут тянуть
Воспользовавшись тем, что аптамеры состоят из ДНК, исследователи подключили свои зонды к ДНК‑реакционным сетям, контролирующим, может ли аптамер вообще связываться. Комплементарные «блокирующие» нитки могут временно скрыть аптамер, а «активирующие» нитки затем удаляют блоки через реакцию обмена нитями, восстанавливая чувствительность к силе. Они также разработали РНК‑блокер, который может быть разрезан ферментом RNase H, и дополнительно замедляли это расщепление с помощью молекул‑«приманок», конкурирующих за фермент. Таким образом они превратили механо‑сенсинг в тайм‑программу: клетки могли генерировать сигнал только после встроенной задержки или в выбранных временных окнах.
Почему это важно для будущих живых материалов
Проще говоря, эта работа превращает ДНК в умный механический замок, который открывается только для определённых клеток, только при определённых силах и только в заданное время. Показав, что малоочевидные рецепторы, такие как нуклеолин и PTK7, могут нести механическую информацию по очень разным внутриклеточным путям, исследование расширяет представление о том, как клетки «ощущают» своё окружение. Поскольку вся система собрана из нуклеиновых кислот, она может напрямую интегрироваться в быстрорастущий набор ДНК‑схем и наноустройств. Это создаёт основу для материалов и инженерных тканей, которые не только чувствуют, когда клетки толкают или тянут, но и отвечают тщательно синхронизированными биохимическими действиями, потенциально направляя заживление, рост или лечение рака в высокопрограммируемом формате.
Цитирование: Xu, T., Sethi, S., Drees, C. et al. Synthetic aptamer mechanoreceptors enable cell-specific force sensing and temporal control via DNA circuits. Nat Commun 17, 2492 (2026). https://doi.org/10.1038/s41467-026-70765-w
Ключевые слова: механотрансдукция, ДНК-аптамеры, механика клеток, синтетическая биология, ДНК-реакционные сети