Clear Sky Science · ru
Метрологическая основа для абсолютной транскриптомики с калибраторами, привязанными к Международной системе единиц
Почему важно превращать сигналы РНК в реальные числа
Современные тесты на гены могут читать, какие гены в клетках включены или выключены, но они сталкиваются с базовым вопросом: сколько молекул там на самом деле? Текущие технологии секвенирования РНК в основном сравнивают относительные изменения между образцами, а не дают жестких, надежных подсчетов. Это проблема, если нужно установить универсальные пороги для заболеваний, сопоставлять результаты между больницами или строить точные модели работы клеток. В этом исследовании предложен новый подход, который привязывает секвенирование РНК к тем же международным единицам, что используются в химии и физике, превращая нечеткие относительные сигналы в абсолютные, сопоставимые числа.
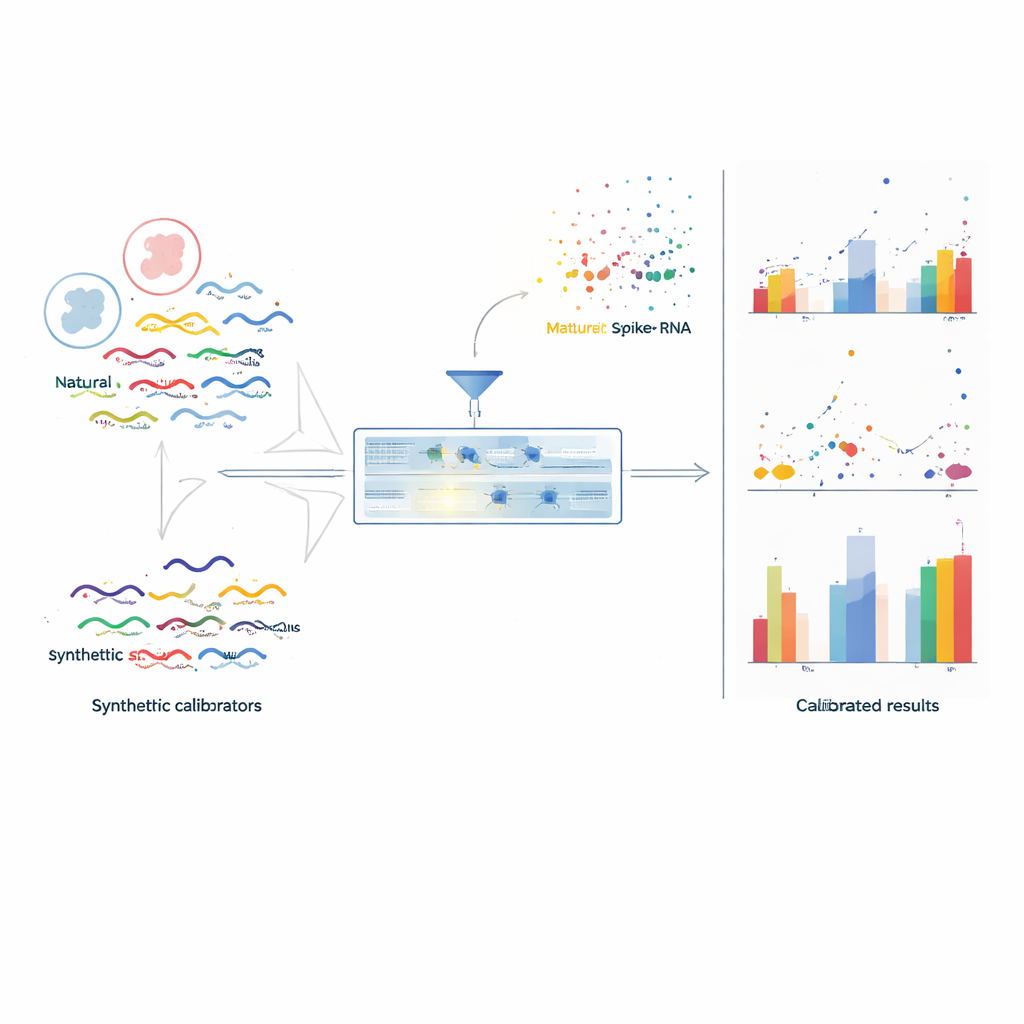
Проблема при сравнении активности генов
Секвенирование РНК работает путем дробления молекул РНК на фрагменты и подсчета, сколько раз представлен каждый ген. Но вмешиваются два типа искажений. Во-первых, системные различия между экспериментами — например, разные лаборатории, приборы или методы подготовки образцов — создают «эффекты партии», из‑за которых один и тот же образец при повторном анализе выглядит по‑разному. Во‑вторых, зависящие от последовательности эффекты — когда гены с определенной длиной или составом оснований захватываются с разной вероятностью — означают, что даже в одном образце некоторые гены постоянно переоцениваются, а другие — недооцениваются. В результате ученые вынуждены в основном говорить о множителях изменений между условиями, а не о реальных числах молекул, и сами эти множители могут вводить в заблуждение от партии к партии.
Новый набор эталонов для измерений РНК
Чтобы устранить это, авторы создали TranScale — панель из 100 синтетических молекул РНК, спроектированных так, чтобы вести себя как настоящие человеческие транскрипты, оставаясь при этом вычислительно различимыми. Эти стандарты охватывают широкий диапазон длин, особенностей последовательности и клинически значимых вариантов, таких как варианты сплайсинга и слияния генов, отражая разнообразие реальной клеточной РНК. Что важно, каждой молекуле TranScale присвоена точная концентрация с использованием первичного метода измерения — масс-спектрометрии с изотопным разведением, прослеживаемой до Международной системы единиц (SI). Вмешивая известное, очень малое количество TranScale в каждый РНК‑образец перед секвенированием, эксперимент получает внутреннюю «линейку», которая проходит те же лабораторные шаги и искажения, что и натуральные РНК.
Превращение шумных ридов в абсолютные количества
При наличии TranScale в каждой библиотеке команда может сопоставить число чтений секвенирования для каждой контрольной молекулы с ее аттестованной концентрацией. Для каждой партии они выбирают хорошо ведущие себя спай‑ины и подгоняют линейную калибровочную кривую, связывающую единицы, основанные на ридах, с истинным числом молекул. Эта простая модель одновременно учитывает и общепартийные, и связанные с последовательностью сдвиги. Та же кривая затем применяется ко всем генам в образце, преобразуя их относительные показания в абсолютные числа копий на единицу РНК. В крупном много‑лабораторном и мультиплатформенном исследовании, специально спроектированном для создания сильных эффектов партии, такая калибровка сократила медианное варьирование абсолютных измерений между центрами с более чем 85% до менее чем 15–25% и восстановила корректную кластеризацию биологических образцов, ранее скрытую техническим шумом.
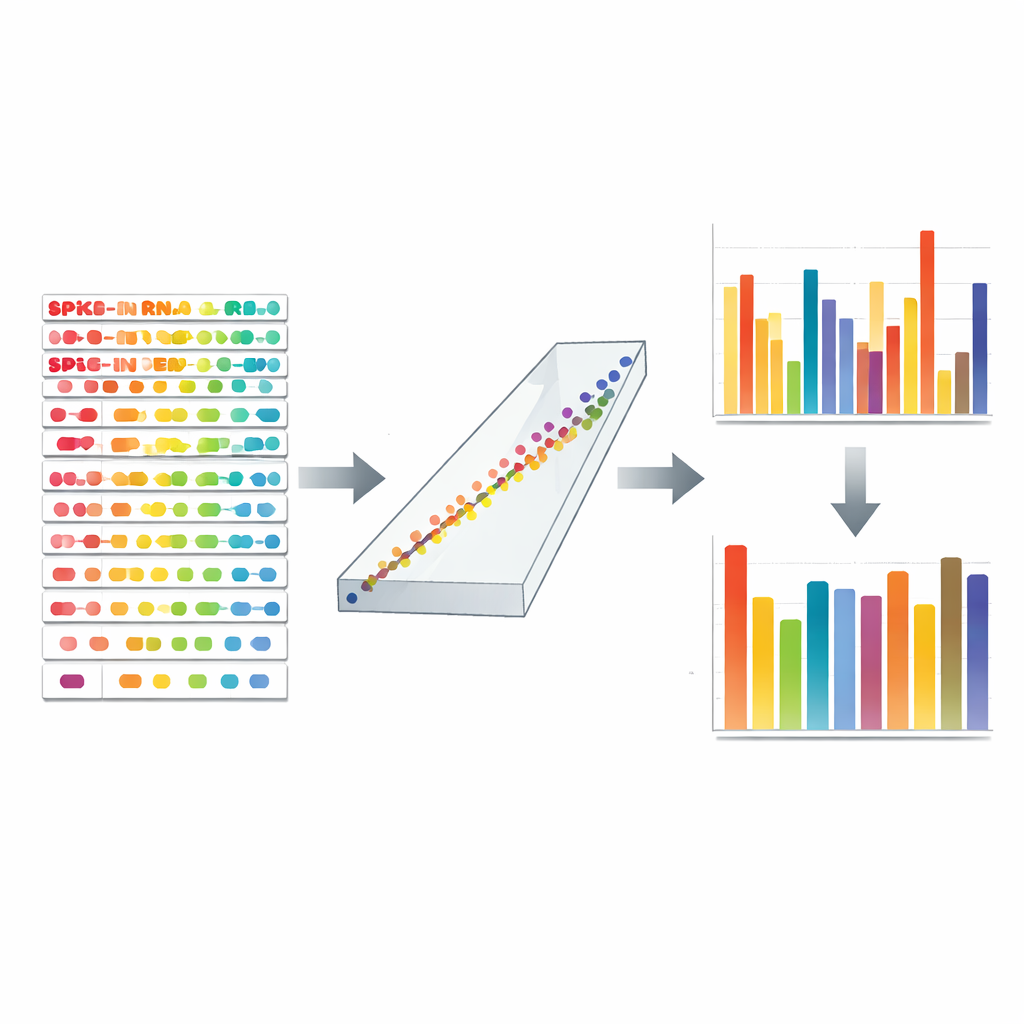
Выявление скрытых ошибок и их исправление
Стандарты TranScale также служат диагностическими зондами качества данных. Сравнивая измеренные значения с их аттестованными истинами, авторы разделили два типа ошибок: насколько неверно оценен абсолютный уровень каждого гена и насколько неверны отношения между условиями. Они обнаружили неожиданные примеры, когда относительные различия выглядели согласованными, но абсолютные числа были сильно искажены, и наоборот. Это означает, что традиционные проверки, ориентированные только на множители изменений, могут пропускать серьёзные проблемы. После калибровки и абсолютные уровни, и отношения для спай‑инов и тысяч реальных человеческих генов тесно совпадали с независимыми измерениями цифровой ПЦР и внешним эталонным набором данных. Исправленные данные открыли гораздо более ясный количественный пейзаж, сделав возможным сравнение генов‑«домработниц» и онкогенов на одной абсолютной шкале и прямую связь изменений в ДНК, например коамплифицированных онкогенов, с их РНК‑выходами.
От относительных трендов к клиническим порогам
В заключение исследователи показали, как абсолютное шкалирование может улучшить медицинские решения. На примере онкогена, часто измеряемого при раке молочной железы, они определили фиксированный порог на основе цифровой ПЦР и проверили, может ли секвенирование РНК надежно классифицировать образцы как нормальные или опухолевые в разных партиях. Некорректированные данные давали непоследовательные ответы из‑за эффектов партии. После калибровки TranScale каждая библиотека согласовывалась с истинной классификацией. Привязав секвенирование РНК к единицам SI через биомиметические стандарты, эта работа закладывает метрологическую основу для транскриптомики. Она открывает путь к универсальным диагностическим порогам, надежному обмену данными между центрами и более точным системным моделям экспрессии генов в норме и при заболевании.
Цитирование: Zhang, Y., Yang, B., Yu, Y. et al. A metrological foundation for absolute transcriptomics using International System of Units-anchored calibrators. Nat Commun 17, 2747 (2026). https://doi.org/10.1038/s41467-026-70582-1
Ключевые слова: секвенирование РНК, абсолютная количественная оценка, метрология, калибровка экспрессии генов, биомолекулярные стандарты