Clear Sky Science · ru
Структурные переходы при поэтапной сборке корпусов протеасом
Как клетки избавляются от молекулярного мусора
Внутри каждой нашей клетки отслужившие и повреждённые белки нужно разрушать, чтобы они не накапливались, как мусор. Огромный молекулярный аппарат, называемый протеасомой, выполняет большую часть этой «уборки» и уже используется в качестве мишени для противораковых препаратов. В этом исследовании показано, как каталитическое ядро протеасомы поэтапно собирается в дрожжевых клетках: учёные заглянули за кулисы и обнаружили неожиданные кратчайшие пути и механизмы защиты, которые гарантируют, что готовая машина заработает точно и только тогда, когда будет готова.
Сборка бочкообразного «измельчителя» белков
Рабочая часть протеасомы — это бочкообразное ядро, состоящее из сложенных колец белковых субъединиц. Внутри этой бочки скрыты каталитические сайты, которые расщепляют другие белки на мелкие фрагменты. Поскольку преждевременное включение этих «лезвий» было бы опасным, клетки собирают бочку через серию частично готовых промежуточных форм. Авторы сосредоточились на ранних вариантах ядра, известных как прекурсорные комплексы, которые обычно редки и недолговечны. Замедлив один из последних шагов сборки, они смогли захватить и очистить эти ранние формы из дрожжей и визуализировать их с помощью высокоразрешающей крио‑электронной микроскопии, которая «замораживает» молекулы в действии и показывает их трёхмерные формы.
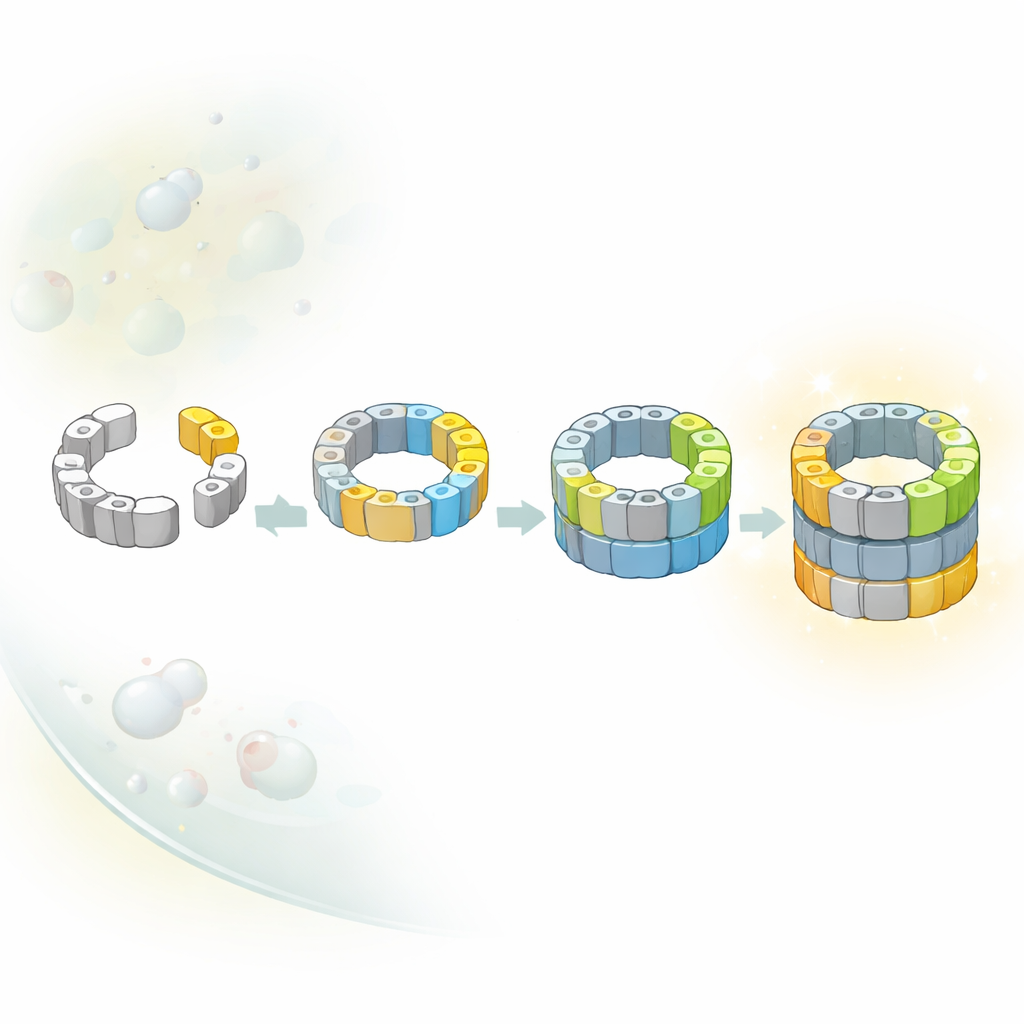
Несколько путей к одному и тому же ядру
Классические учебные схемы часто предполагают, что внутри клетки сложные машины собираются по единому, фиксированному маршруту. Здесь исследователи обнаружили, что для ядра протеасомы это не так. Они выделили несколько различных промежуточных форм, которые различаются тем, какие каталитические субъединицы уже присоединились к полуготовой бочке. Сочетая структурные «снимки» с генетическими приёмами, переключающими отдельные субъединицы, авторы показали, что по меньшей мере два альтернативных пути ведут от ранней полу‑бочки к почти завершённой. По одному пути первым приходит определённый субюнит β5; по другому — раньше может присоединиться другой субюнит, β1. Соотношение этих путей, вероятно, зависит от того, какие строительные блоки в данный момент наиболее доступны в густонаселённой среде клетки.
От свободных частей до запертой камеры резки
Структуры также показывают, как каталитические сайты протеасомы аккуратно подготавливаются по мере сборки. В ранних промежуточных формах ключевые петли вокруг скрытых каталитических остатков гибки и плохо упорядочены, а каталитические центры всё ещё блокируются короткими «пропептидными» сегментами. По мере того как дополнительные субъединицы встраиваются в кольцо, эти петли постепенно приобретают более определённую форму, выстраивая важные аминокислоты, необходимые для самопревращения в активную форму. Только когда две полу‑бочки наконец сходятся, завершая двойное кольцо, эти петли полностью фиксируются в активной конфигурации и инициируют удаление блокирующих сегментов. Эта связь геометрии и химии помогает гарантировать, что мощная резающая активность появляется только внутри запечатанной камеры, защищая остальную часть клетки.
Шапероны направляют, а затем отпускают
В процессе сборки специализированные вспомогательные белки — шапероны — руководят формирующейся бочкой и препятствуют неправильным сочетаниям. Один шаперон, Ump1, изначально почти неструктурирован, но постепенно сворачивается по мере того, как вокруг него окружают всё больше субъединиц; в конце он оказывается в центральной полости и затем разрушается, когда бочка становится активной. Другая пара шаперонов, Pba1–Pba2, захватывает поверхность внешнего кольца двояким хитрым способом. Гибкая петля Pba1 вклинивается между двумя субъединицами внешнего кольца как прокладка, слегка раздвигая их и препятствуя преждевременному закрытию. Одновременно хвостовая часть одной субъединицы внешнего кольца (α1) помогает правильно позиционировать соседние сегменты так, чтобы на заключительном этапе шапероны могли освободиться и кольцо сомкнуться. При удалении хвоста α1 бочка останавливается в поздней, почти завершённой стадии и упрямо сохраняет шапероны, что подтверждает: этот небольшой участок действует как часть механизма сброса.
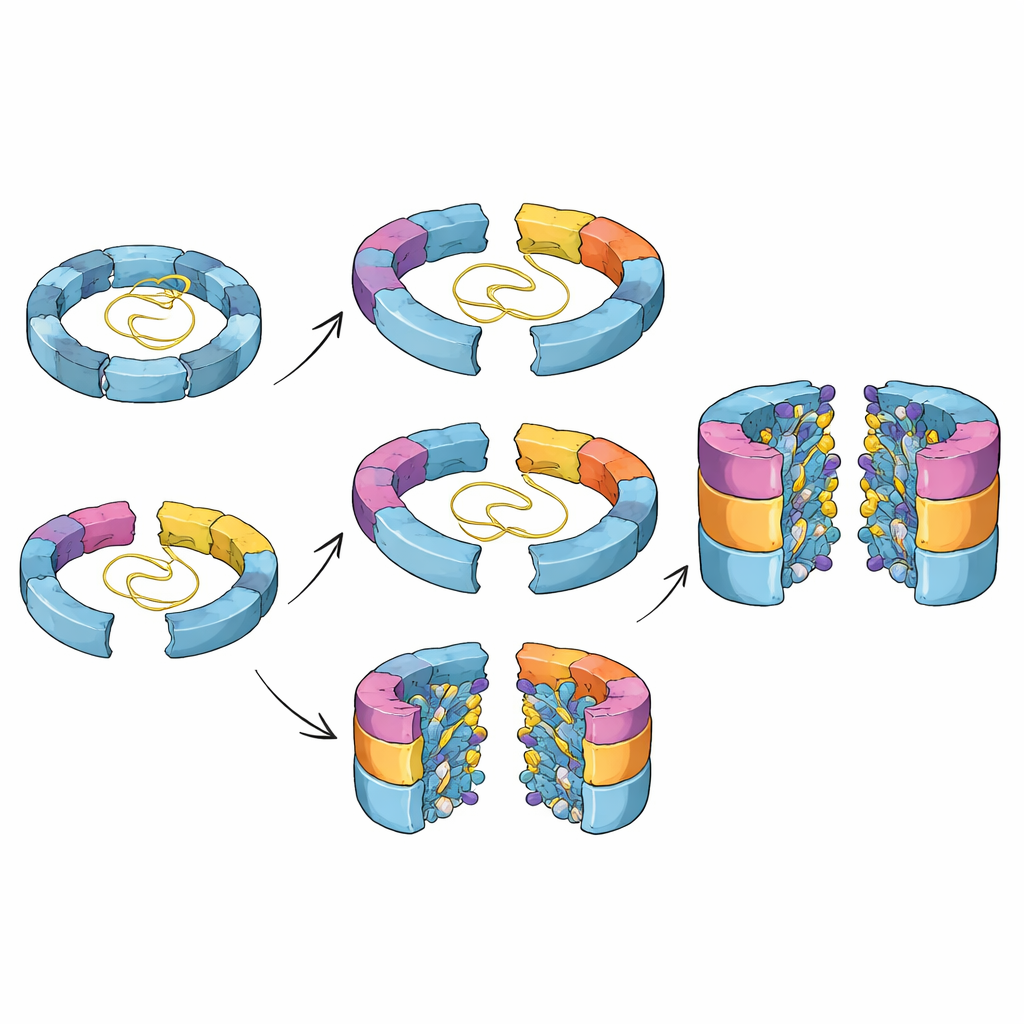
Почему эти скрытые шаги важны
В сумме эти результаты рисуют подробную картину того, как клетки координируют сборку опасного, но жизненно важного «измельчителя» белков. Работа показывает, что ядро протеасомы может собираться несколькими путями, что его активные сайты постепенно формируются, а вспомогательные белки не только стабилизируют ранние промежуточные формы, но и встроены в временную схему, обеспечивающую их уход в нужный момент. Понимание этих скрытых шагов помогает объяснить, как небольшие генетические изменения в факторах сборки могут способствовать заболеваниям, и может способствовать разработке лекарств, которые тонко регулируют активность протеасомы при раке, иммунных расстройствах или нейродегенеративных заболеваниях, воздействуя на её сборку, а не только на готовую форму.
Цитирование: Mark, E., Ramos, P.C., Nunes, M.M. et al. Structural transitions in the stepwise assembly of proteasome core particles. Nat Commun 17, 2582 (2026). https://doi.org/10.1038/s41467-026-70525-w
Ключевые слова: сборка протеасомы, деградация белков, молекулярные шапероны, криоэлектронная микроскопия, клеточный контроль качества