Clear Sky Science · ru
Гидрофобность поверхности и жесткость определяют белковую корону на перорально доставляемых наночастицах для лечения колита
Преобразование таблеток в более умные лекарства
Люди, страдающие воспалительными заболеваниями кишечника, такими как колит, часто принимают мощные противовоспалительные препараты, но значительная часть дозы теряется или вызывает побочные эффекты в других частях тела. В этом исследовании рассматривается новый способ заставить пероральные лекарства действовать как управляемые снаряды: проектирование крошечных несущих лекарство частиц, которые привлекают собственные кишечные белки пациента в качестве естественной системы наведения, помогая препаратам попадать в иммунные клетки, вызывающие воспаление в кишечнике.
Как кишечник «одевает» наночастицы
Когда любая наночастица попадает в организм, она быстро покрывается тонким слоем белков, образуя то, что ученые называют «белковой короной». В больном кишечнике эта корона сильно отличается от таковой в здоровой ткани, поскольку местный состав белков изменён. Авторы ранее обнаружили, что колит формирует особую кишечную корону, которая в некоторой степени направляет частицы к иммунным клеткам — макрофагам, которые и подпитывают, и ограничивают воспаление. В этой работе они намеренно формируют корону, меняя две базовые характеристики несущих лекарство частиц — их способность отталкивать воду (гидрофобность) и их жёсткость (ригидность) — чтобы превратить умеренный, индуцированный болезнью эффект в мощную стратегию таргетирования.
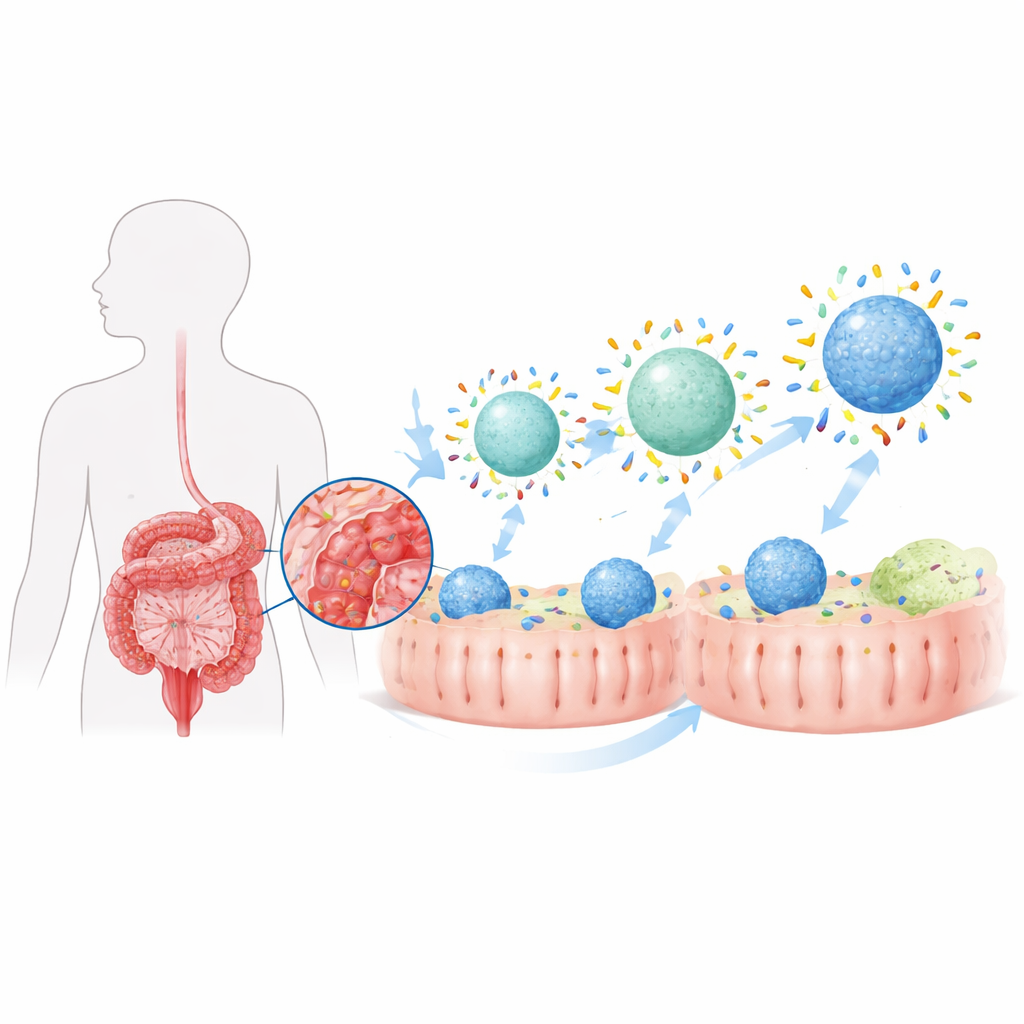
Делаем частицы привлекательнее для белков
Команда создала липидные наночастицы, похожие на крошечные жировые пузырьки, и настроила, насколько поверхностно они гидрофильны или гидрофобны, добавляя разное количество обычного полимерного покрытия. Частицы с более гидрофобной поверхностью связывали значительно больше кишечных белков при экспозиции в средах, моделирующих колит, как в животных моделях, так и в пробирках. Когда эти «фобные» частицы загрузили стероидом будесонидом и дали перорально крысам с колитом, они доставляли гораздо больше препарата в колонические макрофаги, чем более гидрофильные варианты. В результате лечёные животные быстрее восстанавливали массу тела, у них отмечалось меньше укорачивания и повреждения толстой кишки и снижались уровни воспалительных молекул в кишечнике. Однако, несмотря на улучшение воспаления, состояние не вернулось полностью к здоровому, что указывает на то, что простое увеличение общего количества белков короны было недостаточно.
Укрепление частиц для выбора лучших партнёров
Чтобы продвинуть концепцию дальше, исследователи сохранили гидрофобность поверхности, но изменили внутреннюю структуру, делая частицы мягкими, промежуточными или жёсткими, заполняя их ядра пластиковыми шариками разного размера. Все три варианта по-прежнему набирали схожее суммарное количество кишечных белков, но состав короны менялся. Самые жёсткие частицы формировали короны, особенно богатые белками, которые могут сцепляться с рецепторами на макрофагах или переносить небольшие нутриенты, которые эти клетки поглощают. Один из таких белков, S100A8, обилен в воспалённом кишечнике и может взаимодействовать со специфическими рецепторами макрофагов. Блокирование S100A8 на короне резко снизило поглощение жёстких частиц макрофагами, выявив его как ключевой компонент таргетирования, выбранный по критерию ригидности частицы.
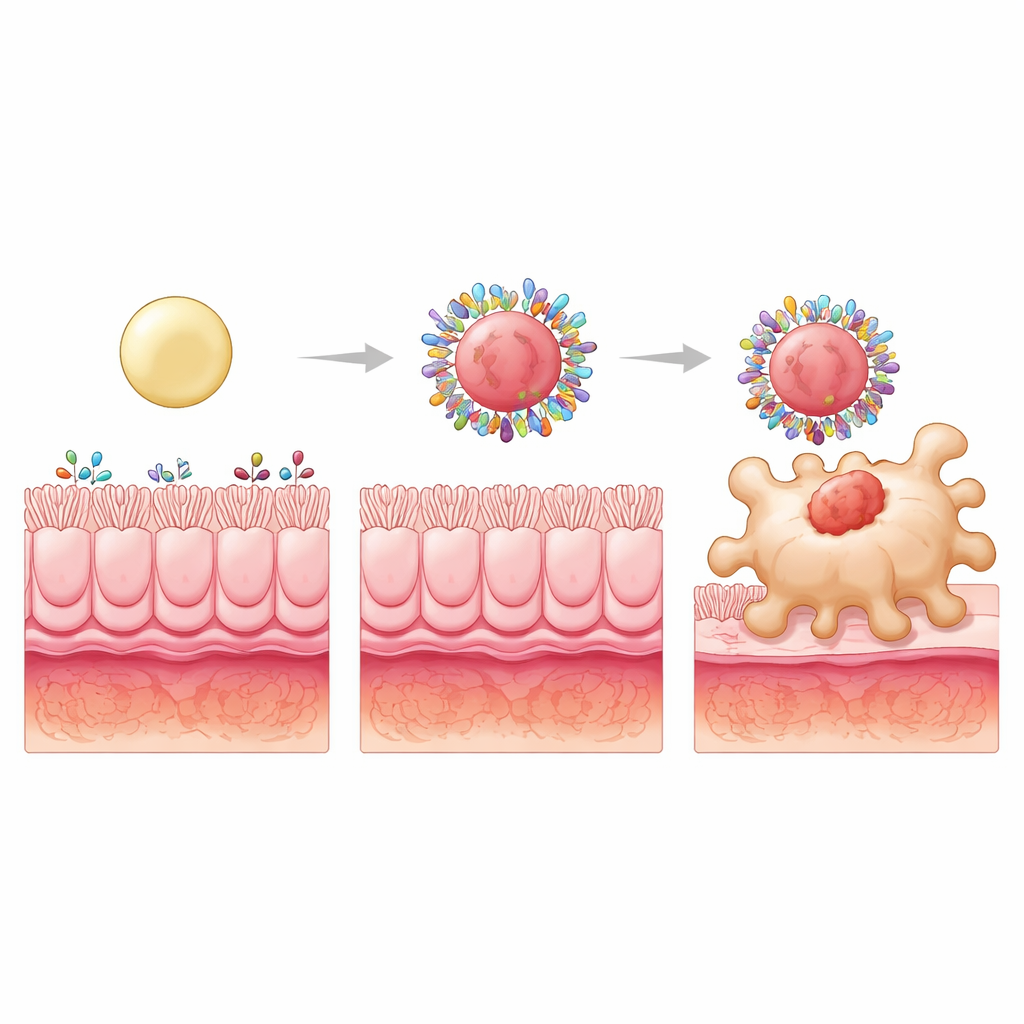
От лучшего таргетирования к лучшему заживлению
Когда будесонид помещали в эти частицы с высокой гидрофобностью и высокой жёсткостью и давали перорально крысам с колитом, эффект был впечатляющим. Жёсткая формула не только снижала повреждение кишечника и окислительный стресс, но и нормализовала множество воспалительных сигналов до уровней, наблюдаемых у здоровых животных. Она восстанавливала более здоровый баланс между «атакующими» и «спокойными» типами макрофагов и увеличивала число регуляторных Т-клеток, которые помогают сдерживать иммунные реакции. Важно, что эти улучшения зависели от изменённой при болезни белковой среды при колите; та же конструкция не показывала особого таргетирования у здоровых крыс, что подчёркивает, что корона — динамичный, специфичный для болезни партнёр.
Почему это важно для будущих лекарств
Эта работа демонстрирует, что мы можем направлять собственные белки организма действовать как умные, самовоспроизводящиеся «метки» на пероральных носителях лекарств просто путём настройки поверхностных и механических свойств носителей. Сначала увеличивая захват белков за счёт гидрофобных поверхностей, а затем используя жёсткость, чтобы отбирать белки, направляющие к макрофагам, такие как S100A8, исследователи создали наночастицы, которые естественным образом ищут иммунные клетки, приводящие к колиту, и доставляют терапию туда, где она наиболее необходима. Та же логика проектирования — управление тем, как частицы ощущаются и ведут себя на поверхности кишечника — может быть адаптирована для множества типов наномедицин и заболеваний, предлагая новый, более тонкий путь к целевой терапии без навешивания искусственных молекул-мишеней.
Цитирование: Wu, J., Ni, M., Xing, L. et al. Surface hydrophobicity and rigidity determines protein corona on orally delivered nanoparticles treating colitis. Nat Commun 17, 2497 (2026). https://doi.org/10.1038/s41467-026-70453-9
Ключевые слова: доставка лекарств с помощью наночастиц, воспалительные заболевания кишечника, белковая корона, пероральная наномедицина, таргетирование макрофагов