Clear Sky Science · ru
Модификации рибосом связаны с выбором мезенхимного пути судьбы в линии нейрального гребня
Как крохотные клеточные фабрики формируют лица и опухоли
Наши лица и части нервной системы формируются из странствующей популяции эмбриональных клеток, называемых нейральным гребнем. Эти клетки способны превращаться в кость, хрящ, нервы и другие ткани. В этом исследовании показано, что их выборы зависят не только от генов, но и от тонких химических правок в клеточных машинах по синтезу белка — рибосомах. Те же молекулярные особенности, которые помогают строить нормальное лицо, при неправильной регуляции могут отмечать более опасные формы детского рака.
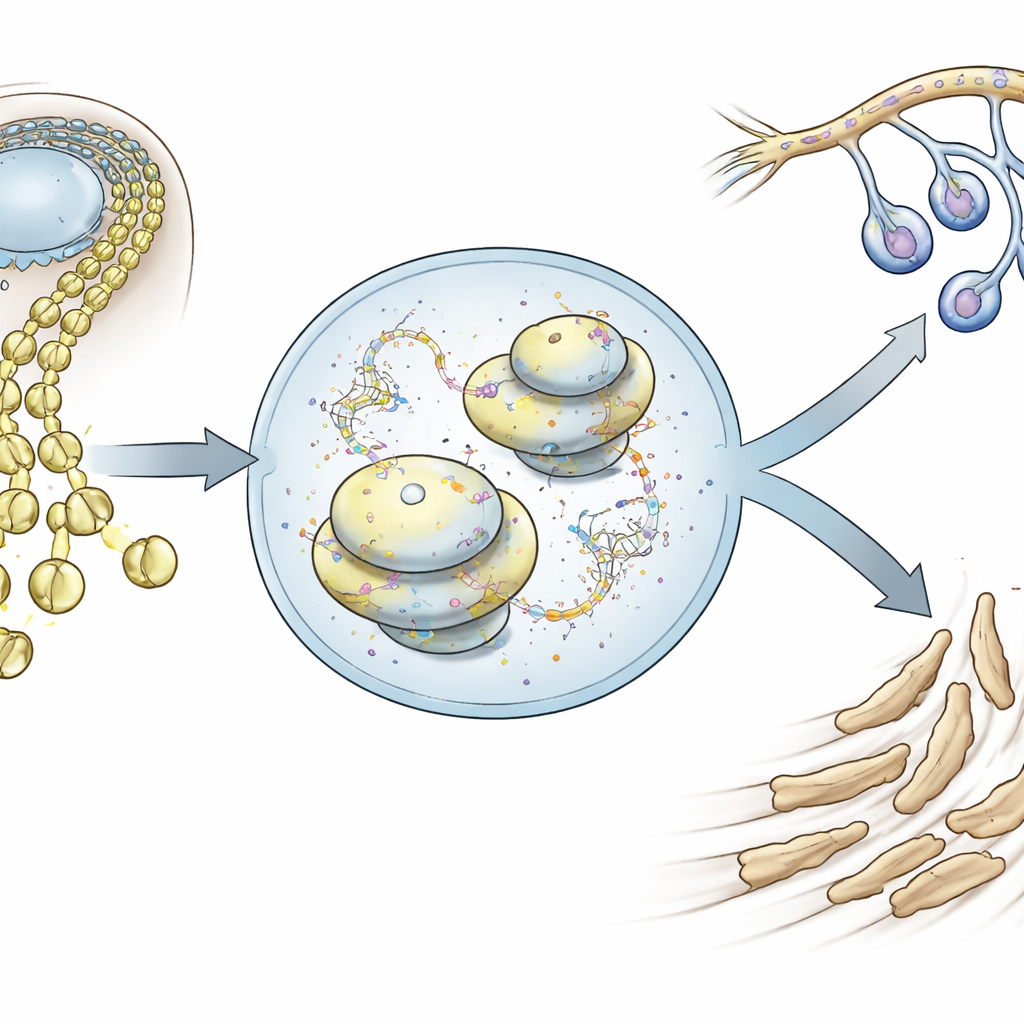
Клетки‑хамелеоны, которые строят лицо
Клетки нейрального гребня появляются вдоль раннего мозга и спинного мозга, затем мигрируют наружу, в конечном счёте формируя большую часть черепа, челюстей и периферических нервов. С помощью секвенирования РНК одной клетки в эмбрионах мыши авторы проследили за тысячами отдельных краниальных клеток нейрального гребня по мере их выхода из нервной трубки и перемещения в область лица. Они обнаружили, что очень рано эти клетки уже демонстрируют лёгкое смещение в сторону одного из двух основных путей: мезенхимального, который даст лицевые кости и хрящи, или нейроглиального, который сформирует нейроны и глиальные клетки. Эти две программы активности генов сначала сосуществуют в одних и тех же клетках, но по ходу развития становятся взаимоисключающими, вынуждая принять судьбоносное решение.
Фабрики белка как принимающие решение
Когда команда проанализировала, какие гены связаны с ранним уклоном в сторону лицевого мезенхима, они обнаружили две основные группы. Одна включала известные факторы, которые побуждают клетки ослаблять контакты, мигрировать и менять идентичность — процесс, известный как эпителиально‑мезенхимальный переход. Другая, более неожиданная группа, была сосредоточена на сборке рибосом и химической модификации рибосомной РНК, ядра машины синтеза белка. Вместо простого увеличения числа рибосом краниальные клетки нейрального гребня активировали факторы, которые тонко настраивают, как рибосомы собираются и химически маркируются. Нарушение производства рибосомной РНК в эмбрионах мыши в момент выбора судьбы в основном пощадило развивающиеся нервы, но серьёзно ограничило развитие лицевого скелета, показывая, что мезенхимный путь особенно зависим от этого рибосомного контроля.
Особая метка на рибосомной РНК
Углубляясь, исследователи сосредоточились на одной нуклеотидной позиции в 18S рибосомной РНК, расположении, важном для точного синтеза белка. У краниальных клеток нейрального гребня, склонных к мезенхимным судьбам, секвенирование неоднократно неправильно считывало эту позицию — признак интенсивной химической модификации, а не истинной мутации. Предыдущие работы показали, что трио ферментов вносит здесь сложную модификацию в несколько шагов. Объединив данные человеческой геномики и РНК с масс‑спектрометрическим анализом эмбриональных тканей мыши, исследование подтвердило, что этот сайт нормален в ДНК, но химически модифицирован в РНК в разной степени, и что доля модифицированной формы отличается между тканями мозга и лица. Переэкспрессия или выключение ферментов, создающих эту модификацию, в культурах клеток и в эмбрионах мыши нарушало развитие нейрального гребня и вызывало заметные краниофациальные дефекты, подчёркивая, что точные уровни этой метки РНК помогают направлять клетки в скелетогенетический путь.
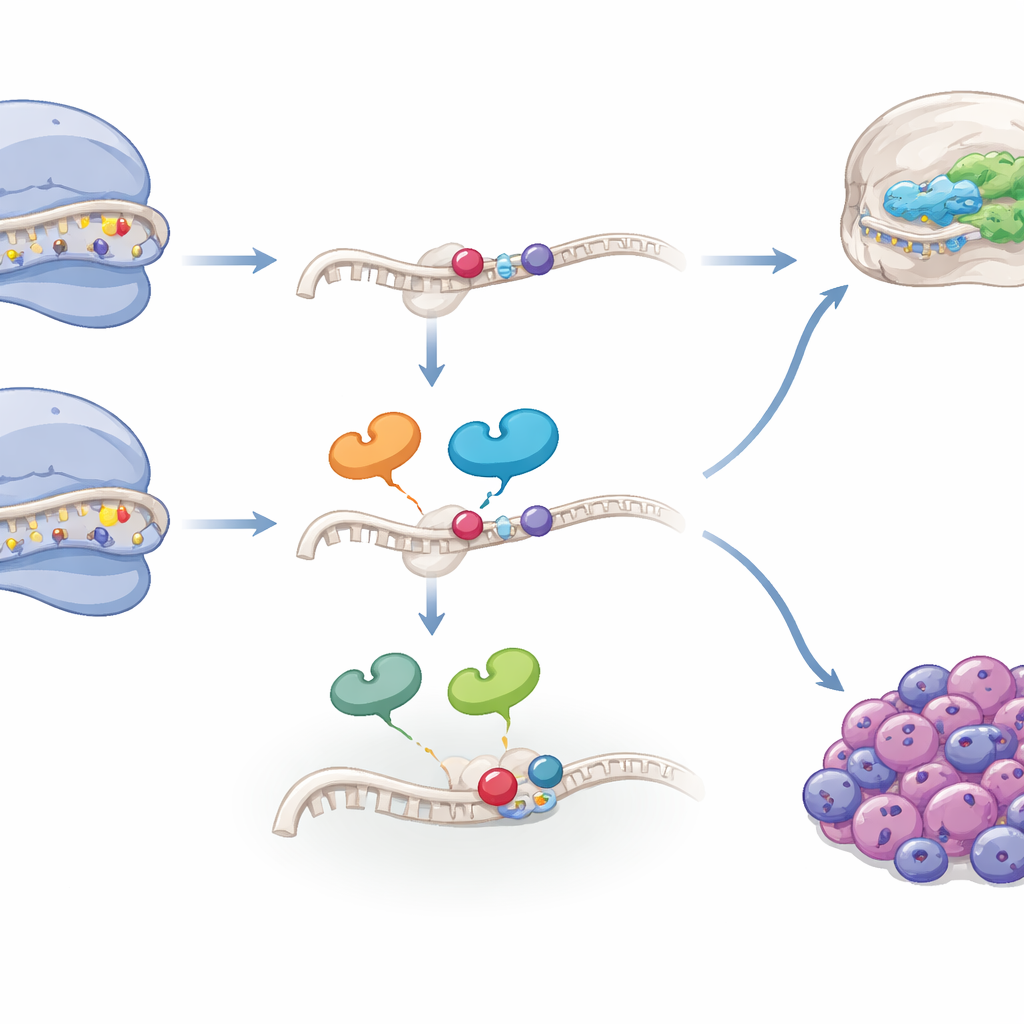
От развития к риску рака
Поскольку клетки нейрального гребня также могут давать начало опухолям, таким как нейробластома, авторы проверили, появляются ли те же рибосомные особенности в раке. Анализ одиночноклеточных и суммарных данных РНК из нескольких когорт нейробластомы и опухолей мозга показал, что сигнатура генов «контроля рибосом и модификации РНК» обогащена в субпопуляциях опухолевых клеток с более мезенхимоподобными чертами — состояниях, часто связанных с устойчивостью к терапии и плохим прогнозом. В нескольких когортах пациентов высокий уровень этой сигнатуры сильно предсказывал худшую выживаемость, особенно при нейробластомах без амплификации известного гена риска MYCN. Отдельные компоненты, такие как фактор сборки WDR74 и фермент модификации TSR3, были повышены в агрессивных клеточных линиях и делали эти клетки более уязвимыми к препаратам, создающим нагрузку на рибосому. Любопытно, что опухоли с очень низким или очень высоким уровнем ключевой РНК‑модификации в выделенной позиции имели худший исход, чем опухоли со средними уровнями, что предполагает, что и дефицит, и избыток этого специализированного пула рибосом могут быть вредны.
Что это значит для лиц и детских онкологических заболеваний
В совокупности эти результаты указывают на то, что рибосомы — не просто пассивные фабрики белка, а настроенные устройства, химический состав которых помогает решить, как эмбриональные клетки строят лицо и как ведут себя некоторые опухоли. В клетках нейрального гребня определённая химическая метка на рибосомной РНК, по‑видимому, способствует синтезу белков, необходимых для формирования лицевой кости и хряща, тогда как её нарушение при раке связано с более опасными, метаформирующимися опухолевыми клетками. Понимание и потенциальная мишень этой рибосомной «тонкой печати» могут открыть новые подходы к предотвращению краниофациальных пороков и к обнаружению или лечению высокорисковых нейробластом.
Цитирование: Poverennaya, I., Murtazina, A., Li, L. et al. Ribosomal modifications are associated with mesenchymal fate selection in the neural crest lineage. Nat Commun 17, 2326 (2026). https://doi.org/10.1038/s41467-026-70375-6
Ключевые слова: развитие нервного гребня, модификации рибосом, краниофациальное формирование, нейробластома, специализированные рибосомы