Clear Sky Science · ru
СнуРНК с завершением CPF‑CF перемещаются через цитоплазму посредством механизма надзора, опосредованного белком‑сторожем для мРНК
Как крошечные направляющие РНК делают неожиданный крюк
Внутри каждой клетки синтез белков зависит от точной молекулярной хореографии. Важную часть этого танца контролируют малые ядерные нуклеолярные РНК, или snoRNA, которые помогают формировать рибосомы — машины, собирающие белки. В этом исследовании показано, что некоторые из этих крошечных направляющих неожиданно покидают ядро, кратко посещают цитоплазму и затем возвращаются, и всё это — из‑за способа, которым прекращается их синтез. Понимание этого скрытого маршрута проливает свет на то, как клетки обеспечивают качество РНК и защищают генетическую информацию.
Взгляд поближе на помощников РНК в клетке
SnoRNA — короткие молекулы РНК, выступающие в роли направляющих, которые направляют химические модификации других РНК, особенно тех, что образуют рибосомы. В клетках дрожжей большинство snoRNA синтезируется в ядре и считалось, что они там и остаются, образуя стабильные комплексы с определёнными белками — snoRNP, рабочие комплексы, изменяющие рРНК. Тем не менее более ранние работы обнаруживали взаимодействие snoRNA с белками, обычно вовлечёнными в вывоз матричных РНК из ядра. Это ставило вопрос: путешествуют ли snoRNA иногда в цитоплазму и если да, то почему?
Обнаружение перемещающихся snoRNA
Повторно анализируя данные секвенирования РНК из тщательно разделённых ядерных и цитоплазматических фракций, авторы обнаружили, что многие snoRNA действительно присутствуют в цитоплазме нормальных дрожжевых клеток, на уровнях, сопоставимых с обычными матричными РНК. Когда они инактивировали ключевые факторы экспорта Mex67 и Xpo1, цитоплазматический пул snoRNA уменьшался, а в ядре накапливались незрелые предшественники snoRNA с удлинёнными 3′‑концами. Микроскопия с флуоресцентными зондами подтвердила эту смену: сигналы, которые обычно наблюдались и в нуклеолусе, и слабо в цитоплазме, становились сильно ядерными при блокировке экспорта. Эти наблюдения показывают, что часть snoRNA, часто всё ещё несущая дополнительные последовательности на концах, активно транспортируется из ядра и не является просто утечкой или загрязнением образцов.
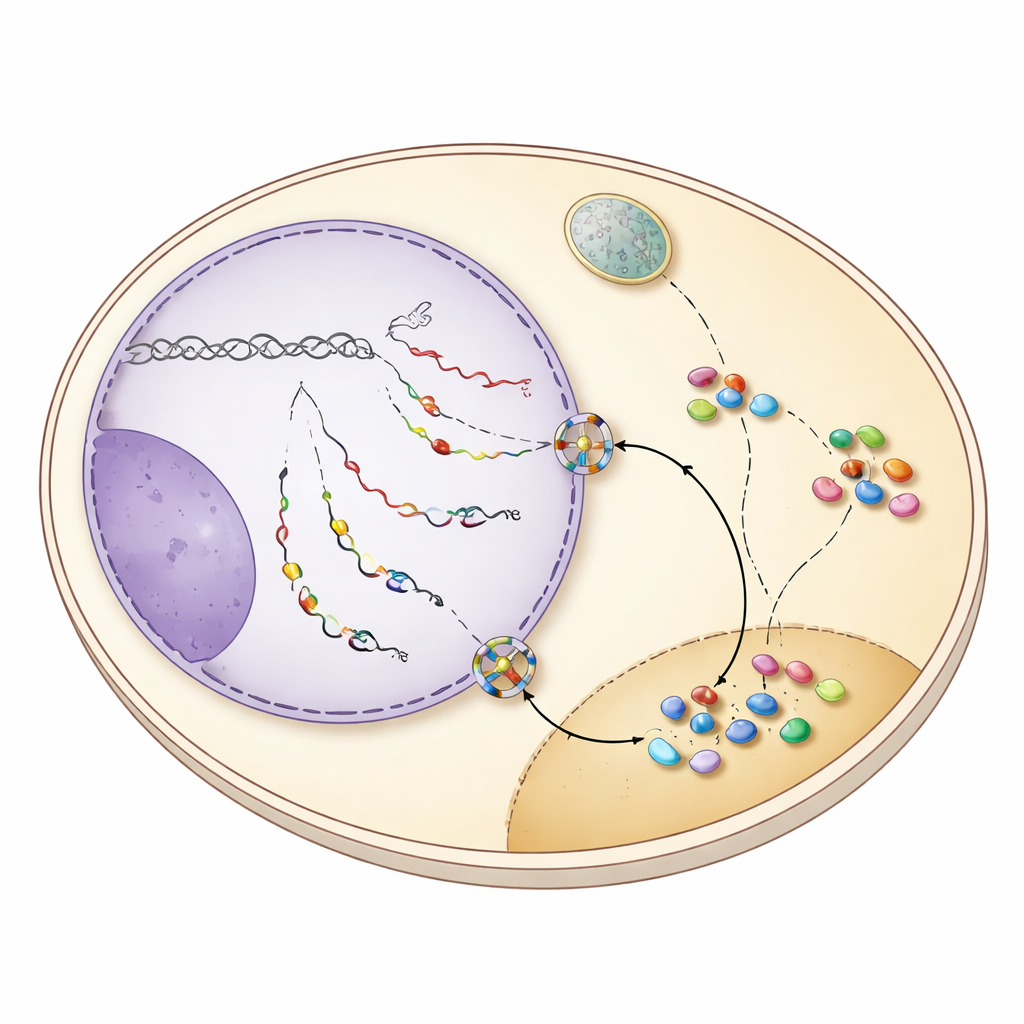
Переключатель белка‑сторожа, отправляющий snoRNA наружу
Ключ к такому шаттлингу кроется в том, как завершается транскрипция snoRNA. У дрожжей большинство snoRNA обычно отделяется от транскрипционного аппарата системой NNS, что оставляет короткий хвост, который быстро подрезается в ядре. Однако многие гены snoRNA также содержат запасные сигналы остановки, распознаваемые второй системой CPF‑CF, более известной по завершению мРНК и добавлению длинных поли(А)хвостов. Когда NNS‑завершение даёт сбой, транскрипты snoRNA продолжаются до этих расположенных ниже сайтов CPF‑CF и получают длинный хвост. Такое изменённое окончание рекрутирует набор «белков‑сторожей» — среди них Hrp1 и Nab2 — которые проверяют корректную обработку и одновременно привлекают фактор экспорта Mex67. Исследование показывает, что когда snoRNA завершаются системой CPF‑CF, белки‑сторожи и Mex67 совместно отправляют эти снабжённые хвостами snoRNA через ядерные поры в цитоплазму.
Билеты в обе стороны и контроль качества
Попав в цитоплазму, snoRNA не остаются без присмотра. Они остаются связаны защитным кольцом белков Lsm и фактором Lhp1, которые экранируют уязвимый конец РНК. Эти признаки позволяют двум рецепторам импорта, Cse1 и Mtr10, распознавать шаттлирующие snoRNA и возвращать их в ядро. Когда авторы инактивировали эти факторы импорта или кольцо Lsm, в цитоплазме накапливались незрелые snoRNA, что подтверждает, что этот механизм обеспечивает их возврат. Вернувшись в ядро, длинные хвосты подрезаются ядерным экзосомом, основные белки snoRNP полностью собираются, и зрелые комплексы перемещаются в нуклеолус. Важно, что snoRNA, прошедшие этот крюк, оставались полностью функциональными: модельная snoRNA snR13 по‑прежнему выполняла свои специфические химические модификации рРНК после завершения CPF‑CF и прохождения через цитоплазму.
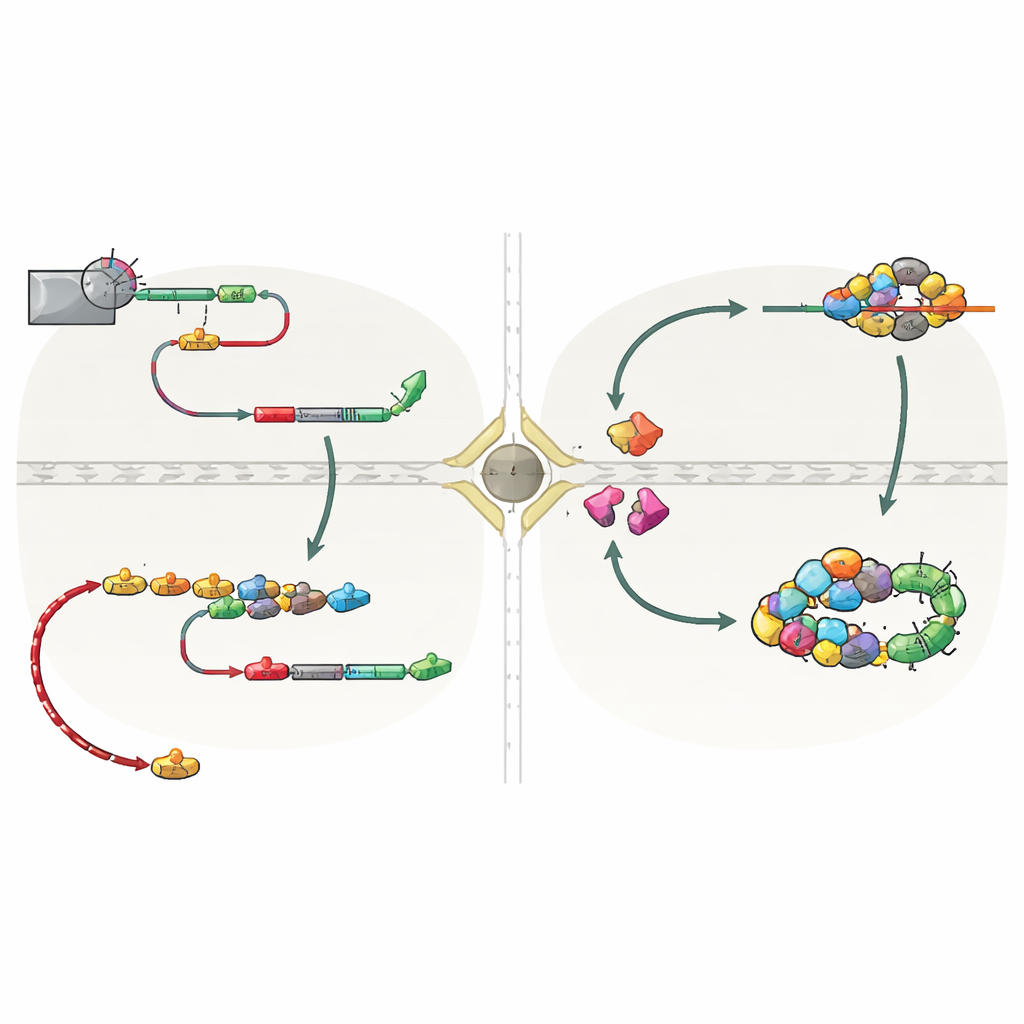
Почему этот скрытый путь важен
Эта работа показывает, что путешествие snoRNA — не частный случай, а встроенный запасной маршрут, контролируемый тем, как заканчивается транскрипция. Когда основная система NNS ослаблена — например, на определённых этапах клеточного цикла — расположенные ниже сигналы CPF‑CF спасают синтез snoRNA. Это предотвращает бесполезную трату уже синтезированной РНК и избегает неконтролируемой транскрипции, которая могла бы мешать соседним генам и повреждать ДНК. Авторы также находят признаки похожего запасного пути в клетках человека, где индивидуально кодируемые snoRNA могут приобретать поли(А)‑хвосты на родственных сайтах. Проще говоря, исследование показывает: «сигнал стоп», выбранный в конце гена snoRNA, решает, созревает ли эта РНК тихо в ядре или кратко выходит и возвращается под наблюдением белков‑сторожей. Этот механизм надзора, зависящий от завершения транскрипции, помогает поддерживать гибкость и безопасность РНК‑ландшафта клетки.
Цитирование: Yu, F., Zaccagnini, G., Duan, Y. et al. CPF-CF-terminated snoRNAs shuttle through the cytoplasm via an mRNA guard protein-mediated surveillance mechanism. Nat Commun 17, 2328 (2026). https://doi.org/10.1038/s41467-026-70373-8
Ключевые слова: snoRNA, контроль качества РНК, экспорт из ядра, завершение транскрипции, генетика дрожжей