Clear Sky Science · ru
Синхронная активация холинергических интернейронов полосатого тела вызывает локальный выброс серотонина
Почему это открытие в химии мозга важно
Привычки, мотивация и компульсивные поведения зависят от небольшой, но жизненно важной области мозга — полосатого тела. Два хорошо известных нейромедиатора, дофамин и серотонин, регулируют работу этой структуры, и многие психиатрические препараты направлены на восстановление их баланса. В исследовании обнаружен ранее незамеченный путь связи: особый класс нейронов, выделяющих ацетилхолин, может напрямую воздействовать на серотонинергические волокна и вызывать увеличение выброса серотонина, но только в определённой части полосатого тела. Эта новая связь может помочь объяснить, почему при расстройствах, таких как обсессивно‑компульсивное расстройство (ОКР) и болезнь Паркинсона, часто наблюдаются одновременные изменения нескольких нейромедиаторных систем.
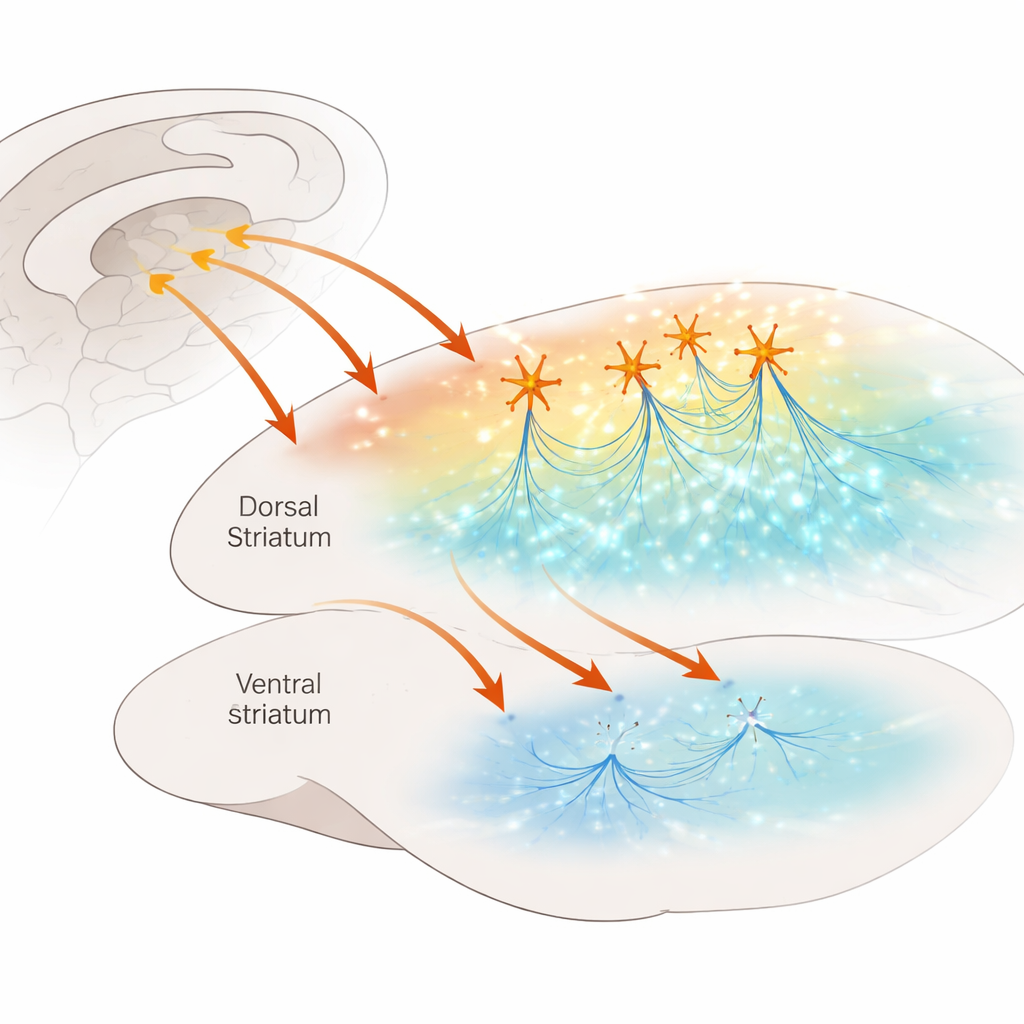
Оживлённый перекрёсток в мозге
Дорсальное полосатое тело действует как узловой центр принятия решений, помогая нам переключаться между целенаправленными действиями и автоматическими привычками. Оно получает плотные входы из коры и окружено нейромодуляторами, такими как дофамин и серотонин, которые тонко настраивают обработку сигналов. В этом узле обитает разреженная, но мощная популяция холинергических интернейронов — клеток, выделяющих ацетилхолин и регулярно генерирующих импульсы, словно маленькие метрономы. Ранние работы показали, что когда эти клетки учащённо и синхронно активируются, они сильно усиливают выброс дофамина, действуя через никотиновые ацетилхолиновые рецепторы, расположенные на дофаминовых волокнах. Оставалось неизвестным, существует ли аналогичный обходной путь для серотонина, хотя серотонин играет центральную роль в настроении, обучении и в эффекте препаратов, применяемых при ОКР и депрессии.
Наблюдать за всплесками серотонина в реальном времени
Чтобы ответить на этот вопрос, исследователи использовали мышей с флуоресцентным сенсором, яркость которого увеличивается при наличии серотонина. Они ввели вирус с этим сенсором в полосатое тело, приготовили тонкие срезы мозга и с помощью двухфотонной микроскопии наблюдали сигналы серотонина при стимуляции ткани. Электрическая стимуляция в дорсальном полосатом теле вызывала заметные, медленно затухающие вспышки активности сенсора серотонина. Когда команда применила препарат, блокирующий никотиновые ацетилхолиновые рецепторы, эти вспышки уменьшались и становились более локализованными, что указывает на то, что ацетилхолин через эти рецепторы способствует как увеличению выброса серотонина, так и его распространению на большую область. Поразительно, что в вентральном полосатом теле — соседнем регионе с ещё более плотной серотонинергической иннервацией — такого вклада никотиновых рецепторов не наблюдали, что показало региональную специфичность этого взаимодействия.
Вызывать выброс серотонина сфокусированным светом
Чтобы выяснить, может ли ацетилхолин, выделяемый только холинергическими интернейронами, сам по себе вызывать выброс серотонина, авторы обратились к оптогенетике. Они модифицировали эти интернейроны так, чтобы те реагировали на короткие вспышки синего или жёлтого света и синхронно активировали их, продолжая при этом мониторинг сенсора серотонина. Один миллисекундный световой импульс был достаточен, чтобы вызвать сильный серотонинергический сигнал в дорсальном полосатом теле, по временной динамике похожий на никотин‑чувствительную компоненту электрически вызванного ответа. Блокада никотиновых рецепторов почти полностью устраняла этот сигнал, даже когда другие химические входы и рецепторы в срезе были фармакологически заглушены. Такое сочетание точной стимуляции и рецепторной блокады показало, что ацетилхолин действует непосредственно на никотиновые рецепторы вдоль серотонинергических волокон, чтобы вызвать локальный выброс серотонина, а не опосредованно через другие типы клеток или через дофаминовые аксоны.
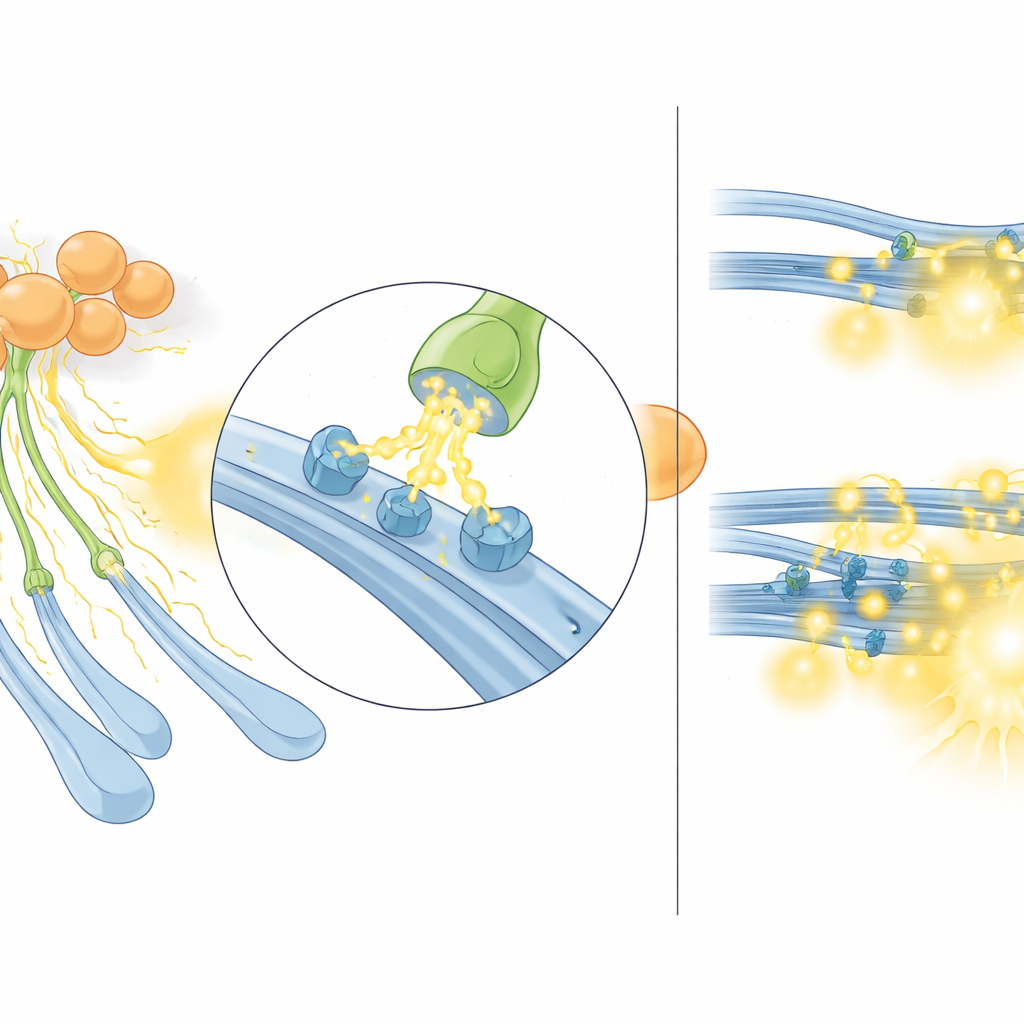
Когда система работает слишком активно
Команда далее исследовала, что происходит в состоянии, релевантном болезни, при котором холинергическая передача аномально усилена. Для этого использовали мышей с нокаутом гена Sapap3 — хорошо известную модель, демонстрирующую чрезмерное ухаживание за собой и другие поведения, похожие на ОКР, у которой ранее было показано повышенное возбуждение холинергических интернейронов и увеличенный выброс ацетилхолина. У этих мышей электрическая стимуляция дорсального полосатого тела вызывала более крупные сигналы сенсора серотонина по сравнению с нормальными животными. Важно, что эта разница исчезала при блокаде никотиновых рецепторов, то есть усиливалась только ацетилхолин‑зависимая часть выброса серотонина. Аналогичная картина наблюдалась и для дофамина. Иными словами, в этом гиперхолинергическом состоянии холинергические интернейроны непропорционально усиливают никотиновую компоненту выброса моноаминов, фактически позволяя ацетилхолину «перехватывать» серотонинергические волокна как основной путь серотонинергической отдачи.
Шире последствия для заболеваний мозга
Эти результаты выявляют тонко настроенный и регионально ограниченный диалог между ацетилхолином и серотонином в дорсальном полосатом теле. В здоровом мозге синхронные всплески активности холинергических интернейронов — например, вызванные внезапными, поведенчески значимыми событиями — могут временно расширять и усиливать серотонинергические сигналы, влияя на обучение и подавление действий. В патологических состояниях, когда ацетилхолин постоянно повышен, как у мышей с нокаутом Sapap3 и, возможно, при таких заболеваниях, как ОКР или болезнь Паркинсона, тот же механизм может чрезмерно усиливаться, способствуя аномальным паттернам сигнализации серотонина и дофамина. Понимание этой скрытой связи открывает новый взгляд на то, как несколько нейромодуляторов взаимодействуют в нормальном поведении и при заболеваниях, и в перспективе может помочь разработать подходы к лечению, которые точнее нацелены на их совместную динамику, а не на отдельную химию каждой системы.
Цитирование: Matityahu, L., Hobel, Z.B., Berkowitz, N. et al. Synchronous activation of striatal cholinergic interneurons induces local serotonin release. Nat Commun 17, 2278 (2026). https://doi.org/10.1038/s41467-026-70359-6
Ключевые слова: стриальный серотонин, холинергические интернейроны, никотиновые ацетилхолиновые рецепторы, обсессивно-компульсивное расстройство, базальные ганглии