Clear Sky Science · ru
Контроль функции лизосом GTP-активирующим белком TBC1D9B и его связывающим партнёром TMEM55B
Как центры утилизации клетки сохраняют равновесие
В каждой нашей клетке есть крошечные мешочки — лизосомы, которые выполняют роль центров переработки и узлов управления ростом. Когда они исправно работают, изношенные компоненты расщепляются и их части повторно используются; при сбое отходы накапливаются, что может приводить к заболеваниям, включая нейродегенерацию и рак. В этом исследовании показано, как два малоизвестных белка помогают переключать лизосомы между подвижным, способствующим росту состоянием и сконированным, направленным на утилизацию положением, проливая свет на то, как клетки адаптируются к избытку и недостатку пищи.
Перемещение центров переработки внутри клетки
Лизосомы не прикованы к месту. Они перемещаются по внутренним «рельсам», их тянут наружу одни молекулярные моторы и втягивают внутрь другие. Их положение в клетке важно: при обилии питательных веществ лизосомы распространяются к периферии клетки и поддерживают сигналы роста; при голодании они отступают к центру, становятся более кислыми и усиливают расщепление клеточного материала. Небольшой переключающий белок ARL8 известен тем, что продвигает лизосомы наружу, но до сих пор не удавалось выявить специализированную «тормозную» систему, которая могла бы его сдерживать. Авторы предположили, что такой тормоз необходим для быстрой перестройки клетки в режим экономии при голоде.
Молекулярное партнёрство на поверхности лизосомы
С помощью методов «рыбалки» белков и масс‑спектрометрии исследователи обнаружили, что белок TBC1D9B связывается с мембранным лизосомальным белком TMEM55B. TMEM55B располагается в наружной оболочке лизосомы, тогда как TBC1D9B в основном растворим и может прикрепляться к мембране. Команда показала, что эти два белка образуют прямой комплекс: очищенный TBC1D9B связывается с выступающей частью TMEM55B в пробирке, а меченые варианты белков вытягивают друг друга из клеточных экстрактов. Тщательное картирование фрагментов белка выявило несколько участков TBC1D9B, контактирующих с TMEM55B, что позиционирует TBC1D9B на поверхности лизосомы, не закрывая при этом область, ответственную за его каталитическую активность.
Когда тормоз отказывает, лизосомы выходят из-под контроля
Чтобы выяснить функции этого партнёрства, авторы использовали редактирование CRISPR для удаления TMEM55B или TBC1D9B из человеческих клеток. В обоих случаях лизосомы перестали собираться вблизи ядра и вместо этого разбрасывались к периферии клетки и перемещались быстрее по своим «рельсам», имитируя состояние постоянно сытых клеток. Повторное введение нормального TBC1D9B восстановило правильное расположение, тогда как вариант без каталитической активности — нет, что указывает на необходимость ферментативной функции. При голодании контрольные клетки втягивали лизосомы внутрь и усиливали их переваривающую активность, о чём свидетельствовало повышение активности ключевых ферментов и улучшенное расщепление тестового груза. Клетки без TMEM55B или TBC1D9B не смогли этого сделать: их лизосомы оставались периферическими, а деградационный отклик на голод был ослаблен. Аутофагия — процесс, при котором клетки «поедают» повреждённые компоненты — также нарушалась: наблюдалась менее эффективная обработка аутофагического репортера и накопление адапторного белка p62.
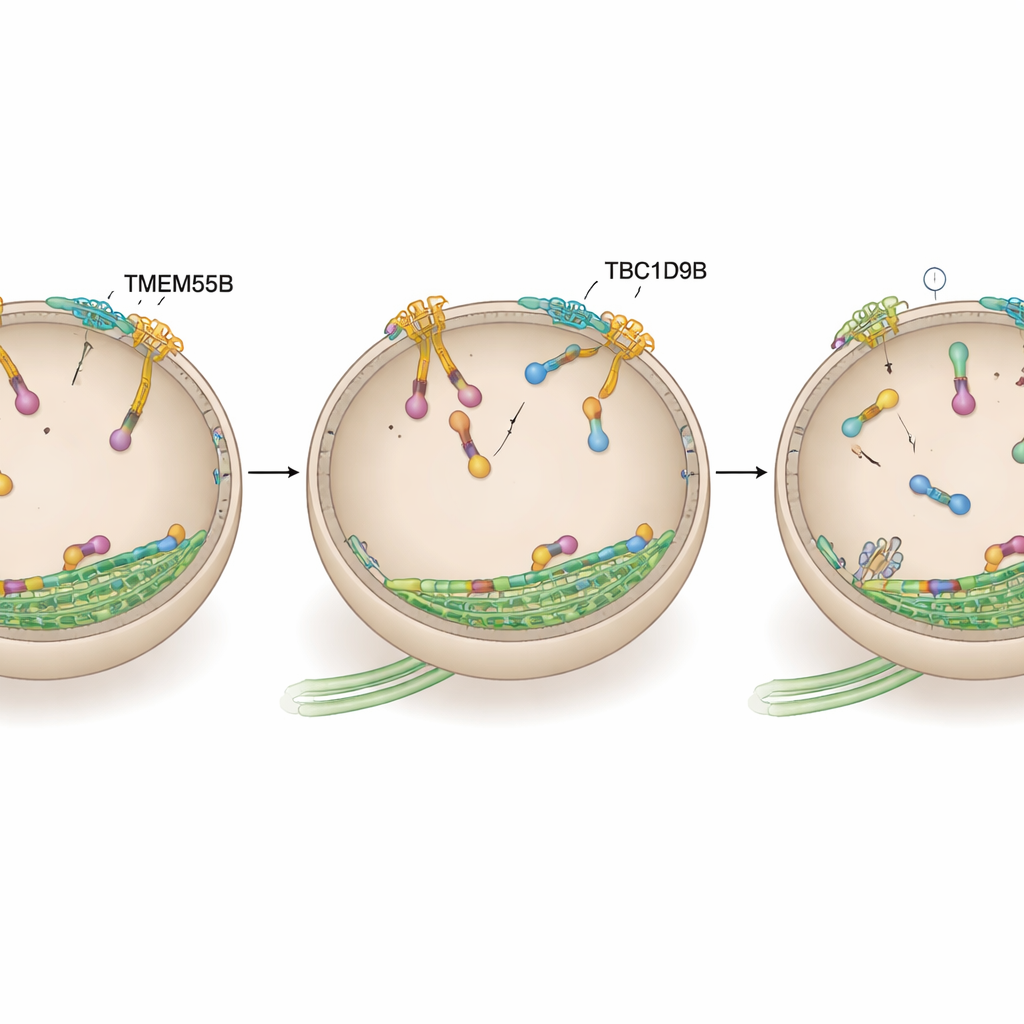
Выключение двигателя лизосомы
Далее команда проверила, действует ли TBC1D9B напрямую на ARL8 — переключатель, отвечающий за движение наружу. С помощью проксимального метилирования в человеческих нейронах и тестов связывания в клеточных линиях и с очищенными белками они показали, что TBC1D9B селективно связывается с активной, GTP‑загруженной формой варианта ARL8B, но не с его неактивной формой и не с близким родственным ARL8A. Структурное моделирование предсказало, что ключевые остатки в TBC1D9B контактируют с карманом, связывающим GTP у ARL8B. В биохимических тестах TBC1D9B ускорял гидролиз GTP, связанного с ARL8B, фактически переводя белок из состояния «включено» в «выключено»; мутантный вариант TBC1D9B, лишённый этих остатков, был неспособен этого делать. В согласии с этим, в клетках, лишённых TMEM55B или TBC1D9B, на лизосомах обнаруживалось больше ARL8B, тогда как сверхэкспрессия TBC1D9B втягивала лизосомы обратно к центру, что напоминало ослабление активности ARL8B.
Новая ручка управления клеточным хозяйством
Наконец, авторы проверили, объясняет ли этот «тормоз» ARL8B клеточные изменения, наблюдаемые при отсутствии TBC1D9B. При удалении ARL8B лизосомы оставались сосредоточенными у ядра независимо от наличия TMEM55B или TBC1D9B, а дефекты аутофагии, вызванные потерей TBC1D9B, в основном устранялись. В совокупности данные поддерживают модель, в которой TMEM55B привлекает TBC1D9B к лизосомам, где тот инактивирует ARL8B и позволяет лизосомам переключаться с рассеянного состояния, поддерживающего рост, на централизованное состояние, ориентированное на переваривание. Для неспециалистов это означает, что исследование выявило важный регуляторный «регулятор», который клетки используют, чтобы решать, когда активизировать переработку — процесс, имеющий последствия для заболеваний, связанных с накоплением отходов в мозге, обменом веществ и раком.
Цитирование: Duhay, V., Tian, M., Kosieradzka, K. et al. Control of lysosome function by the GTPase-activating protein TBC1D9B and its binding partner TMEM55B. Nat Commun 17, 2487 (2026). https://doi.org/10.1038/s41467-026-70345-y
Ключевые слова: лизосомы, аутофагия, клеточная сигнализация, транспорт органелл, нейродегенерация