Clear Sky Science · ru
Фрагменты SLIT3 координируют нейроваскулярную экспансию и термогенез в бурой жировой ткани
Как «хороший жир» в нашем организме помогает сохранять тепло
Когда мы оказываемся на холоде, организм быстро включается в поддержание тепла. Ключевую роль в этой реакции играет бурая жировая ткань — особый тип жира, который сжигает калории для выработки тепла. В этом исследовании показано, как бурая ткань организует свою сеть мельчайших кровеносных сосудов и нервных волокон для усиления теплообразования, раскрывая скрытую систему коммуникации, которую в будущем можно будет использовать для улучшения метаболизма и лечения заболеваний, связанных с ожирением.
Скрытая печь внутри тела
Бурая жировая ткань действует подобно внутренней печи. В отличие от белой жировой ткани, запасавшей энергию, бурая ткань потребляет топливо и генерирует тепло при воздействии низкой температуры. Для эффективной работы клетки бурой ткани нуждаются в обильном кровоснабжении, чтобы доставлять кислород и питательные вещества, и в плотной сети симпатических нервов, которые подают сигнал о необходимости «прибавить отопление». На холоде эти сосуды и нервные волокна заметно расширяются. До настоящего времени оставалось неясным, как разные компоненты ткани так точно согласуют свой рост.
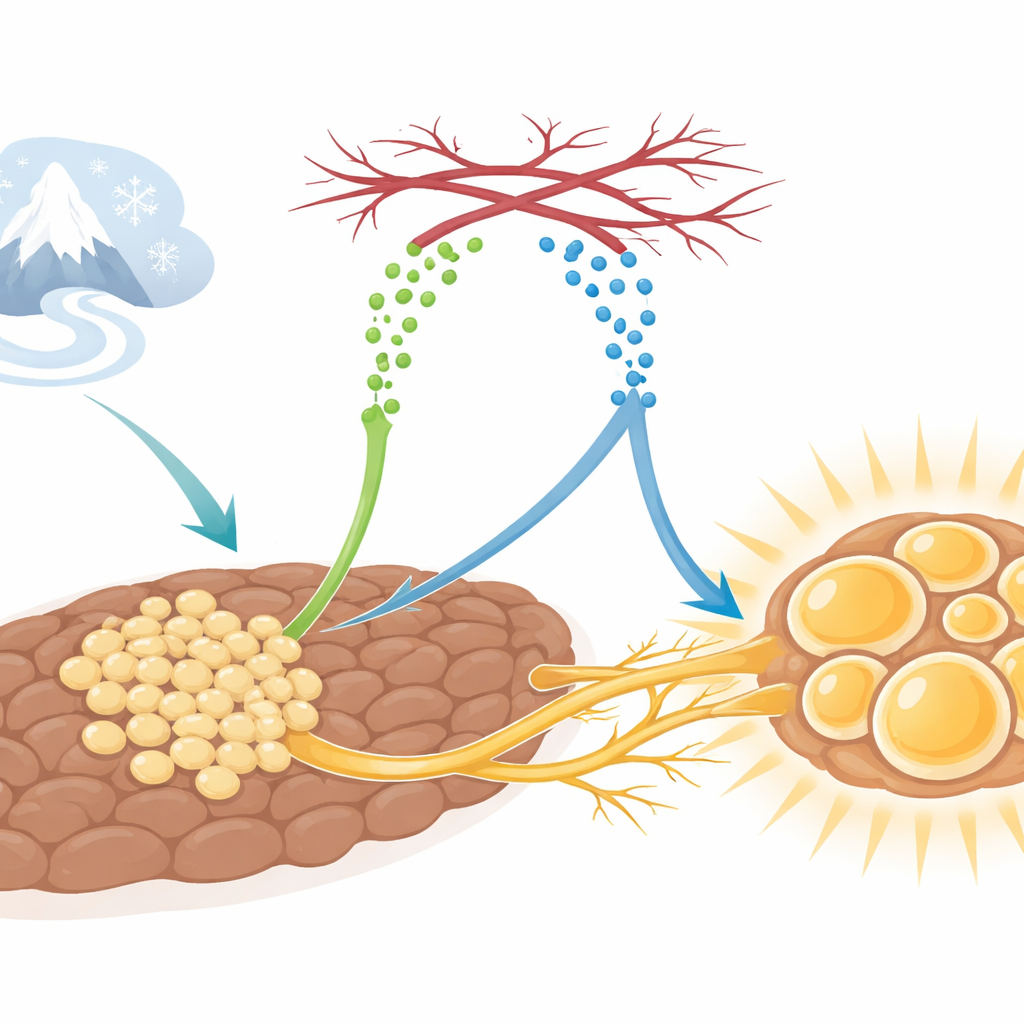
Молекула-посланник, запускающая процесс
Исследователи обнаружили, что белок под названием SLIT3, вырабатываемый незрелыми жировыми клетками — предшественниками адипоцитов, — играет центральную роль в этой координации. У мышей, подвергшихся холоду, уровень SLIT3 в бурой ткани повышается. При блокировке SLIT3 именно в бурой жировой ткани или в этих предшественниках животные испытывали трудности с поддержанием температуры тела в холоде. Их бурая ткань «обветшала»: жировые капли увеличивались, снижалась экспрессия генов, отвечающих за выработку тепла, таких как Ucp1, и уменьшалось энергопотребление, несмотря на то что пищевой прием и активность оставались без изменений. Это указывало на то, что SLIT3 — ключевой организатор реакции бурой ткани на холод не путем изменения внутреннего «механизма» каждой клетки, а через формирование окружающей тканевой среды.
Совместное строительство сосудов и нервных проводов
При более детальном изучении ученые обнаружили, что в бурой ткани без SLIT3 стало меньше мелких кровеносных сосудов и симпатических нервных волокон, пронизывающих ткань. 3D-визуализация подтвердила, что нервная сеть значительно реже. Важно, что при обходе обычного нервного сигнала посредством препарата, который напрямую активирует бурую ткань, клетки реагировали нормально. Это показало: SLIT3 не обязателен для способности адипоцитов сжигать топливо, а необходим для строительства нейроваскулярной «проводки», которая позволяет мозгу контролировать эти клетки. Команда выделила предшественники адипоцитов как главный локальный источник SLIT3 и показала, что удаление SLIT3 только в этих клетках достаточно, чтобы подавить рост сосудов, рост нервов и выработку тепла при холодовом воздействии.
Один белок, две части, две функции
SLIT3 не действует как единый статичный сигнал. Исследователи показали, что фермент BMP1 расщепляет SLIT3 на два отдельных фрагмента с различными ролями. N-концевой фрагмент (SLIT3-N) в основном стимулирует рост капилляров, действуя через рецепторы на эндотелиальных клетках, выстилающих кровеносные сосуды. C-концевой фрагмент (SLIT3-C) преимущественно способствует расширению симпатических нервов. Они выявили рецептор PLXNA1 на нервных волокнах как прямой «док» для SLIT3-C, что подтверждалось биохимическими тестами на связывание и компьютерными структурными моделями. При снижении уровня PLXNA1 способность SLIT3 или SLIT3-C усиливать рост нервов и повышать температуру бурой ткани утрачивалась, а общая плотность нервов и уровни норадреналина в ткани резко падали.
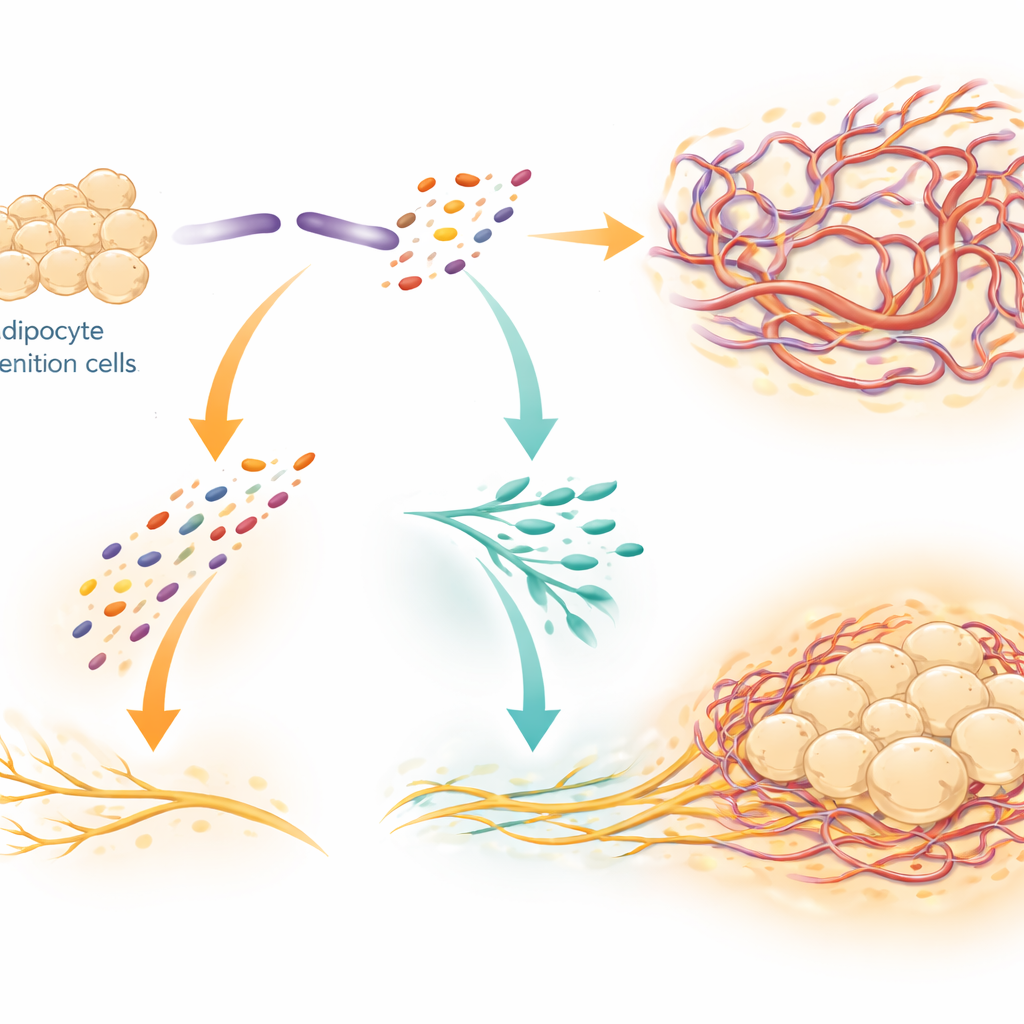
Связь с человеческим метаболизмом и здоровьем
Чтобы выяснить, имеет ли эта система значение для людей, авторы проанализировали образцы жировой ткани из крупных когорт людей с ожирением. Более высокая экспрессия SLIT3 в адипозной ткани ассоциировалась со здоровыми признаками: большим уровнем гормона адипонектина, меньшим количеством воспалительных иммунных клеток в висцеральном жире, лучшим контролем уровня глюкозы в крови и более высокими уровнями полезного адипокина оментин. Генетические исследования в других работах также связывали варианты рядом с геном SLIT3 и его рецептором PLXNA1 с ожирением и инсулинорезистентностью. Вместе эти данные говорят о том, что путь SLIT3 может способствовать поддержанию здоровой жировой ткани и метаболического баланса у людей.
Что это значит для сохранения тепла и здоровья
В целом исследование показывает, что незрелые жировые клетки в бурой ткани делают больше, чем просто превращаются в зрелые адипоциты: они активно формируют опорную сеть ткани. Выделяя SLIT3 и допуская его расщепление на два фрагмента, эти клетки независимо, но синхронно стимулируют рост сосудов и нервов, необходимых для эффективного производства тепла. Эта тонко настроенная «две в одном» сигнальная система обеспечивает способность бурой ткани быстро включаться, когда окружающая среда требует дополнительного тепла. В перспективе понимание и безопасное использование этого пути может открыть новые возможности для повышения расхода энергии, улучшения здоровья жировой ткани и борьбы с метаболическими заболеваниями.
Цитирование: Serdan, T.D.A., Cervantes, H., Frank, B. et al. SLIT3 fragments orchestrate neurovascular expansion and thermogenesis in brown adipose tissue. Nat Commun 17, 2445 (2026). https://doi.org/10.1038/s41467-026-70310-9
Ключевые слова: бурая жировая ткань, термогенез, нейроваскулярное ремоделирование, сигнализация SLIT3, метаболическое здоровье