Clear Sky Science · ru
Активация NF-κB в астроцитах ухудшает заживление после черепно‑мозговой травмы у самцов мышей
Почему мозговые ушибы не всегда заживают чисто
Когда человек получает удар по голове, видимая снаружи травма — лишь часть картины. Глубоко в мозге разворачивается сложная реакция на повреждение, от которой зависит, восстановится ли человек или у него останутся длительные нарушения мышления, настроения или моторики. Это исследование на самцах мышей показывает, как ключевой стресс‑маршрут в опорных клетках — астроцитах — может превратить нормальную репаративную реакцию в процесс, который фактически усугубляет повреждение после черепно‑мозговой травмы.
Скрытые первичные спасатели мозга
Астроциты — звездообразные клетки, окружающие нейроны и кровеносные сосуды, которые помогают поддерживать стабильность внутренней среды мозга. После травмы головы они быстро меняют форму и поведение, формируя барьер вокруг повреждённой зоны и помогая восстанавливать ткань. Исследователи сосредоточились на молекулярном переключателе внутри этих клеток — NF-κB, хорошо известном как регулятор воспаления во многих тканях. Они изучали, помогает ли этот переключатель или вредит заживлению мозга после повреждения закрытого типа, схожего с распространёнными у людей сотрясениями и контузиями.
Стресс‑переключатель, который загорается после удара
Анализируя активность генов в тканях мозга мышей после травмы, команда обнаружила всплеск генов, связанных с воспалением и NF-κB‑сигнальным путём, особенно на 3–7‑е дни после травмы, когда нарастает вторичное повреждение. С использованием репортёрных мышей они показали, что активация NF-κB не распространяется по всему мозгу, а концентрируется вокруг места удара. Там она была особенно выражена в микроглии (иммунных сторожах мозга) и в астроцитах, формирующих границу раны. Эта временная и пространственная локализация наводит на мысль, что NF-κB в астроцитах может быть критическим регулятором организации рубца и контроля иммунного ответа.
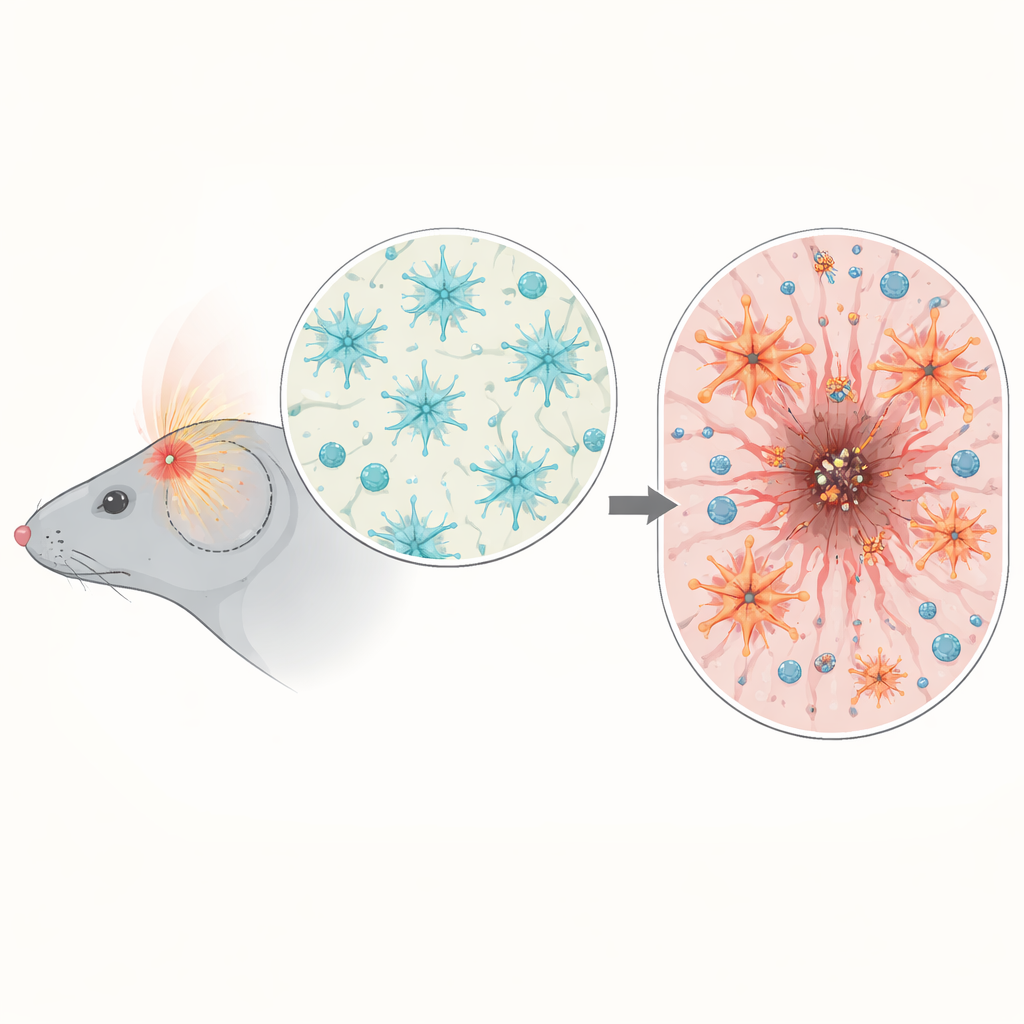
Когда астроциты работают слишком активно
Чтобы проверить причинно‑следственную связь, учёные создали мышей, у которых активность NF-κB в астроцитах была либо искусственно повышена, либо ослаблена, но только после завершения развития мозга. После травмы головы мыши с гиперактивным NF-κB в астроцитах теряли больше веса, показывали худшие ранние неврологические показатели и имели более крупные и стойкие очаги повреждения как в гистологических срезах, так и на МРТ. Вместо аккуратного, чётко оформленного рубца, изолирующего повреждённое ядро, их астроциты формировали толстую, дезорганизованную границу, которая не сокращала рану со временем. Нарушался нормальный баланс матриксных белков вокруг повреждения, а ключевая наружная барьерная структура — глиальная лимитанс — формировалась слабо, оставляя окружающий мозг менее защищённым.
Когда программы заживления сбиваются с пути
Вдаваясь в молекулярные детали, команда выделила астроциты и соседние иммунные клетки для посегнетного анализа экспрессии генов. У здоровых животных травма обычно подавляет часть повседневных «бытовых» функций астроцитов и одновременно включает гены, поддерживающие закрытие раны и регенерацию. Напротив, астроциты с хронически активным NF-κB уже выглядели «повреждёнными» даже до травмы, а после удара не смогли полностью включить полезные программы ремонта, такие как контролируемая трансформация, помогающая клеткам выстроить эффективную границу. Вместо этого они преимущественно активировали воспалительные гены, приобрели черты токсичного состояния астроцитов, связанного со старением и нейродегенерацией, и демонстрировали признаки секреторного профиля, похожего на сенесценцию, связанного с хроническими, не заживающими ранами.
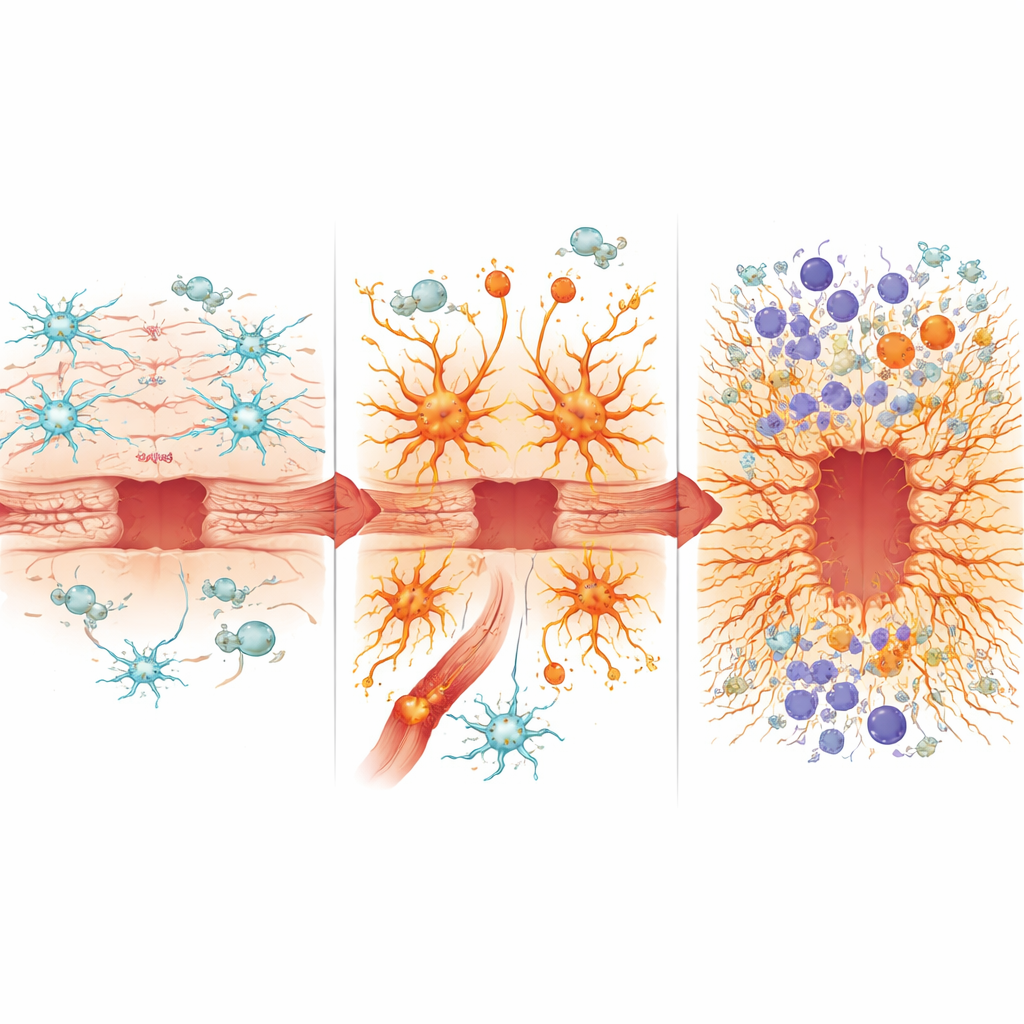
Подпитывание иммунного пламени
Эти неправильно запрограммированные астроциты также перестроили иммунную среду мозга. Гематоэнцефалический барьер стал более проницаемым, пропуская больше периферических иммунных клеток. У мышей с гиперактивным NF-κB в астроцитах наблюдалось более интенсивное инфильтрирование воспалительными миелоидными клетками и изменённые пропорции нейтрофилов, моноцитов и дендритных клеток, а также увеличение цитотоксичных Т‑клеток, которые могут дальше повреждать ткань. Иммунные клетки в такой среде выражали усиленные сигналы, опосредованные интерфероном и инфламмасомой, связанные с агрессивным, потенциально нейротоксичным воспалением. Одновременно уровни нескольких защитных или про‑репаративных белков, таких как остеопонтин, снижались, тогда как другие, связанные с оксидативным стрессом, избытком железа и формированием рубца — включая гемоксигеназу‑1 и липокалина‑2 — были повышены. Соотношение остеопонтина и липокалина‑2 проявило себя как простой маркер, который соответствовал лучшему или худшему заживлению в разных штаммах мышей.
Что это значит для восстановления после черепно‑мозговой травмы
В совокупности результаты показывают, что при хронической активации стресс‑пути NF-κB в астроцитах эти клетки переключаются с поддержки упорядоченного восстановления на стимуляцию хаотичного рубцевания и длительного воспаления. Вместо того чтобы выстраивать аккуратную границу, содержащую повреждение и позволяющую ремоделировать ткань, они способствуют образованию проницаемой, воспалительной ниши, которая увеличивает очаг поражения и ухудшает долгосрочный прогноз. Хотя работа выполнена на самцах мышей, она указывает на NF-κB в астроцитах как перспективную терапевтическую мишень для улучшения восстановления после черепно‑мозговой травмы и предполагает, что уровни в крови таких молекул, как остеопонтин и липокалин‑2, могут в будущем помочь клиницистам отслеживать, насколько хорошо заживает мозг пациента.
Цитирование: Hein, T.M., Nespoli, E., Hakani, M. et al. NF-κB activation in astrocytes impairs wound healing after traumatic brain injury in male mice. Nat Commun 17, 2323 (2026). https://doi.org/10.1038/s41467-026-70304-7
Ключевые слова: черепно-мозговая травма, астроциты, нейровоспаление, образование мозгового рубца, NF-kappa B