Clear Sky Science · ru
NAA40 и NAC взаимодействуют при ко-трансляционной ацетилировании гистонов у человека
Как клетки тонко настраивают свои генетические переключатели
Внутри каждой человеческой клетки вновь синтезируемые белки подвергаются химическим изменениям по мере их выхода из молекулярных «фабрик» белка — рибосом. Эти небольшие модификации могут определить, куда направится белок, какова будет его стабильность и даже как будут включаться или выключаться гены. В этой статье рассматривается высокоспецифичный фермент NAA40 и вспомогательный комплекс NAC, показывая, как они совместно работают на рибосоме, модифицируя гистоновые белки — шпульки, вокруг которых намотана ДНК — и тем самым влияют на активность генов и потенциально на развитие рака.
Маленькая шапочка, меняющая поведение гистонов
Многие белки человека получают небольшую химическую «шапочку» на своём N‑конце — процесс, известный как N‑терминальная ацетилирование. Гистоны H2A и H4, участвующие в упаковке ДНК в хроматин, почти всегда несут такую метку. NAA40 необычен среди ферментов тем, что специализируется почти исключительно на добавлении этой шапочки к данным гистонам в момент их синтеза. Эта ацетильная метка конкурирует с другими химическими модификациями, такими как фосфорилирование и метилирование, в той же области гистонов, поэтому активность NAA40 может менять степень уплотнения ДНК и регуляцию генов. Важно, что изменённые уровни NAA40 связывают с несколькими типами рака, что делает его перспективной мишенью для новых терапий.
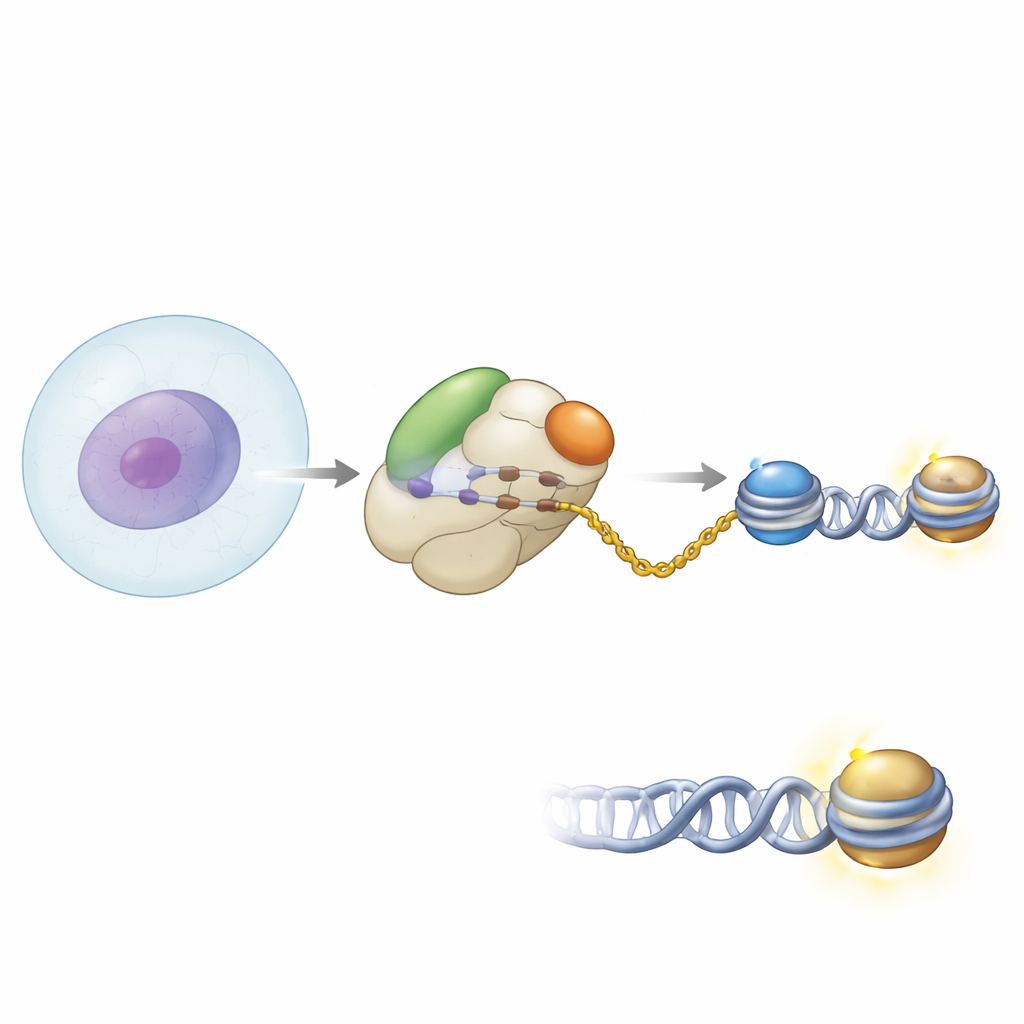
Партнёрство у входа на белковую фабрику
Авторы использовали биохимические методы и крио‑электронную микроскопию высокого разрешения, чтобы увидеть, как NAA40 располагается на человеческой рибосоме. Они обнаружили, что NAA40 размещается прямо у выхода туннеля, откуда появляются новосинтезированные полипептидные цепи. Там он не действует в одиночку: NAA40 связывается рядом с NAC — комплексом, ассоциированным с нарастающим полипептидом, который сопровождает новые белки при их выходе. Структурные снимки показали, что NAA40 якорится на рибосоме с помощью уникального положительно заряженного спиралевидного участка в своём N‑конце, тогда как NAC прикреплён к поверхности рибосомы через один из своих субъединиц. Гибкий домен NAC протягивается к NAA40, фактически соединяя фермент с рибосомой.
Зачем NAC нужен для настройки гистонов
Чтобы проверить важность этого партнёрства, исследователи воссоздали эти взаимодействия с очищенными компонентами в пробирках. Они наблюдали, что NAA40 сам по себе слабо связывается с рибосомами, но в присутствии NAC связывание с рибосомой становится значительно сильнее. Если удалить конкретный участок NAC, называемый «UBA», который контактирует с NAA40, это усиленное связывание исчезает. В клетках человека истощение NAC приводило к снижению NAA40‑зависимого ацетилирования гистона H4 и сопутствующему увеличению конкурентной фосфорильной метки на том же хвосте гистона. Это изменение происходило без изменения количества или локализации самого NAA40, указывая на то, что основная роль NAC — привлекать и правильно позиционировать NAA40 на транслирующих рибосомах, чтобы гистоны могли эффективно модифицироваться в момент их синтеза.
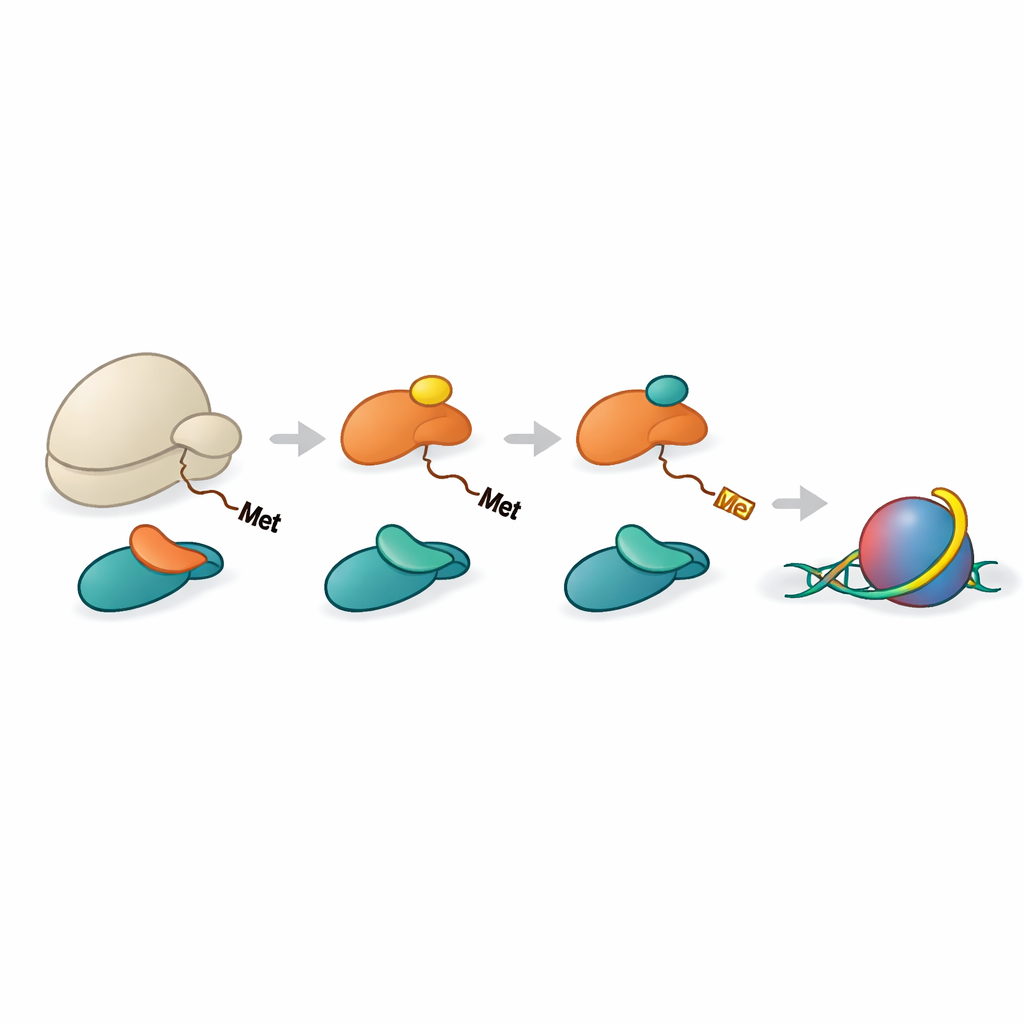
Координированная сборочная линия для обработки гистонов
Гистоны H2A и H4 должны сначала потерять исходную аминокислоту метионин, прежде чем NAA40 сможет их распознать. Другой фермент, METAP1, выполняет эту обрезку. Команда показала, что NAC может способствовать совместному привлечению METAP1 и NAA40 к рибосоме, формируя многоферментную сборочную станцию у выхода пептида. Структуры высокого разрешения воссозданных комплексов продемонстрировали, что METAP1 и NAA40 связываются рядом друг с другом на рибосоме, а их активные центры располагаются на почти равном расстоянии от выходного туннеля. Такая геометрия обеспечивает, что как только хвост гистона выступает на дюжину или около того аминокислот за пределы рибосомы, METAP1 может удалить стартовый метионин, и NAA40 сразу добавить ацетильную шапочку, минимизируя задержку между этими двумя шагами.
Последствия для контроля генов и рака
В целом исследование показывает, что NAA40 не блуждает по клетке в поисках гистонов для модификации. Скорее, он закреплён на рибосоме при помощи NAC, образуя часть организованной станции обработки, которая подготавливает гистоны в момент их синтеза. Плотное связывание удаления метионина и добавления ацетиля гарантирует, что гистоны H2A, H4 и вариант H2A.X, связанный с повреждением ДНК, быстро получают ацетильную метку, способную формировать структуру хроматина и регуляцию генов. Поскольку нарушения этого раннего шага маркировки гистонов могут способствовать канцерогенезу, понимание точного расположения NAA40, NAC и METAP1 на рибосоме даёт структурный чертёж, который может направлять разработку лекарств, нацеленных на тонкую настройку этого критического эпигенетического контрольного пункта.
Цитирование: Guan, D., Denk, T., Klavaris, A. et al. NAA40 and NAC cooperate in co-translational histone acetylation in humans. Nat Commun 17, 2486 (2026). https://doi.org/10.1038/s41467-026-70279-5
Ключевые слова: ацетилирование гистонов, NAA40, рибосома, комплекс, связанный с нарастающим полипептидом, эпигенетическая регуляция