Clear Sky Science · ru
Переход от ацетилирования к фосфорилированию, зависимый от клеточного цикла, регулирует своевременное созревание центросом
Сохраним наши генетические грузы на правильном пути
Каждый раз, когда клетка в нашем теле делится, ей нужно крайне точно распределить свою ДНК. Когда этот процесс нарушается, клетки могут потерять или приобрести хромосомы — опасное состояние, связанное с раком и другими заболеваниями. В этом исследовании обнаружен молекулярный таймер, который помогает клеткам собирать крошечные структуры, необходимые для правильного разделения хромосом, — это выявляет потенциальную уязвимость, которую в будущем можно будет использовать в антираковых терапиях.
Маленькие транспортные узлы клетки
В центре каждой делящейся клетки расположены центросомы — небольшие структуры, которые действуют как транспортные узлы для нитей, оттягивающих хромосомы. Перед вступлением клетки в деление эти узлы должны «созреть»: они накапливают вспомогательные белки и становятся мощными организаторами микротрубочек — динамических нитей, формирующих делительное веретено. Если созревание происходит слишком рано, слишком поздно или не происходит вовсе, хромосомы могут распределяться неправильно, что приводит к клеткам с аномальным числом хромосом. Понимание того, как клетки включают центросомы в нужный момент, долгие годы оставалось важным вопросом клеточной биологии.
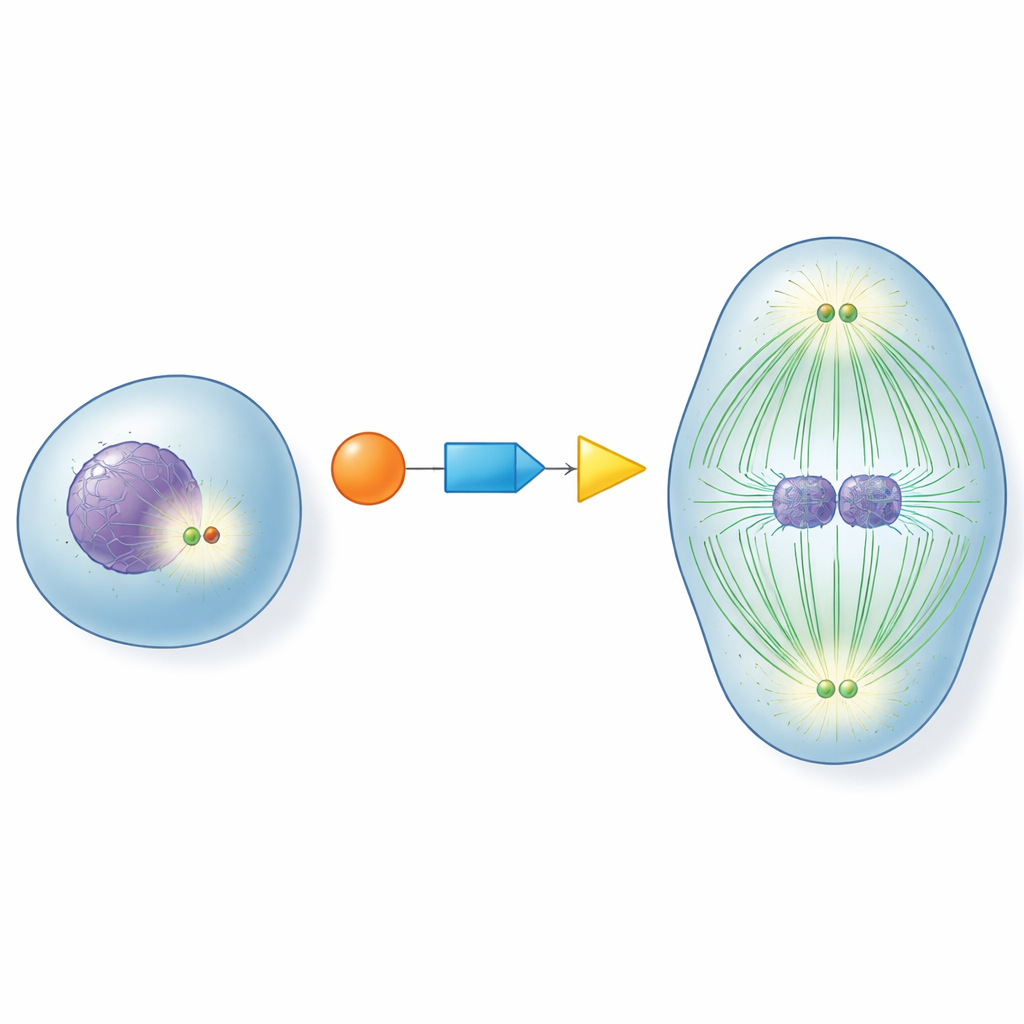
Молекулярная эстафета для идеального тайминга
Авторы сосредоточились на трёх ключевых белках, действующих как эстафета: CDK1 — главный регулятор клеточного цикла; RNF40 — прежде в основном известный как модификатор белков упаковки ДНК; и PLK1 — важный драйвер деления клетки. Они обнаружили, что RNF40 физически присутствует в центросомах на протяжении всего клеточного цикла и напрямую связывается с PLK1. По мере приближения клетки к делению CDK1 химически помечает RNF40 в двух конкретных позициях, что делает RNF40 лучшей «стоянкой» для PLK1. Эта цепочка CDK1–RNF40–PLK1 обеспечивает прибытие PLK1 в центросомы точно в поздней подготовительной фазе деления, запуская мощное созревание центросом, рост микротрубочек и сборку правильно сформированного биполярного веретена.
Переключатель белка, меняющий форму
Любопытно, что RNF40 не всегда принимает эти активирующие метки. В фазах покоя и копирования ДНК RNF40 несёт другую химическую «декорацию» — ацетильные группы — на двух близко расположенных позициях. Эти ацетильные метки добавляет фермент PCAF и позже удаляет деацетилазный партнёр HDAC1. Ацетилированная версия RNF40 сопротивляется модификации CDK1, фактически блокируя следующий шаг эстафеты. По мере перехода клетки в окончательную предделительную стадию HDAC1 постепенно стирает ацетильные метки, позволяя CDK1 добавить фосфатные группы. Этот тщательно отлаженный переход от ацетилирования к фосфорилированию превращает RNF40 из «режима ожидания» в «включённое» состояние, готовое рекрутировать PLK1 и активировать центросому.
Что происходит, когда тайминг сбивается
Чтобы проверить, насколько важен этот переключатель, исследователи создали клетки, в которых RNF40 больше не мог фосфорилироваться, или в которых он был принудительно удержан в состоянии, имитирующем ацетилирование. В обоих случаях PLK1 не накапливался должным образом в центросомах. Такие клетки демонстрировали ослабленный рост микротрубочек из центросом, деформированные веретёна и невыстроенные хромосомы. Многие из них оказались с лишними или отсутствующими хромосомами — состояние, известное как анеуплоидия — а некоторые стали двуядерными, признаки катастрофических ошибок деления. В моделях рака клетки с «ацетилированным» RNF40 формировали в мышах меньшие опухоли и были более чувствительны к распространённым химиотерапевтическим препаратам, применяемым при колоректальном раке, что указывает на то, что нарушение этого переключателя может замедлить рост опухоли.
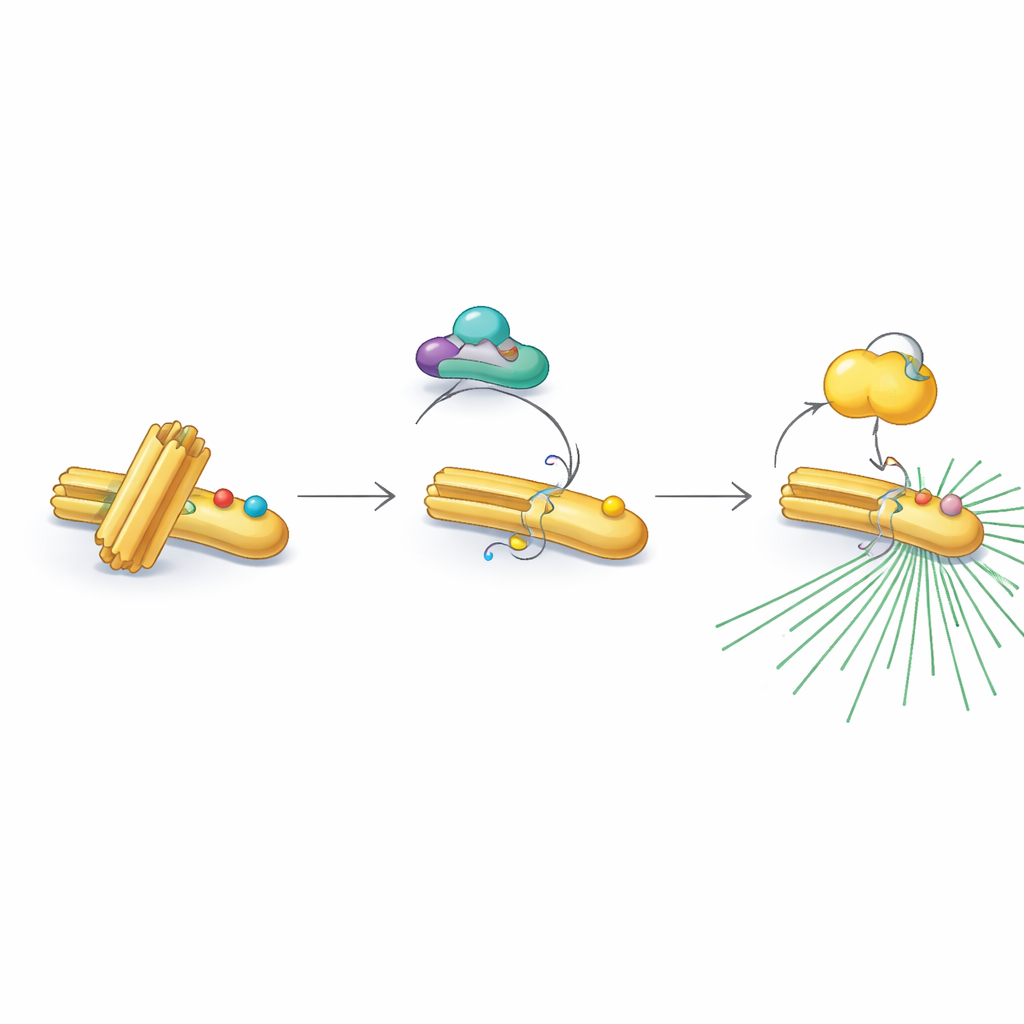
Связь с человеческим раком и будущие возможности
Команда также проанализировала данные пациентов и образцы опухолей. Они обнаружили, что RNF40 часто аномально повышен при колоректальном раке и что некоторые ассоциированные с раком мутации рядом с сайтами модификации нарушают его фосфорилирование, подрывая нормальную функцию центросом. Эти наблюдения напрямую связывают описанный механизм тайминга с человеческими заболеваниями. Указав на конкретный белок, координирующий момент созревания центросом и разделения хромосом, исследование выделяет сигнальный «узел», который можно было бы нацелить, чтобы заставить быстро делящиеся раковые клетки совершать фатальные ошибки деления, при этом менее затрагивая здоровые клетки.
Новый рычаг для обеспечения точного клеточного деления
Для неспециалистов ключевая мысль такова: клетки полагаются на тонко настроенный химический переключатель на одном белке, RNF40, чтобы точно решить, когда активировать механизмы разделения хромосом. Переход от ацетилирования к фосфорилированию ведёт себя как светофор на оживлённом перекрёстке, загорающийся зелёным только тогда, когда клетка действительно готова делиться. Когда «светофор» выходит из строя, клетки сбиваются при делении, накапливают генетические ошибки и могут превратиться в раковые. Понимание и контроль этого переключателя могут открыть новые пути для лечения, которые избирательно дестабилизируют раковые клетки, нарушая их способность правильно делиться.
Цитирование: Li, J., Liang, J., Chen, G. et al. A cell cycle-dependent transition of acetylation to phosphorylation regulates timely centrosome maturation. Nat Commun 17, 2583 (2026). https://doi.org/10.1038/s41467-026-70271-z
Ключевые слова: созревание центросом, клеточное деление, нестабильность хромосом, сигнализация PLK1, колоректальный рак