Clear Sky Science · ru
Восстановление ранней постнатальной дисрегуляции синапсов спасает дегенерацию мотонейронов в мышиной модели спинальной и бульбарной мышечной атрофии
Почему крошечные ранние изменения могут иметь значение для последующей мышечной слабости
Спинальная и бульбарная мышечная атрофия (SBMA) — редкое наследственное заболевание, при котором взрослые, чаще мужчины, постепенно теряют силу в конечностях, туловище и гортани. Симптомы проявляются в среднем возрасте, однако тонкие нарушения начинаются намного раньше. В этом исследовании поднимается неожиданный вопрос: могут ли кратковременные события в первые дни после рождения тихо заложить почву для потери нервных клеток спустя десятилетия — и может ли коррекция этих ранних сбоев защитить движение?
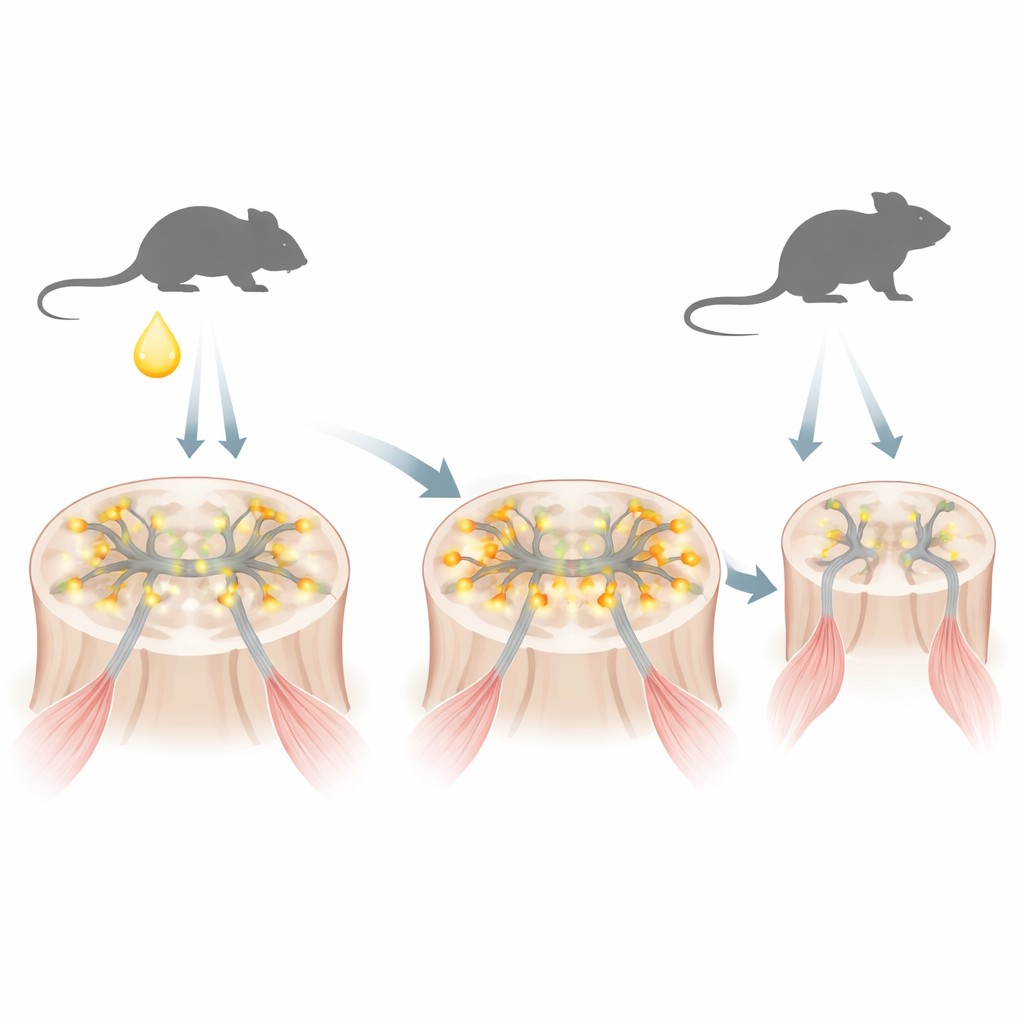
Заболевание, укоренённое в гормонозависимом переключателе
SBMA вызывается изменённой версией андрогенного рецептора, белка, чувствительного к мужским гормонам, таким как тестостерон. Модифицированный рецептор несёт чрезмерно длинную последовательность аминокислоты глутамина. В мышиной модели, имитирующей человеческое заболевание, авторы обнаружили, что сразу после рождения, когда у новорождённых самцов кратковременно повышается тестостерон, этот мутантный рецептор быстро накапливается внутри ядер мотонейронов — нервных клеток, управляющих мышцами. На ранней стадии белок ещё не образует крупные агрегаты, обычно ассоциируемые с нейродегенерацией, но он уже изменяет набор включённых и выключенных генов.
Раннее синаптическое перенапряжение и беспокойные мотонейроны
Используя геномный РНК‑сиквенсинг спинного мозга новорождённых мышей, исследователи обнаружили, что многие гены, вовлечённые в возбуждающие синапсы — точки контакта, где нейроны передают сигнал друг другу — были необычно активны. Многие из этих генов кодируют глутаматные рецепторы, которые повышают склонность нейронов к возбуждению. Группа проследила этот эффект до нарушения функции REST, главного «тормоза» — белка, который в норме строго контролирует такие синаптические гены в ходе развития. У мышей с SBMA и у мотонейронов, полученных из индуцированных плюрипотентных стволовых клеток пациентов, активность REST была ослаблена, а укороченная форма REST4 преобладала, что снимало торможение и усиливало экспрессию глутаматергических синаптических генов. В согласии с этим новорождённые мотонейроны SBMA показывали повышенный уровень c‑Fos — маркера недавней активации, а мотонейроны, полученные от пациентов, демонстрировали более сильные и частые всплески кальция — признаки гипервозбудимости.
Кратковременное раннее лечение, меняющее течение на всю жизнь
Затем исследователи спросили, изменится ли долгосрочное течение болезни, если снизить активность мутантного рецептора или восстановить тормоз REST только в этот неонатальный период. Они вводили антисмысловые олигонуклеотиды — короткие цепочки модифицированного генетического материала — в ликворную пространстве вокруг мозга и спинного мозга однодневных мышат SBMA. Один тип олигонуклеотидов временно снижал уровни как мутантного, так и нормального андрогенного рецептора в центральной нервной системе. Второй тип сдвигал сплайсинг REST в сторону полноразмерной формы и прочь от REST4, тем самым сдерживая синаптические гены. Поразительно, что хотя эти вмешательства проводились однократно и их прямые молекулярные эффекты исчезали в течение нескольких недель, мыши жили дольше, лучше ходили по вращающемуся стержню и сохраняли более сильный захват в более позднем возрасте. Их мотонейроны и мышечные волокна были менее атрофированы, а ранние маркёры нейрональной гиперактивности и последующие всплески стресс‑связанных нейропептидов были ослаблены.
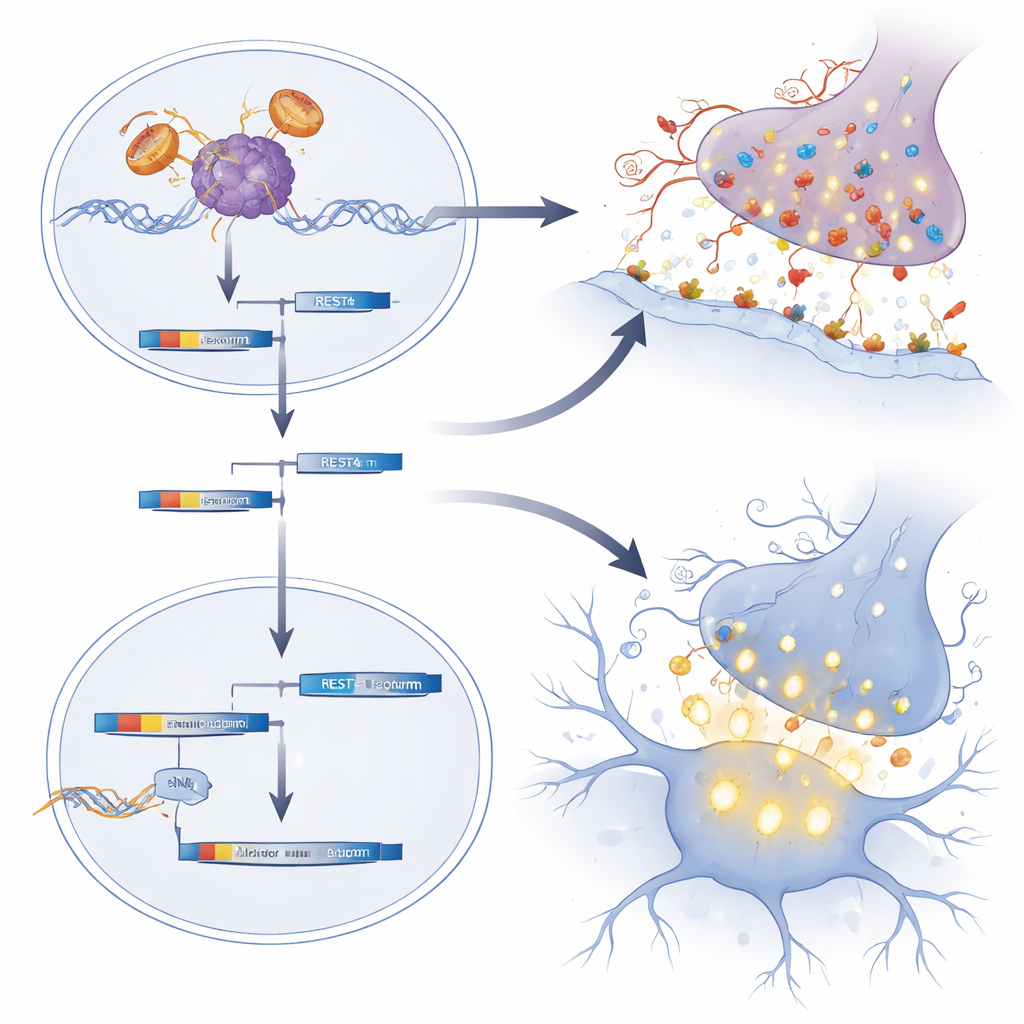
Как ранние гормоны и настройка генов формируют уязвимость
Работа также подчёркивает особую уязвимость мотонейронов к кратковременному выбросу тестостерона, который происходит вскоре после рождения. Когда новорождённым мышам SBMA давали дополнительный тестостерон, их последующая слабость и потеря веса ухудшались, а генетические программы, связанные со здоровым созреванием мотонейронов, ещё сильнее нарушались. У нормальных мышей таких повреждений не наблюдалось, что подчёркивает: вред вызывает сочетание мутантного рецептора и гормонального всплеска. В совокупности результаты указывают на то, что при SBMA избыток возбуждающих синапсов и чрезмерно возбудимые мотонейроны в ранней жизни постепенно тянут систему к сбою, хотя явные симптомы появляются только в среднем возрасте.
Что это значит для людей, живущих с SBMA
Для неспециалиста главный вывод таков: SBMA может быть отчасти заболеванием неправильно временно настроенных и неправильно соединённых синапсов в первые дни после рождения. Неисправный гормональный датчик подталкивает развивающиеся мотонейроны в состояние гиперактивности, и этот ранний стресс в конечном счёте способствует их дегенерации через годы. Обнадеживающий момент заключается в том, что точно спроектированные генетические лекарства, доставленные в эти критические окна, могут восстановить баланс сигналов в мотонейронах, успокоить их чрезмерную активность и заметно отсрочить или уменьшить последующую потерю нервных клеток у животных. Перенос таких вмешательств в раннем возрасте на людей потребует большой осторожности и дальнейших исследований, но эти результаты указывают на новые стратегии, нацеленные на корни SBMA задолго до появления слабости.
Цитирование: Hirunagi, T., Sahashi, K., Iida, M. et al. Restoring early postnatal synaptic dysregulation rescues motor neuron degeneration in a mouse model of Spinal and Bulbar Muscular Atrophy. Nat Commun 17, 2412 (2026). https://doi.org/10.1038/s41467-026-70244-2
Ключевые слова: спинальная и бульбарная мышечная атрофия, гипервозбудимость мотонейронов, андрогенный рецептор, REST регуляция синапсов, терапия антисмысловыми олигонуклеотидами