Clear Sky Science · ru
Выбор пути между реакциями «клик» и переносом ацильной группы, управляемый аминоацилфосфатами
Почему время имеет значение в повседневной химии
Внутри каждой клетки важные молекулы синтезируются и модифицируются в очень точной последовательности, подобно шагам рецепта. Это расписание определяет, включается ли белок, выключается или даже меняет форму. Химики хотели бы имитировать такое встроенное расписание с помощью простых, неживых молекул в воде, не полагаясь на ферменты или внешние триггеры вроде света или резких изменений pH. В этой работе описана искусственная реакционная система, которая делает именно это: она использует структуру коротких пептидов и распространённую реакцию образования связи из «клик‑химии», чтобы определить, какой химический шаг произойдёт первым, а какой должен подождать своей очереди.
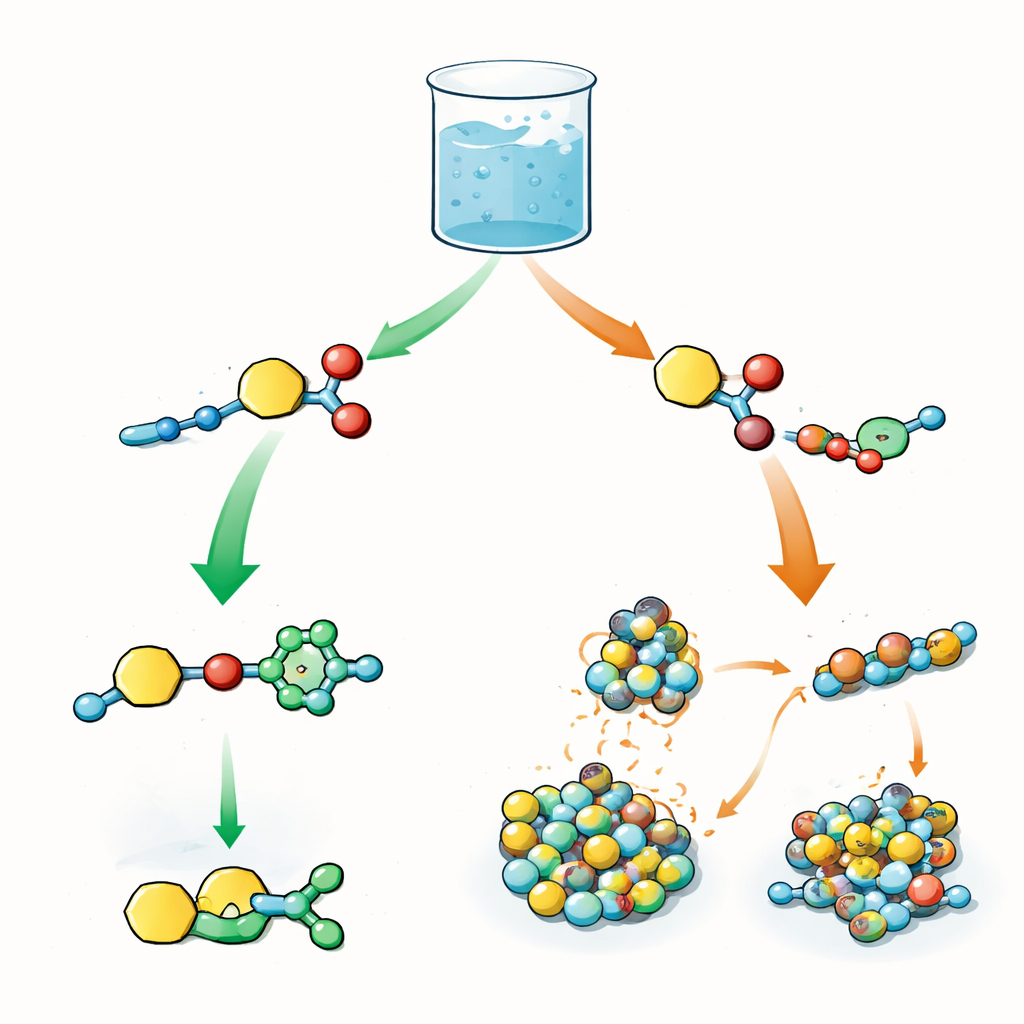
Две конкурирующие реакции в одном сосуде
Авторы спроектировали центральный строительный блок, несущий две реакционноспособные функции: одну, способную передавать «ацильную» группу (малый фрагмент, часто использующийся для модификации белков), и другую, способную участвовать в клик‑реакции — медь‑катализируемом присоединении азида к алкину (CuAAC). В одном и том же сосуде этот строительный блок смешивают с азидами и короткими пептидами, выступающими нуклеофилами, то есть захватывающими ацильную группу. В биологии порядок таких шагов — активация, перенос и последующие модификации — контролирует поведение белков. Здесь вопрос похож: когда обе реакции возможны одновременно, система выбирает сначала клик‑реакцию, сначала перенос ациля или получается смесь обоих путей?
Медленный кислород, быстрый сера
Команда сначала изучает пептиды, содержащие тирозин — аминокислоту с кислородсодержащей боковой цепью. При слабощелочных условиях клик‑реакция идёт быстрее: алкин и азид быстро соединяются, в то время как перенос ациля на боковую цепь тирозина замедлен и мало проявляет накопления определяемых промежуточных продуктов. Существует несколько продуктов, возникших из клик‑пути, и заметного временного разделения между этапами почти нет. Когда исследователи переходят к цистеину, аминокислоте с серосодержащей боковой цепью, картина меняется на противоположную. Цистеин быстро формирует тиоэстеры — серосвязанные ацильные продукты — которые образуются в высоком выходе задолго до появления каких‑либо клик‑продуктов. Только через многие часы начинают появляться продукты клик‑реакции. Такое изменение происходит потому, что сера не только более реакционноспособна, но и связывается с ионами меди, «захватывая» катализатор и временно приостанавливая путь клик‑реакции.
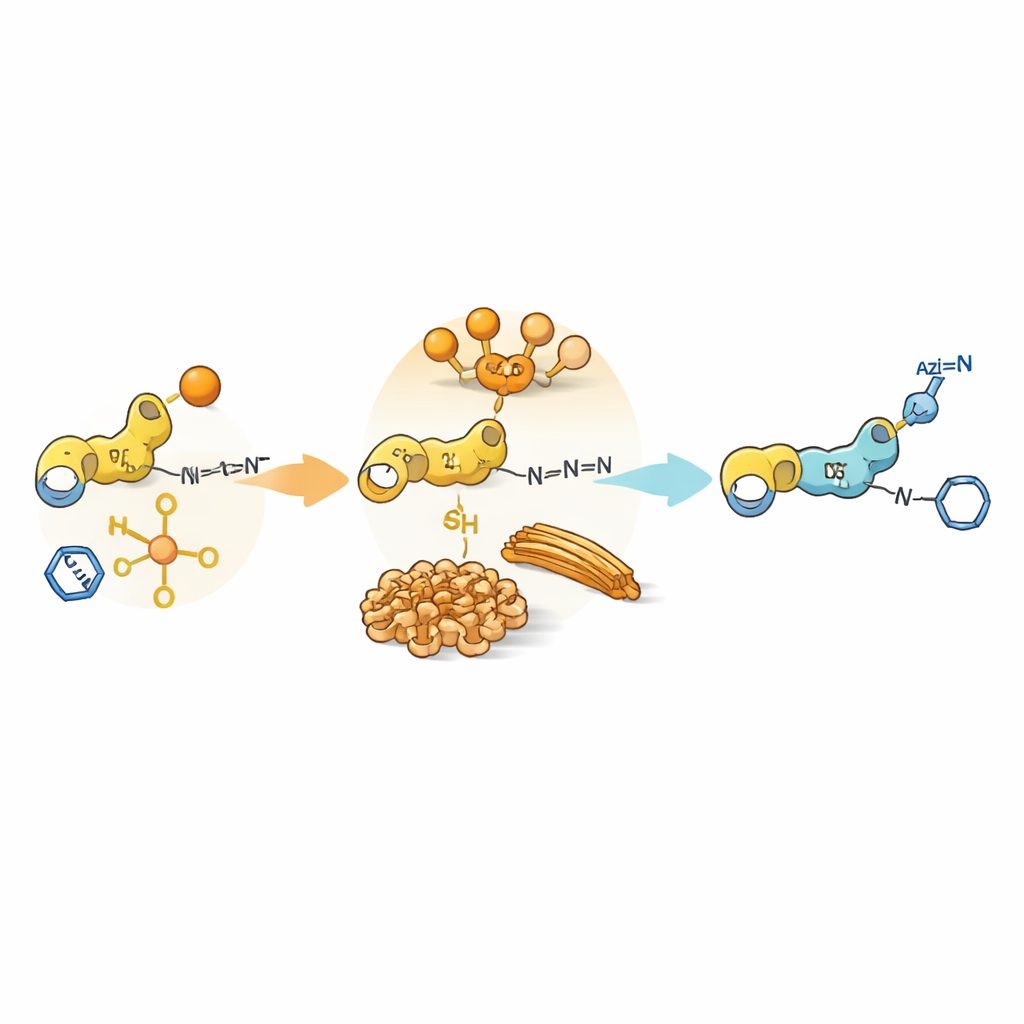
Самосборка как химический затвор
Помимо простой реакционной способности, сами пептиды могут слипаться в более крупные структуры, образуя в воде мягкие гели или волокна. Эти сборки создают микродомены, где одни компоненты сконцентрированы, а другие исключены. Для некоторых ди‑пептидов с тирозином или цистеином и дополнительными ароматическими группами промежуточные продукты самособираются в фибриллы или плотные частицы. Внутри этих упакованных областей перенос ациля оказывается благоприятным, потому что нуклеофил и донор ациля находятся рядом, в то время как азид и медный катализатор преимущественно остаются в окружающем растворе. В результате, хотя клик‑реакция по природе быстра в свободном растворе, её замедляет необходимость проникнуть в захваченные реакционные участки. Это «несовпадение фаз» между местом нахождения катализатора и расположением субстратов удлиняет жизнь ацилированных промежуточных продуктов и откладывает начало клик‑химии.
Программирование каскадов и выбора
Чтобы проверить, насколько далеко можно продвинуть такое встроенное расписание, авторы создают более сложные ситуации. В одном случае один пептид содержит и цистеин, и тирозин, предлагая два различных сайта для переноса ациля. Реакция идёт как трёхступенчатый каскад: сначала на цистеине формируется тиоэстер, затем вторая ацильная группа перемещается на тирозин, и только после этих шагов появляются продукты клик‑реакции. В другом наборе экспериментов два различных азида — один гибкий и алифатический, другой жёсткий и ароматический — конкурируют за один и тот же реактивный центр. Удивительно, но система устойчиво отдаёт предпочтение алифатическому азиду, показывая, что даже форма и электронные свойства азида могут смещать доминирующие продукты, в то время как временная последовательность переносов ациля остаётся под контролем пептидов.
Что это означает для будущих «умных» материалов
Проще говоря, эта работа демонстрирует, как можно упаковать несколько потенциально конкурирующих реакций в одну простую водную смесь и всё же заставить их идти в заданном порядке — без ферментов, насосов или внешних переключателей. Выбирая, несёт ли пептид кислород или серу, регулируя его склонность к самосборке и меняя природу азид‑партнёра, авторы кодируют своего рода внутренние часы в небольшую химическую сеть. Ранние, обратимые перенесения ациля создают кратковременные промежуточные продукты, которые определяют, когда и как произойдёт стойкая, почти необратимая клик‑реакция. Такие запрограммированные последовательности могут стать основой для «умных» материалов и синтетических реакционных сетей, которые «принимают решения» о своих путях со временем, подобно тщательно рассчитанной химии в живых клетках.
Цитирование: Bhattacharjee, D., Sharma, A., Dai, K. et al. Pathway selection between click and acyl transfer reactions driven by aminoacyl phosphates. Nat Commun 17, 2407 (2026). https://doi.org/10.1038/s41467-026-70199-4
Ключевые слова: клик‑химия, перенос ацильной группы, супрамолекулярная сборка, сети реакций, пептидная химия