Clear Sky Science · ru
Молекулярная карта в DNA-PAINT с помощью модифицированной модели гауссовских смесей
Видеть невидимый мир молекул
Современная биология всё чаще опирается на микроскопы, которые позволяют видеть не только клетки, но и отдельные молекулы внутри них. Тем не менее преобразовать слабый, мерцающий свет от этих молекул в надёжную «карту» их положений оказывается удивительно сложной задачей. В этом исследовании представлен новый вычислительный метод под названием G5M, который делает такие молекулярные карты значительно точнее и детальнее, помогая учёным понять, как белки расположены и сгруппированы в живых клетках с точностью до нескольких миллиардных долей метра.
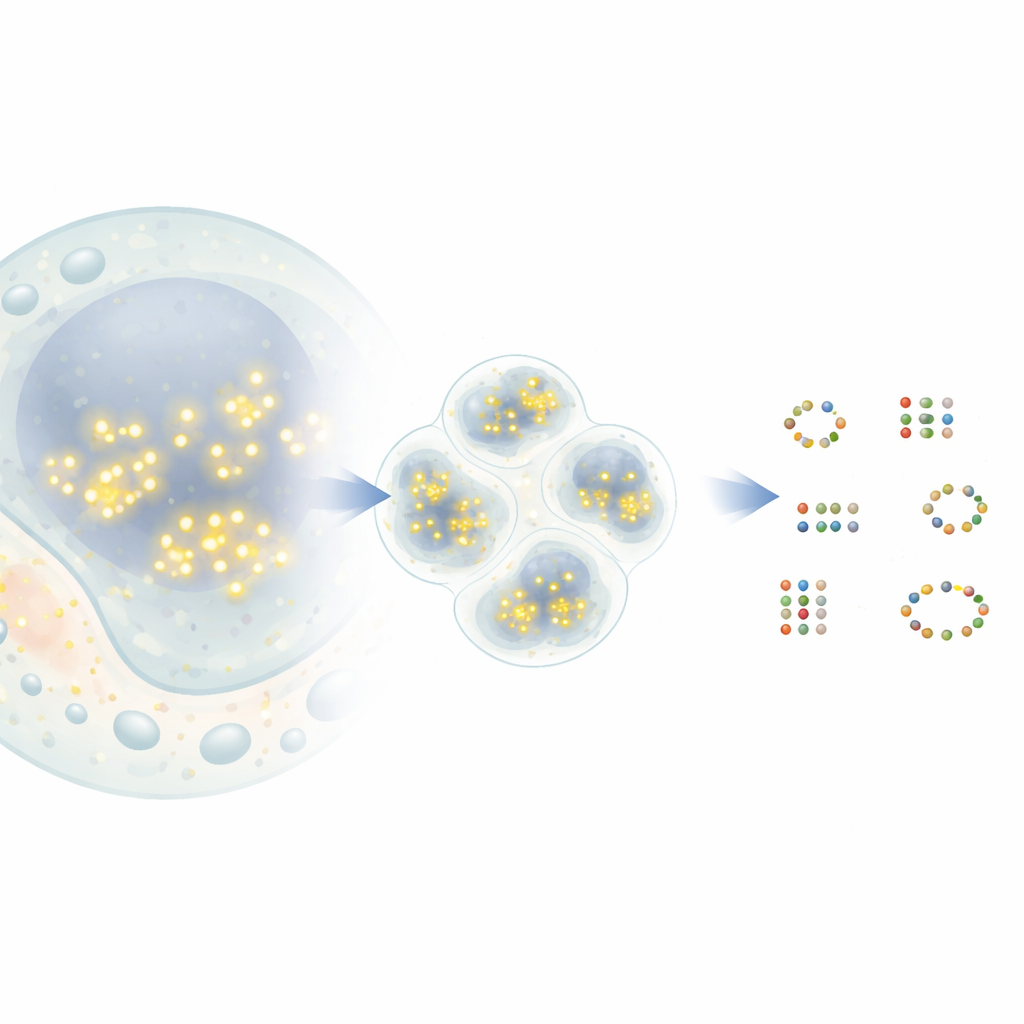
От мигающих точек к молекулярным картам
В популярной технике супер‑разрешения DNA‑PAINT короткие цепочки ДНК с флуоресцентными метками кратковременно связываются и отвязываются с соответствующими ДНК‑метками, прикреплёнными к целевым белкам. Каждый раз, когда метка связывается, она появляется как яркая точка в микроскопе, а затем снова исчезает. Со временем множество таких событий создаёт вокруг каждого белка облако точек. В принципе, центр такого облака указывает на истинную позицию белка с точностью до нанометров. На практике же точки от соседних белков могут перекрываться, а часть точек возникает из фоновых шумов. Существующие инструменты анализа часто сливают близкие соседние точки в один белок или, наоборот, придумывают несуществующие белки, что ограничивает объём извлекаемой биологической информации.
Более умный способ находить реальные молекулы
Новый метод G5M рассматривает скопление точек как смесь простых колоколообразных облаков, каждое из которых соответствует одному реальному молекуле. Вместо простого группирования точек по плотности G5M использует вероятностную модель, которая включает предварительную информацию об эксперименте: насколько точно измеряются положения, как быстро цепочки ДНК связываются и отвязываются, и как микроскоп размывает свет в двух или трёх измерениях. Затем метод проверяет различные возможные объяснения — разное число и форма облаков — и автоматически выбирает то, которое лучше всего балансирует между качеством соответствия и простотой. Дополнительные предохранители отбрасывают сомнительные решения, например облака, которые слишком узкие, слишком широкие, основаны на слишком малом числе точек или недостаточно чётко отделены друг от друга.
Доказательство эффективности в симуляциях и ДНК‑наноструктурах
Для проверки G5M авторы сначала использовали реалистичные компьютерные симуляции простых сцен: пары молекул и небольшие решётки из двенадцати молекул, разнесённых всего на несколько нанометров. По сравнению с ведущим на сегодняшний день методом, известным как Gradient Ascent, G5M находил значительно больше молекул, которые должны быть видимы при теоретическом пределе разрешения, почти не сообщая о несуществующих молекулах. В ключевых случаях он восстанавливал тесно расположенные пары в двадцать семь раз чаще, чем старый метод, и улучшал эффективное разрешение более чем наполовину. Команда затем подтвердила эти достижения экспериментально, используя структуры ДНК‑оригами — искусственные ДНК‑формы с докинговыми сайтами, размещёнными в точно известных позициях — показав, что G5M надёжно считает и локализует почти все ожидаемые сайты в широком диапазоне условий съёмки.
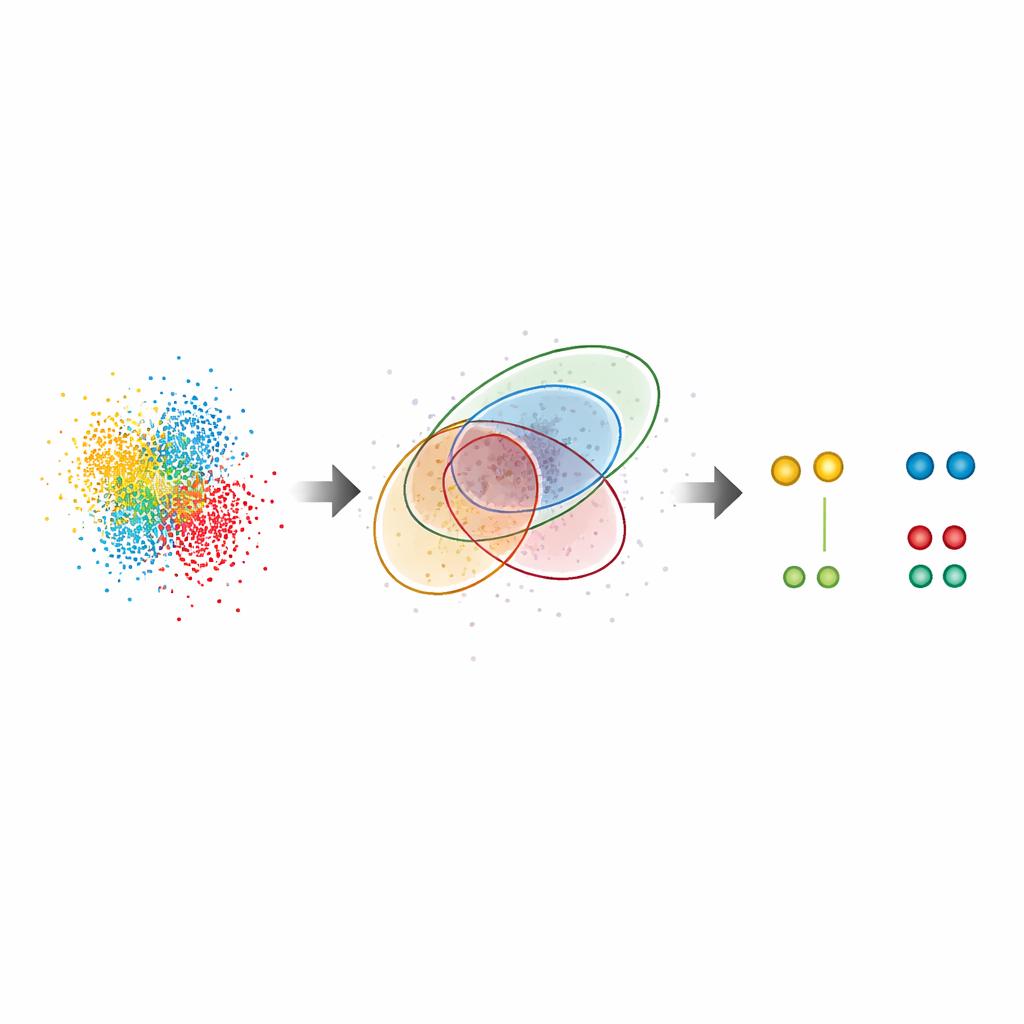
Выявление скрытых закономерностей в настоящих клетках
Помимо тестовых образцов, G5M был применён к сложным биологическим системам. В ядерных поровых комплексах — гигантских воротах в ядре клетки — метод восстановил известное кольцевое расположение ключевого белка Nup96, даже там, где партнёры были разнесены всего на ~10 нанометров. Он обнаружил почти вдвое больше пар белков по сравнению со стандартным методом и воспроизвёл независимые оценки эффективности мечения, что указывает на то, что он не пропускает многие молекулы и не добавляет ложных. Авторы также изучали CD20, поверхностный рецептор, вовлечённый в опухолевые заболевания крови и являющийся мишенью терапевтических антител. Здесь G5M выявил существенно больше небольших кластеров (димеров, тримеров и тетрамеров) CD20 на мембране клетки, проясняя, как антитело против рака и связанные лекарственные форматы перестраивают эти рецепторы. Метод даже повысил эффективность ультра‑высокого разрешения подхода RESI, который опирается на разнесение сигналов по нескольким раундам съёмки.
Что это означает для будущей микроскопии
Извлекая более надёжную информацию из существующих данных DNA‑PAINT, G5M показывает, что только программное обеспечение может открыть новые биологические подробности, без изменения микроскопов или красителей. Алгоритм сохраняет крайне низкий уровень ложных сигналов при одновременном разрешении молекул, находящихся практически в контакте — это важно при ответе на вопросы о том, сколько белков входит в комплекс, как они расположены и как лекарство меняет их организацию. Интегрированный в платформу с открытым исходным кодом Picasso и устойчивый к типичным настройкам, G5M готов стать стандартным инструментом для преобразования мигающей флуоресценции в надёжные молекулярные карты, помогая исследователям картировать нанометровую организацию жизни внутри клеток.
Цитирование: Kowalewski, R., Reinhardt, S.C.M., Pachmayr, I. et al. Molecular mapping in DNA-PAINT via modified Gaussian Mixture Modeling. Nat Commun 17, 2315 (2026). https://doi.org/10.1038/s41467-026-70198-5
Ключевые слова: суперразрешающая микроскопия, DNA-PAINT, молекулярное картирование, олигомеризация белков, алгоритмы анализа изображений