Clear Sky Science · ru
Мультиомика на уровне отдельных клеток выявляет механочувствительную ось эндотелия PIEZO1–IL‑33, приводящую к легочному фиброзу
Почему важна жесткость легких
Легочный фиброз — разрушительное заболевание, при котором когда‑то эластичные альвеолы постепенно превращаются в плотную рубцовую ткань, и каждый вдох становится трудным. В настоящее время врачи могут лишь замедлить прогрессирование болезни, но не остановить и не обратить её вспять. В этом исследовании задают внешне простой, но важный вопрос: как клетки, выстилающие кровеносные сосуды легких, ощущают, что окружающая ткань стала аномально жесткой, и как это ощущение преобразуется в усиление рубцевания? Отслеживая эту цепочку событий до отдельных клеток и конкретных генов, авторы обнаруживают механический «переключатель» в сосудах, который может представлять собой потенциальную мишень для лекарств.
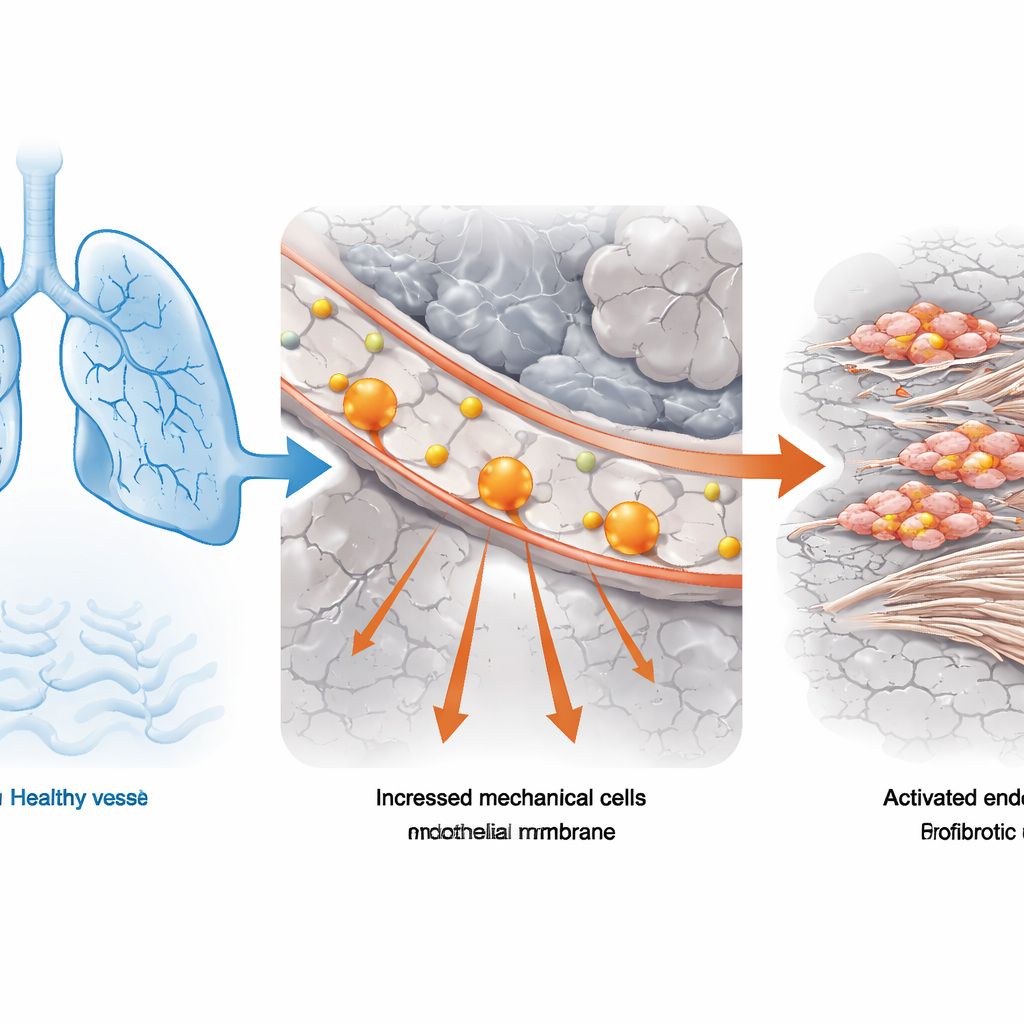
От функциональных тестов легких к отдельным клеткам
Команда начала с образцов легочной ткани пациентов с идиопатическим легочным фиброзом, самой распространенной формой заболевания, и донорских образцов нормальных легких. Они объединили стандартные измерения функции легких (как много воздуха человек может выдохнуть с усилием) с мощным секвенированием РНК отдельных клеток, которое показывает, какие гены активны в тысячах отдельных клеток. С помощью вычислительного инструмента, связывающего суммарные клинические данные с профилями на уровне отдельных клеток, исследователи выявили типы клеток, наиболее тесно связанные с тяжелым нарушением функции легких. Эндотелиальные клетки сосудов — клетки, образующие внутреннюю выстилку кровеносных сосудов — выделялись особенно в образцах пациентов с объемом легких менее половины нормы. В этих эндотелиальных клетках программы генов, связанные с «механическим стрессом», были устойчиво повышены, что указывает на то, что аномальные физические силы являются частью проблемы.
Механический стресс как скрытый фактор
Чтобы проверить, является ли связь между механочувствительностью и болезнью общей, авторы обратились к двум модельным системам легочного рубцевания у мышей: одной, вызванной химиотерапевтическим препаратом блеомицином, и другой — хроническим воздействием кремнеземной пыли, профессиональным риском. Применив методы одиночноклеточной аналитики к этим экспериментальным легким, они вновь обнаружили, что эндотелиальные клетки несут отчетливые сигнатуры повышенного механического стресса. В обеих моделях, по мере утолщения и уплотнения окружающей легочной ткани, выстилка сосудов переходила в малопригодное состояние. Такое совпадение между образцами людей и животными усилило идею о том, что искаженные физические силы в легком, а не только воспаление или иммунная активность, играют центральную роль в развитии и прогрессии фиброза.
Датчик давления с критической ролью
Углубляясь, команда искала конкретные «механосенсоры» — белки, превращающие физическое растяжение в биохимические сигналы, — которые были повышены в стрессированных эндотелиальных клетках. Один ионный канал, называемый PIEZO1, не раз выделялся как основной подозреваемый. У мышей и людей с фиброзом уровень PIEZO1 в эндотелиальных клетках сосудов был заметно выше, чем у здоровых контролей. Когда исследователи создали мышей, у которых PIEZO1 был удален только в эндотелии, эти животные оказались значительно более устойчивыми к блеомицин‑индуцированному рубцеванию легких: у них было меньше накопления коллагена, меньше активированных фиброзообразующих клеток и низкий уровень химического маркера фиброза. Фармакологическое блокирование PIEZO1 с помощью пептидного ингибитора также уменьшало рубцевание, тогда как его активация усугубляла фиброз — если только рецептор присутствовал в эндотелиальных клетках. Вместе эти эксперименты показали, что PIEZO1 в выстилке сосудов — не просто наблюдатель, а необходимый драйвер болезни.
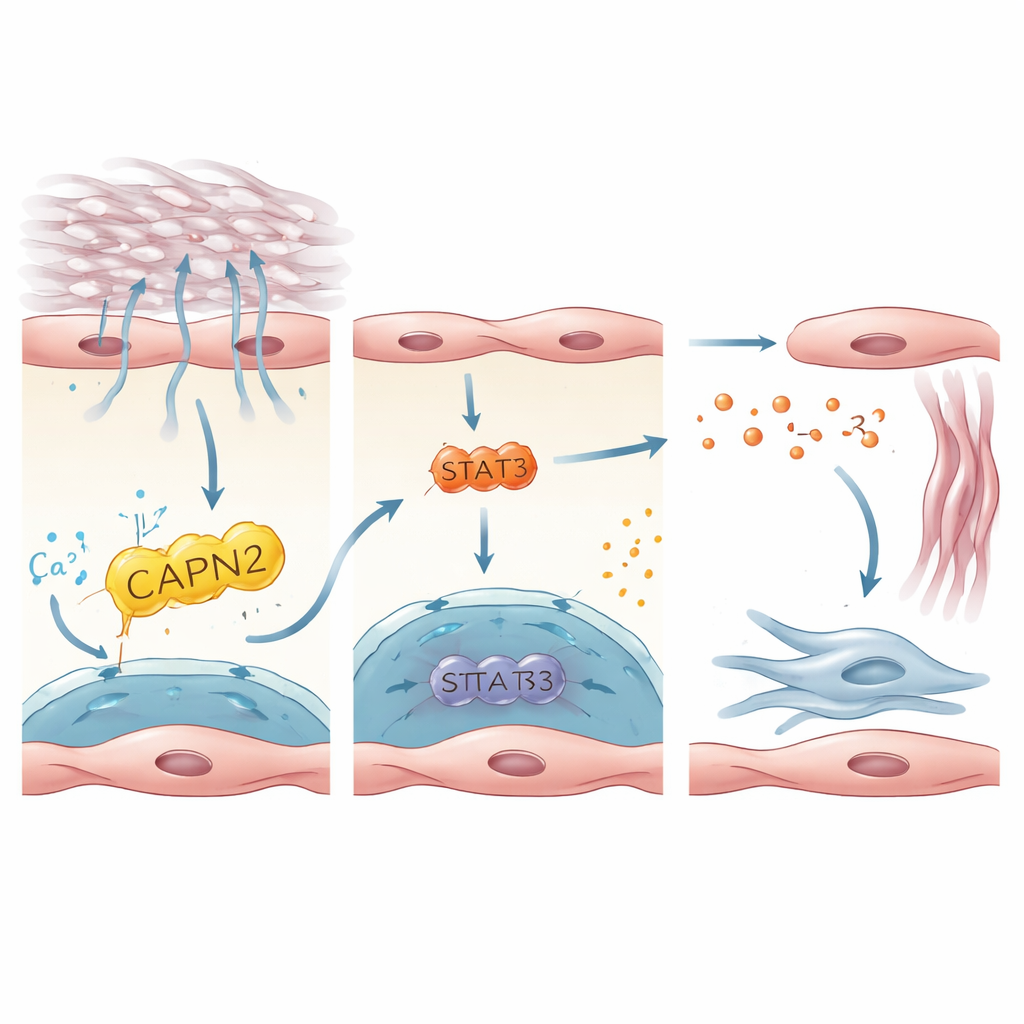
Сигнальная цепочка, пробуждающая фибробласты
Далее исследование проследило, как активация PIEZO1 в эндотелиальных клетках преобразуется в сигналы, которые пробуждают фибробласты — клетки, откладывающие рубцовую ткань. Интегрируя данные человека и мыши, авторы выделили интерлейкин‑33 (IL‑33), небольшой белок, выделяемый стрессированными или поврежденными клетками, как ключевой мессенджер. IL‑33 сильно экспрессировался в PIEZO1‑положительных эндотелиальных клетках и был повышен в легких пациентов и мышей с фиброзом. В культивируемых человеческих эндотелиальных клетках, выращенных на жестких подложках или растянутых, чтобы имитировать дыхание в условиях жесткого легкого, активация PIEZO1 усиливала продукцию IL‑33. Это зависело от фермента низового звена CAPN2 и транскрипционного фактора STAT3, которые совместно регулировали активность гена IL‑33. У мышей удаление IL‑33 специфически в эндотелии защищало от фиброза, тогда как принудительная сверхэкспрессия IL‑33 в эндотелиальных клетках устраняла защитный эффект потери PIEZO1. Эти результаты описывают линейную ось: механический стресс → PIEZO1 → CAPN2/STAT3 → IL‑33 → активация фибробластов и рубцевание.
Что это значит для будущих терапий
Для неспециалистов важный вывод состоит в том, что легочный фиброз обусловлен не только «бесчинством» иммунных клеток; это также заболевание нарушения «осязания» в кровеносных сосудах. Эндотелиальные клетки чувствуют, что окружающая ткань стала слишком жесткой, включают «переключатель» PIEZO1 и в ответ выделяют IL‑33 — сигнал опасности, который побуждает соседние фибробласты продолжать откладывать рубцовую ткань. Расчленяя эту цепочку от механической силы до экспрессии генов, работа выделяет несколько перспективных мишеней — сам PIEZO1, каскад CAPN2‑STAT3 и IL‑33 — для терапий, нацеленных на разрыв самоподдерживающегося цикла жесткости и рубцевания. Хотя необходимы дополнительные исследования для безопасной модуляции этих путей у людей, эта механочувствительная эндотелиальная ось предлагает новый, физически обоснованный подход к лечению заболевания, которое долгое время противостояло эффективной терапии.
Цитирование: Zhang, L., Gui, X., Hou, R. et al. Single-cell multiomics uncovers an endothelial mechanosensitive PIEZO1-IL-33 axis driving pulmonary fibrosis. Nat Commun 17, 2655 (2026). https://doi.org/10.1038/s41467-026-70193-w
Ключевые слова: легочный фиброз, эндотелиальные клетки, механотрансдукция, PIEZO1, IL‑33