Clear Sky Science · ru
Сборка ковалентного «заряда» в биосинтезе фострицина включает малонилирование-лактонобразование бифункциональной тиоэстеразой и ферментативную демалонилизацию
Как природа собирает крошечный химический «заряд»
Противораковые препараты и антибиотики часто зависят от нескольких правильно расположенных атомов — крошечного «заряда», который захватывает белок и отключает его. Природное соединение фострицин — именно такой молекула, обладающая мощной активностью против ферментов, участвующих в росте клеток. Но её сложная структура затрудняет производство и модификацию в лаборатории. В этом исследовании по шагам раскрывается, как бактерии собирают ключевой заряд фострицина, показывая ферментативные приёмы, которые химики теперь могут заимствовать для разработки новых лекарств.
Особый «крючок» в мощных природных лекарствах
Многие перспективные лекарства из почвенных бактерий принадлежат к семейству поликетидов. В этой группе есть подсемейство, несущие реактивное кольцо, известное химикам как α,β-ненасыщенный δ-лактон, которое действует как молекулярный крючок. Оно может образовывать ковалентную связь с определёнными аминокислотами в белках, выключая ключевые биологические переключатели. В фострицине и родственных молекулах этот «крючок» сочетается с фосфатной группой, которая помогает им нацеливаться на специфические ферменты, контролирующие деление клеток. Эти свойства делают их привлекательными кандидатами против рака, но та же реактивность и структурная сложность затрудняют их синтез и делают нестабильными при хранении.
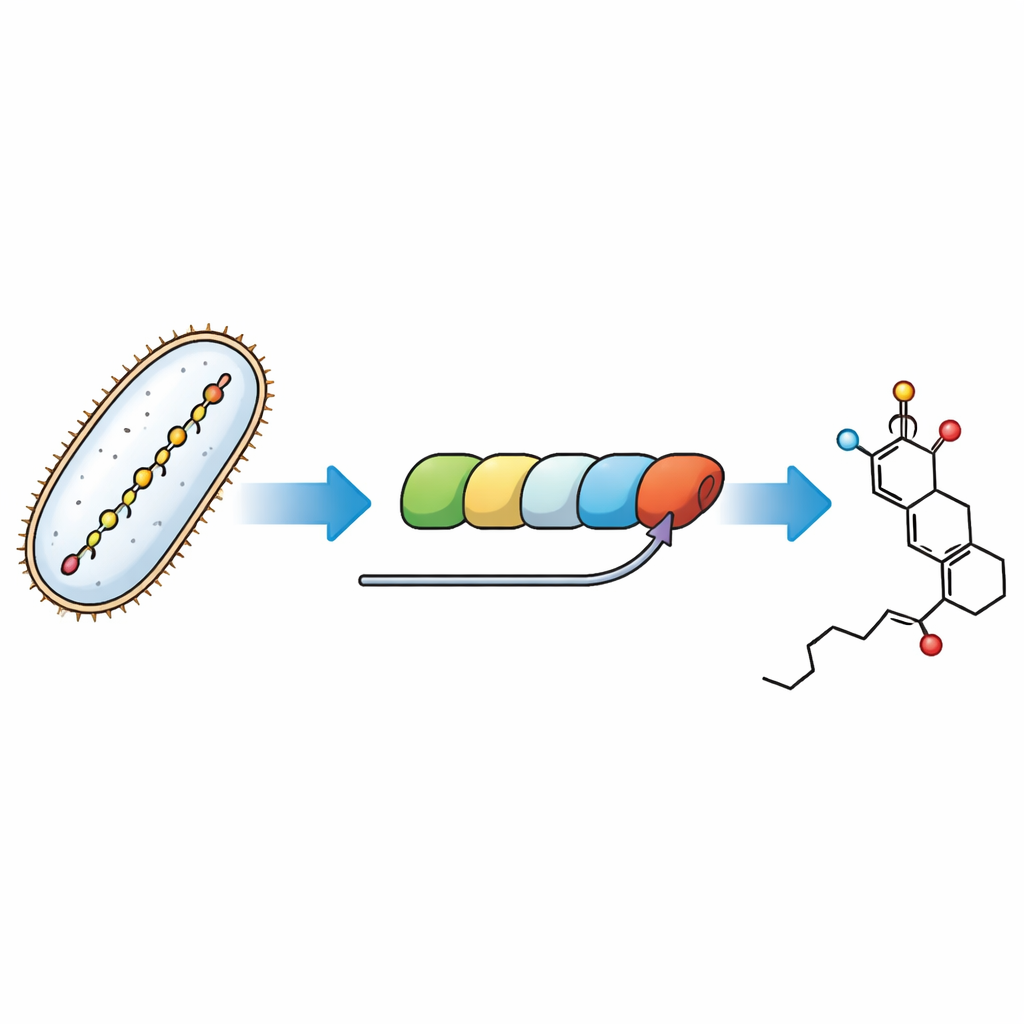
Отслеживание финальных шагов молекулярной конвейерной линии
Бактерии собирают фострицин с помощью массивного модульного белкового комплекса, называемого поликетидсинтазой — конвейера, где каждая станция удлиняет и формирует растущую углеродную цепочку. Загадка, рассмотренная здесь, — как последний модуль этого конвейера формирует кольцо «заряда» и устанавливает временную «ручку», называемую малонильной группой, которую затем нужно удалить. Воссоздавая путь в пробирках с очищенными ферментами и специально разработанными малыми молекулами-заместителями природных интермедиатов, исследователи могли наблюдать отдельные шаги и отнести их к конкретным частям конвейера.
Многофункциональный фермент с неожиданным талантом
Команда обнаружила, что последняя станция конвейера — домен, названный FosTE — ведёт себя иначе, чем ожидалось. Типичные версии такого домена просто отрезают готовые продукты от конвейера. FosTE, напротив, сначала захватывает малонильный фрагмент из обычного клеточного строевого блока и переносит его на определённый атом кислорода в растущей цепочке, а затем способствует тому, чтобы цепочка свернулась и замкнулась в кольцо «заряда». Мутация единственного реактивного остатка серина в FosTE блокирует обе активности. Моделирование структуры указывает на две положительно заряженные аргининовые остатки в активном центре, которые удерживают малонильный фрагмент и позиционируют его для переноса — функции, обычно выполняемые другим классом ферментов. Замена этих аргининов на нейтральные остатки стирает стадию переноса малонила, оставляя при этом в основном неизменным образование кольца, что подтверждает их критическую роль.
Фиксация «заряда» и предотвращение потерь
После того как кольцо сформировано и несёт временную малонильную группу, другой фермент, FosM, должен удалить эту группу, чтобы обнажить полностью вооружённый «заряд». Исследование показывает, что FosM работает эффективно только после того, как ещё один фермент — широкоспецифичная киназа FosH — добавляет фосфат в соседнюю позицию молекулы. Когда исследователи подавали малонилированное кольцо только на FosM, происходила лишь умеренная конверсия. Предварительное добавление FosH приводило к почти полному удалению малонильной группы и образованию конечного реакционного фрагмента. Важно, что FosH также может фосфорилировать родственные «обходные» интермедиаты, возникающие в побочных реакциях, спасая их и позволяя корректно перерабатываться вместо превращения в тупиковые побочные продукты.
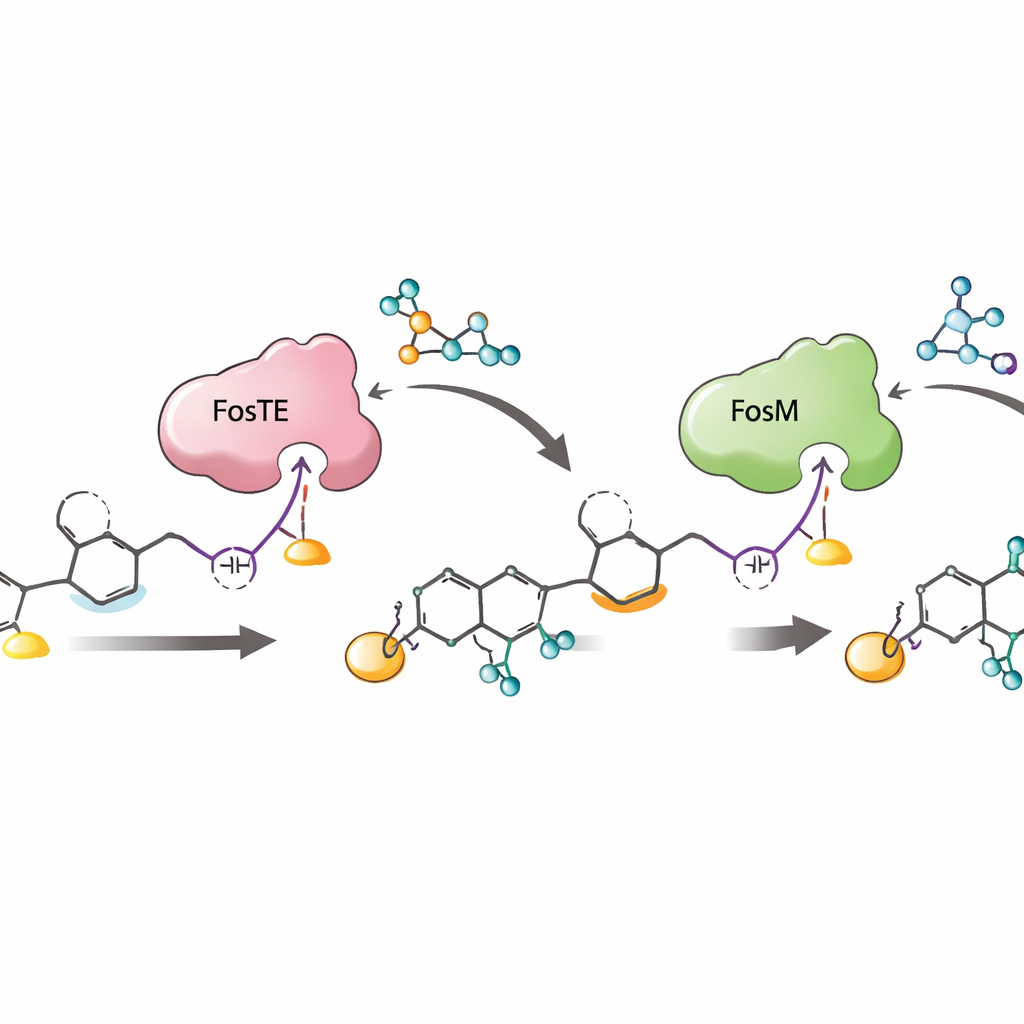
Почему эта ферментативная хореография важна
В совокупности работа раскрывает слаженную последовательность: удлинение цепи на конвейере, малонильное присоединение и замыкание кольца под управлением FosTE, фосфорилирование FosH и, наконец, демалонилизация FosM. Такой порядок не только эффективно конструирует чувствительный «заряд», но и защищает нестабильные интермедиаты от распада и максимизирует образование желаемой фосфорилированной формы, наиболее активной как предшественник лекарства. Показывая, как один домен фермента может одновременно декорировать и высвобождать растущую молекулу — и как партнёрные ферменты тонко настраивают и спасают реакционноспособные интермедиаты — исследование предлагает схему для проектирования новых поликетидов с «зарядами» и для построения более коротких, эффективных синтетических маршрутов к сложным противораковым агентам, таким как фострицин.
Цитирование: Nguyen, L.N.K.T., Schlotte, L., Hoffmann, J. et al. Covalent warhead assembly in fostriecin biosynthesis involves malonylation-lactonisation by a bifunctional thioesterase and enzymatic demalonylation. Nat Commun 17, 2365 (2026). https://doi.org/10.1038/s41467-026-70144-5
Ключевые слова: фострицин, биосинтез поликетидов, инжиниринг ферментов, активные группы природных продуктов, хемоэнзимный синтез