Clear Sky Science · ru
Сигнальная система эндотелийного C‑типа натрийуретического пептида/гуанилатциклазы‑B предотвращает легочную артериальную гипертензию
Почему это важно для легких и сердца
Легочная артериальная гипертензия — редкое, но смертельно опасное состояние, при котором сосуды, переносящие кровь от сердца к легким, становятся чрезмерно узкими и утолщенными. Такая нагрузка может привести к правосторонней сердечной недостаточности и, в конечном итоге, к смерти. Существующие препараты в основном расширяют эти сосуды, но мало влияют на первичное повреждение сосудистой стенки. Исследование, лежащее в основе этой статьи, раскрывает естественный защитный сигнал, вырабатываемый клетками, выстилающими легочные сосуды, и показывает, как усиление этого сигнала может как предотвращать, так и лечить заболевание.
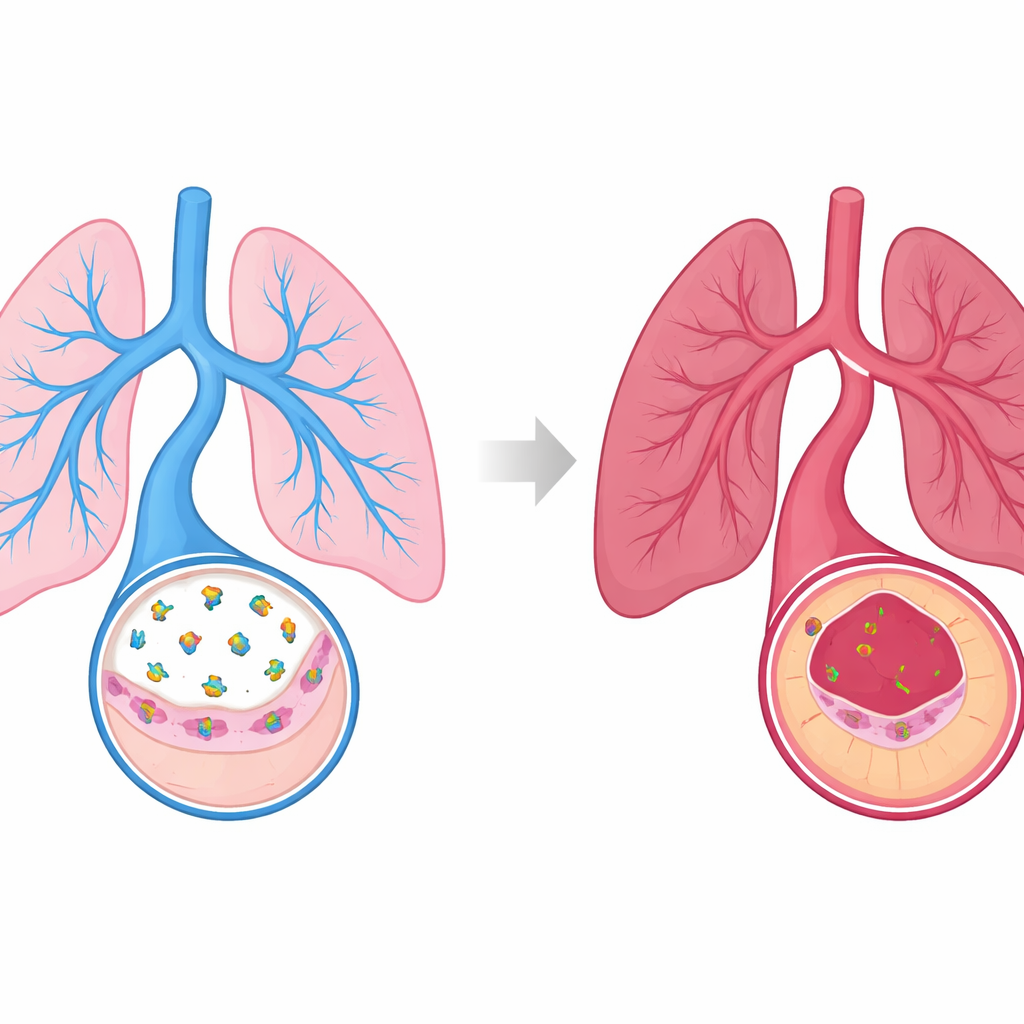
Защитное послание от выстилки сосудов
Внутренняя выстилка сосудов состоит из эндотелиальных клеток, которые постоянно общаются с окружающим мышечным слоем, чтобы поддерживать просвет и здоровье сосудов. Авторы сосредоточились на небольшом гормоне — натрийуретическом пептиде типа C (CNP), который эти эндотелиальные клетки выделяют в легких. CNP действует локально через рецепторную белковую гуанилатциклазу‑B на тех же клетках, вызывая образование химического посредника, который помогает сосудам расслабляться и сопротивляться повреждению. При исследовании мышей, подвергнутых двум разным триггерам легочной гипертензии — токсическому химическому агенту и среде с пониженным содержанием кислорода — учёные обнаружили, что в легких, развивающих заболевание, уровни и CNP, и его рецептора были значительно ниже, чем в здоровых легких.
Отключение сигнала усугубляет заболевание у животных
Чтобы проверить, действительно ли потеря CNP‑сигнализации приводит к болезни, команда создала мышей, у которых либо сам CNP, либо его рецептор GC‑B были удалены только в эндотелиальных клетках. При воздействии тех же триггеров у этих мышей артерии легких сужались сильнее, давление в правой части сердца повышалось выше, а сердечная мышца утолщалась больше, чем у нормальных мышей. Напротив, удаление рецептора только из окружающих гладкомышечных клеток не ухудшало болезнь. Это указывает на ключевую роль CNP, действующего именно на эндотелиальные клетки, а не напрямую на мышечный слой.
Как сигнал успокаивает стенку сосуда
При более тщательном рассмотрении исследователи обнаружили, что путь CNP–GC‑B в эндотелиальных клетках действует как тормоз для нескольких вредных реакций. При его отсутствии эти клетки вырабатывали больше эндотелина‑1 — мощного молекулы, сужающей сосуды, — и повышали уровни провоспалительных посредников, таких как интерлейкин‑6, CCL2 и TGF‑β1. В экспериментах на культурах клеток восстановление CNP подавляло эти сигналы, но только при наличии рецептора GC‑B. CNP также помогал восстановить баланс между двумя конкурирующими системами контроля роста внутри клеток, известными как SMAD2/3 и SMAD1/5/9, которые совместно определяют, останется ли сосудистая стенка стабильной или утолщается. При сохраненной CNP‑сигнализации гены, связанные со здоровыми, неразросшимися артериями, оставались активными; при её отсутствии баланс смещался в сторону избыточного роста и рубцевания.
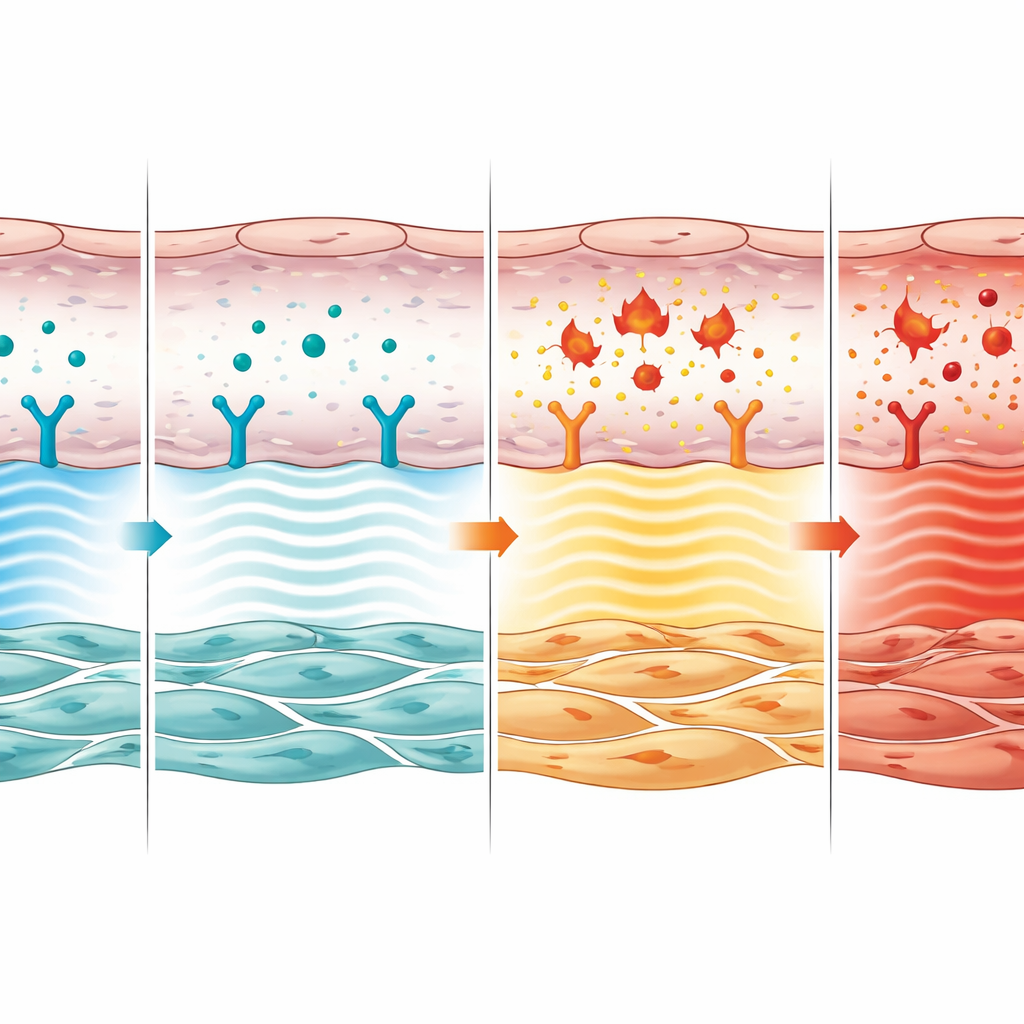
От клеточного диалога к ремоделированию сосуда
Далее команда изучила, как этот эндотелиальный сигнал влияет на соседние гладкомышечные клетки, которые фактически утолщают сосудистую стенку. Они показали, что химические сигналы, выделяемые здоровыми эндотелиальными клетками, реагирующими на CNP, замедляли рост и миграцию гладкомышечных клеток в лабораторных условиях. Когда рецептор CNP был удален из эндотелиальных клеток, эти сигналы, напротив, стимулировали размножение и перемещение гладкомышечных клеток, повторяя ремоделирование стенки сосуда, наблюдаемое при болезни. В легких мышей артерии, лишенные эндотелиальной CNP‑сигнализации, содержали больше делящихся гладкомышечных клеток и меньше погибающих, что подтверждает, что этот путь обычно сдерживает избыточный рост, перекрывающий кровоток.
Испытание лекареподобного CNP в тяжёлых моделях
Воодушевлённые этими результатами, авторы протестировали более долговечную форму CNP, называемую CNP‑53, которую непрерывно доставляли с помощью крошечных насосов грызунам. У мышей введение CNP‑53 во время воздействия триггеров болезни предотвращало повышение давления в легких и утолщение стенки артерий — но только если в эндотелиальных клетках сохранялся рецептор GC‑B. У крыс и мышей с особенно тяжелой, похожей на человеческую формой легочной гипертензии, начало лечения CNP‑53 после установления болезни снижало легочные давления и улучшало показатели работы сердца. В сочетании с двумя существующими препаратами — одним, блокирующим эндотелин, и другим, влияющим на связанный путь роста — CNP‑53 давал дополнительную пользу, не снижая при этом нормальное артериальное давление.
Что это означает для будущих методов лечения
В сумме исследование показывает, что естественный гормон, вырабатываемый выстилкой легочных сосудов, действует как страж против легочной артериальной гипертензии. Когда сигнал CNP–GC‑B снижен, воспаление, сосудосуживающие молекулы и пути роста выходят из-под контроля, утолщая стенку артерии и перегружая сердце. Восстановление или усиление этого сигнала с помощью препаратов на основе CNP, особенно вариантов, разработанных для более длительного нахождения в организме, может открыть новый путь лечения, направленный на сам патологический процесс, а не только на расширение сосудов. Хотя для перевода этих результатов в клинические терапии для людей требуется дополнительная работа, результаты говорят о том, что помощь выстилке сосудов в правильной «коммуникации» может оказаться ключевой для защиты пациентов с этим разрушительным заболеванием легких и сердца.
Цитирование: Yanagisawa, H., Kuwahara, K., Nakagawa, Y. et al. Endothelial C-type natriuretic peptide/guanylyl cyclase-B signaling prevents pulmonary arterial hypertension. Nat Commun 17, 2331 (2026). https://doi.org/10.1038/s41467-026-70139-2
Ключевые слова: легочная артериальная гипертензия, эндотелиальная сигнальная передача, натрийуретический пептид типа C, ремоделирование сосудов, кровообращение в легких