Clear Sky Science · ru
Трансляционная регуляция через окислительную десульфурацию модификаций тРНК
Как клетки настраивают производство белков в условиях стресса
Каждая клетка должна решить, какие белки синтезировать, с какой скоростью и когда замедлиться. В этом исследовании выявлен деликатный химический переключатель на молекулах транспортной РНК (тРНК), который помогает клеткам снижать производство белков, когда среда становится более окислительной — например, при воспалении или метаболическом стрессе. Наблюдая поведение этого переключателя в клетках млекопитающих и в пробирочных системах, исследователи раскрывают новый механизм, при котором изменения, похожие на повреждения РНК, могут служить регуляторным сигналом.
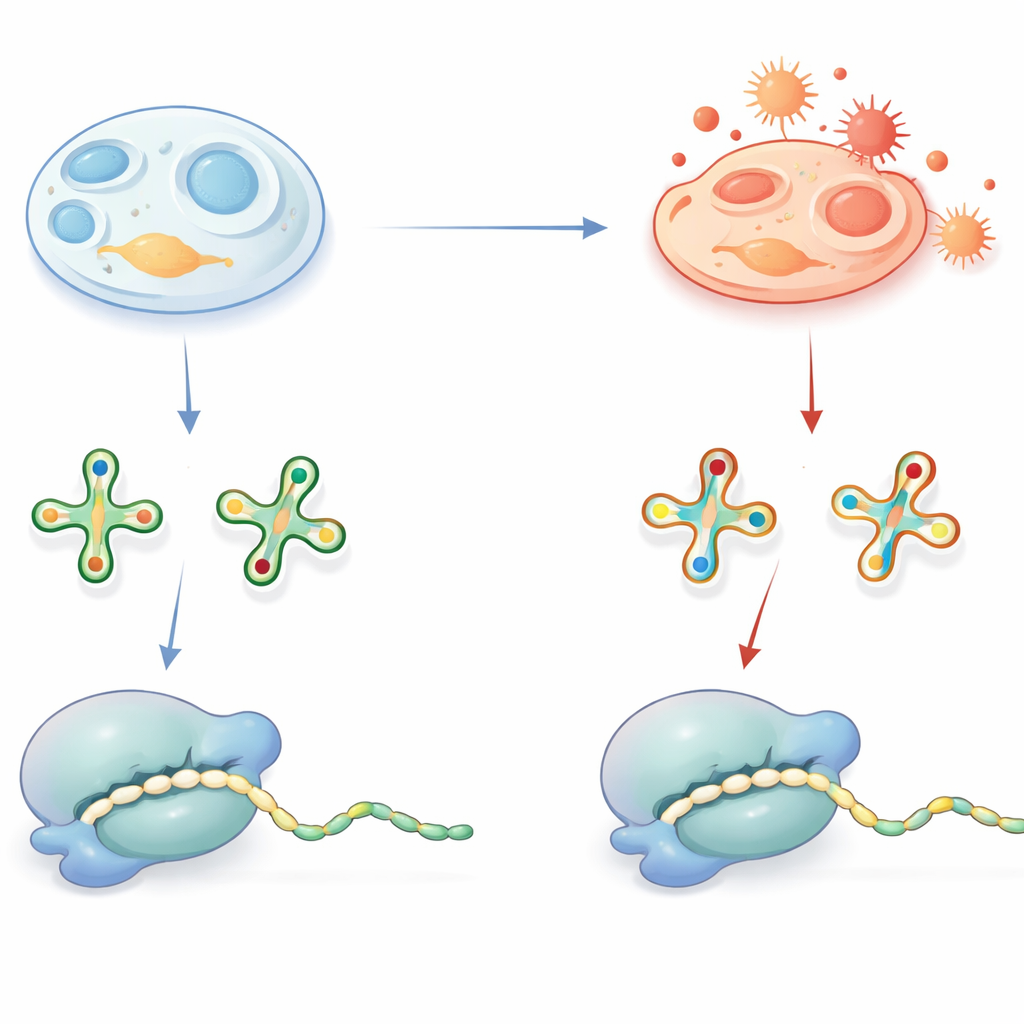
Маленькие метки на тРНК с большими последствиями
тРНК выступают адаптерами, которые считывают трехбуквенные «слова» в матричной РНК и доставляют соответствующие аминокислоты во время синтеза белка. Для точной и эффективной работы многие тРНК несут особые химические украшения, особенно в ключевой позиции, контактирующей с третьей буквой кодона. Одна широко распространённая модификация — группа, содержащая серу, на уридиновом нуклеозиде, часто обозначаемая как производное 2-тиоуридина. При нормальных условиях эта сера помогает тРНК распознавать правильные кодоны, оканчивающиеся на A или G, и поддерживает быструю и безошибочную трансляцию. Дефекты таких украшений уже известны как причина человеческих заболеваний, что подчёркивает их значимость.
Когда окислительный стресс переписывает тРНК
Сера, которая улучшает декодирование, имеет и уязвимость: она химически подвержена окислению. Авторы поставили вопрос, удаляется ли эта группа внутри клеток в окислительных условиях и что это означает для синтеза белка. С помощью чувствительной масс-спектрометрии они обнаружили окисленные, лишённые серы варианты этих тРНК-оснований — так называемые производные h2U — в тканях мышей, митохондриях свиней, бактериях, дрожжах и ряде линий человеческих клеток. Хитрый эксперимент со вводимым бактериальным маркером тРНК показал, что метки h2U не являются артефактами, возникшими при подготовке образца, а формируются в живых клетках. Хотя окисленные версии присутствовали лишь в доле тРНК, их содержание варьировало между тканями и типами клеток, что свидетельствует о влиянии редокс-состояния клетки и антиоксидантного потенциала на частоту этой конверсии.
Как окисленные тРНК замедляют конвейер
Далее исследователи проверили, как эти изменённые тРНК работают во время синтеза белка. Они химически превратили серосодержащую форму в окисленную h2U в совокупной массе тРНК и использовали полностью воссозданную человеческую систему трансляции in vitro. Референтный белок, чье производство сильно зависит от этих модифицированных тРНК, показал резкое снижение выхода при десульфурации тРНК, тогда как контрольный репортер, избегающий затронутых кодонов, переводился нормально. Биохимические анализы объяснили почему: окисленные тРНК для лизина, глутамина и глутамата заряжались своими аминокислотами значительно хуже, тогда как соответствующие тРНК для аргинина в основном оставались невредимыми. Важно, что тРНК, несущие h2U, по‑прежнему обнаруживались в рибосомных (полисомных) фракциях из клеток, что указывает на то, что они участвуют в трансляции, но делают это неэффективно.
Структурный взгляд на ослабленное декодирование
Чтобы увидеть, как именно окисление меняет декодирование, команда использовала высокоразрешающую криогенную электронную микроскопию для съёмки бактериальных рибосом, запрограммированных человеческой тРНК для лизина и конкретными кодонами. В нормальном, серосодержащем состоянии модифицированное основание в «колеблющейся» позиции тРНК формировало либо стандартную пару оснований с кодоном, оканчивающимся на A, либо специальную «вобблирующую» пару с кодоном на G, обе прочно расположенные в декодирующем центре рибосомы. После десульфурации то же основание могло установить только одно слабое взаимодействие с кодоном на A и образовывало менее стабильную wobble‑пару с кодоном на G. Эксперименты по связыванию согласуются с этими структурами: окисленная тРНК для лизина фактически теряла способность распознавать кодон AAA и намного хуже распознавала кодон AAG. В совокупности эти данные показывают, что, казалось бы, небольшая химическая правка может привести к замедлению трансляции, специфичному для отдельных кодонов.
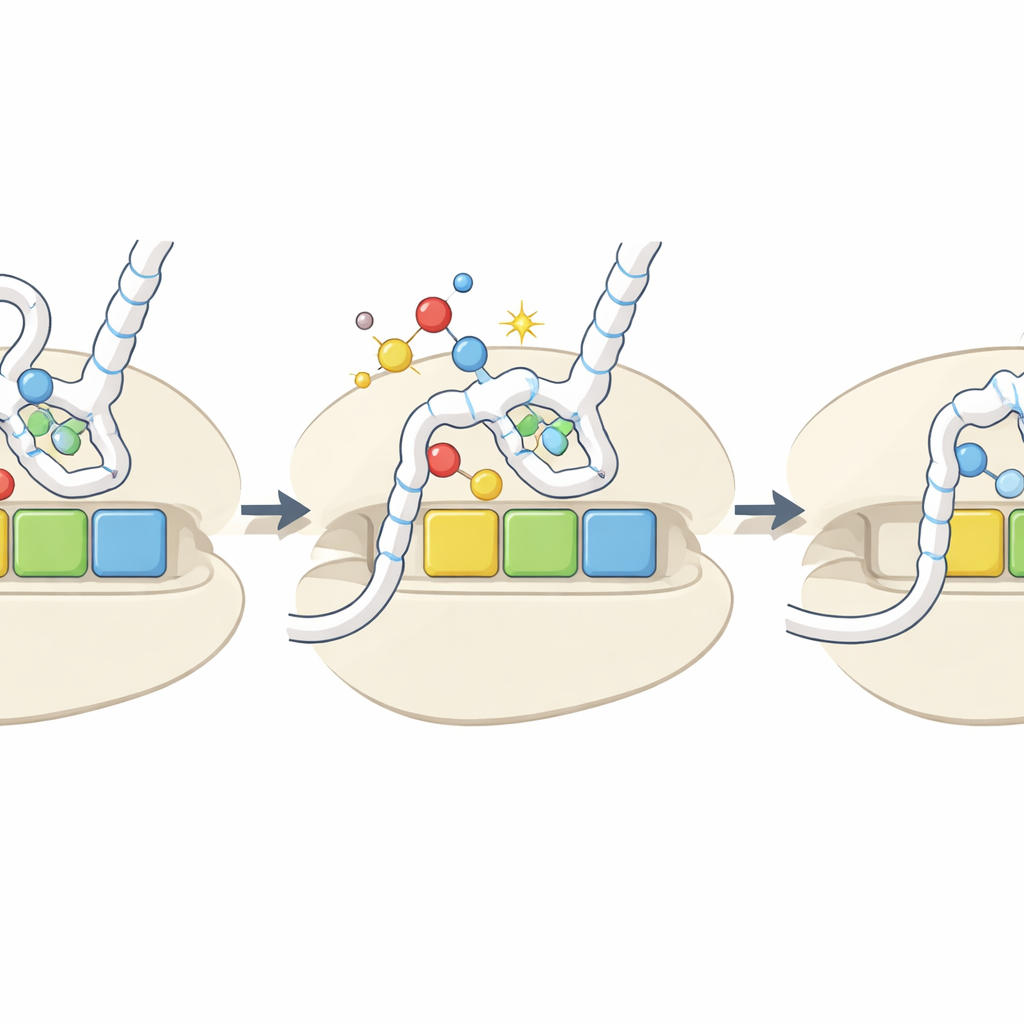
Сигнал повреждения, ставший регуляторной ручкой
В целом исследование предлагает, что окислительное удаление серы из ключевых оснований тРНК действует как встроенный датчик редокс‑среды клетки. При окислительном стрессе больше тРНК конвертируется в форму h2U, которые слабо заряжаются и слабо связываются с определёнными кодонами. Это селективно замедляет трансляцию на этих кодонах, что потенциально изменяет стабильность затронутых мРНК, влияет на свёртывание белков и запускает стресс‑ответные пути при остановке рибосом. Хотя окисленные метки относительно редки и их уровень не всегда резко растёт при экспериментальном стрессе, их кодон- и аминокислотно‑специфические эффекты означают, что даже умеренные изменения могут изменить, какие белки синтезируются и с какой скоростью в сложных условиях.
Цитирование: Mo, Y., Ishiguro, K., Miyauchi, K. et al. Translational regulation by oxidative desulfuration of tRNA modifications. Nat Commun 17, 2125 (2026). https://doi.org/10.1038/s41467-026-70126-7
Ключевые слова: модификация тРНК, окислительный стресс, синтез белка, регуляция трансляции, повреждение РНК