Clear Sky Science · ru
Таргетирование зависящего от тРНК использования тирозина выявляет метаболическую уязвимость при гепатоцеллюлярной карциноме
Лишение раковых клеток распространённого строительного блока
Клетки рака печени, как и все быстро делящиеся клетки, нуждаются в постоянном поступлении аминокислот — мельчайших строительных блоков белков. Это исследование показывает, что гепатоцеллюлярная карцинома, наиболее распространённая форма рака печени, имеет неожиданную слабость: она сильно зависит от аминокислоты тирозина и для выработки энергии, и для выживания. Селективно ограничивая использование тирозина раковыми клетками, исследователи смогли замедлить рост опухолей, повредить энергетические центры клеток и вызвать форму клеточной гибели, которую можно использовать для новых методов лечения.
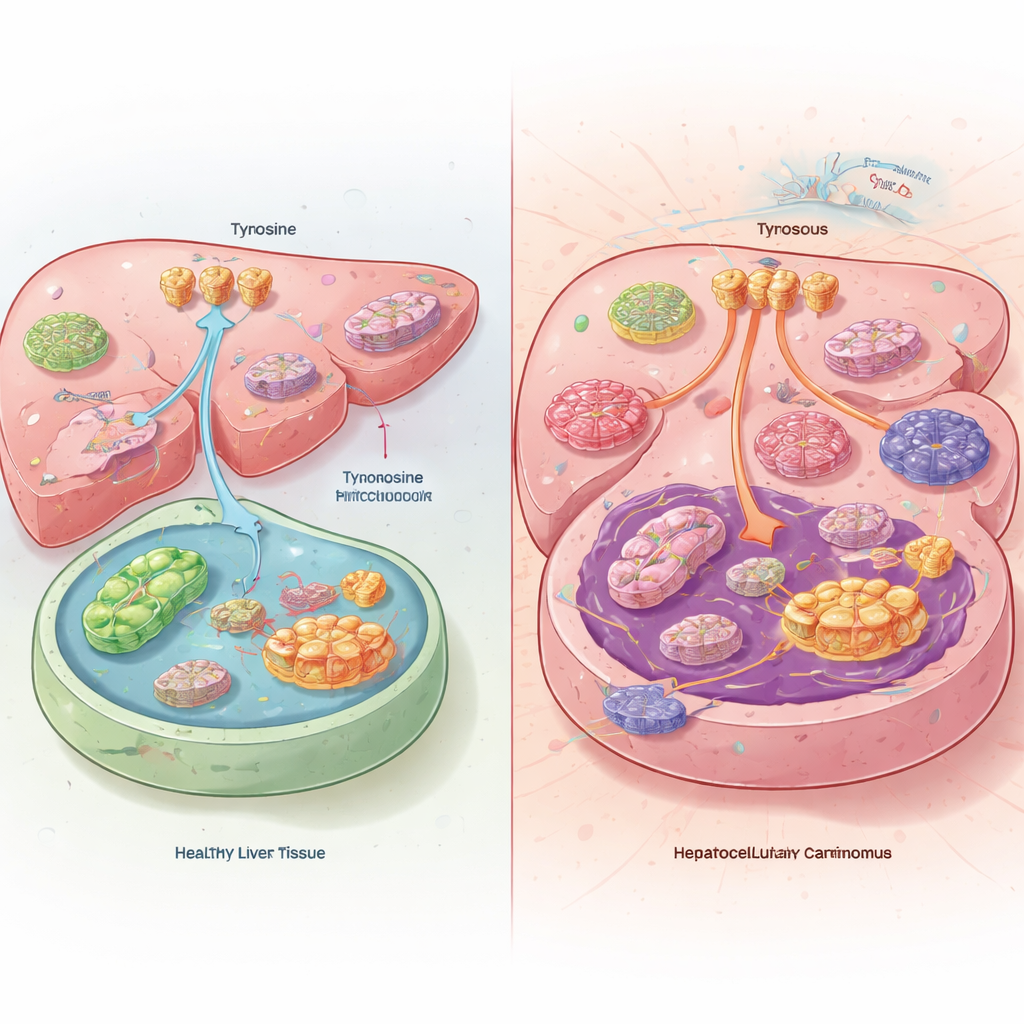
Скрытый дисбаланс в опухолях печени
При сравнении опухолей печени с нормальной тканью печени у пациентов и мышей команда обнаружила нечто парадоксальное. Внутри раковых клеток уровень тирозина был фактически низким, хотя опухоли поглощали больше тирозина из крови и реже его расщепляли. Вместо того чтобы использовать тирозин как топливо, опухоли перенаправляли его в синтез белков. Рак добивался этого за счёт повышения активности транспортёров тирозина на поверхности клеток и снижения активности ферментов, которые обычно разрушали тирозин в печени. Мыши на диете без тирозина развивали меньшие опухоли и жили дольше, в то время как избыток тирозина в пище ускорял рост их рака.
Как рак перестраивает синтез белка
Исследователи проследили эту «жажду» тирозина до мощного онкогена MYC. В опухолях печени MYC включает белок YARS1, который присоединяет тирозин к специфической транспортной РНК (tRNA-TyrGUA). Эта заряженная тРНК необходима рибосомам для сборки белков, богатых тирозином. В работе показано, что раки печени увеличивают экспрессию как YARS1, так и соответствующей тРНК, обеспечивая привилегированный поток тирозина в синтез белков. Нарушение этого канала — снижение уровня тирозина, подавление YARS1 или tRNA-TyrGUA либо блокировка загрузки тирозина — резко снижало жизнеспособность раковых клеток в культурах и у мышей, выявляя метаболическую уязвимость, тесно связанную с их высокой потребностью в синтезе белка.
Подрыв энергетических центров и жирового баланса
Объединив данные о глобальном уровне РНК, синтезе белков и метаболитах, команда выделила два особенно чувствительных мишени при ограничении тирозина. Первая, NDUFB8, является компонентом митохондриального комплекса I — ключевого элемента энергетической машины клетки. Вторая, SCD1, помогает превращать насыщенные жиры в мононенасыщенные, которые безопаснее хранить в мембранах и липидных каплях. При ограничении тирозина, используемого для трансляции, производство NDUFB8 и SCD1 снижалось, тогда как уровни их РНК оставались в основном неизменными — явное свидетельство того, что страдает трансляция, а не транскрипция. Это приводило к плохо собранному комплексу I, снижению клеточного дыхания, избытку реактивных форм кислорода и смещению жирового состава от мононенасыщенных жиров в сторону более хрупких полиненасыщенных форм, легко окисляющихся.
Вытеснение раковых клеток в железозависимую гибель
Комбинация митохондриального повреждения и нестабильных липидов толкала клетки рака печени к ферроптозу — железозависимой форме клеточной смерти, вызванной перекисным окислением липидов. Опухоли пытались сопротивляться, увеличивая уровни естественных блокаторов ферроптоза, таких как GPX4 и родственные молекулы, но крупный скрининг CRISPR показал, что отключение этих защитников делает ограничение тирозина ещё более губительным. В клеточных и мышиных моделях сочетание стратегий ограничения тирозина с препаратами, ингибирующими GPX4 или BCL2 — или с существующими лекарствами против рака печени, такими как сорафениб и венетоклакс — обеспечивало более сильный контроль опухолей, уменьшение их бремени и увеличение выживаемости.
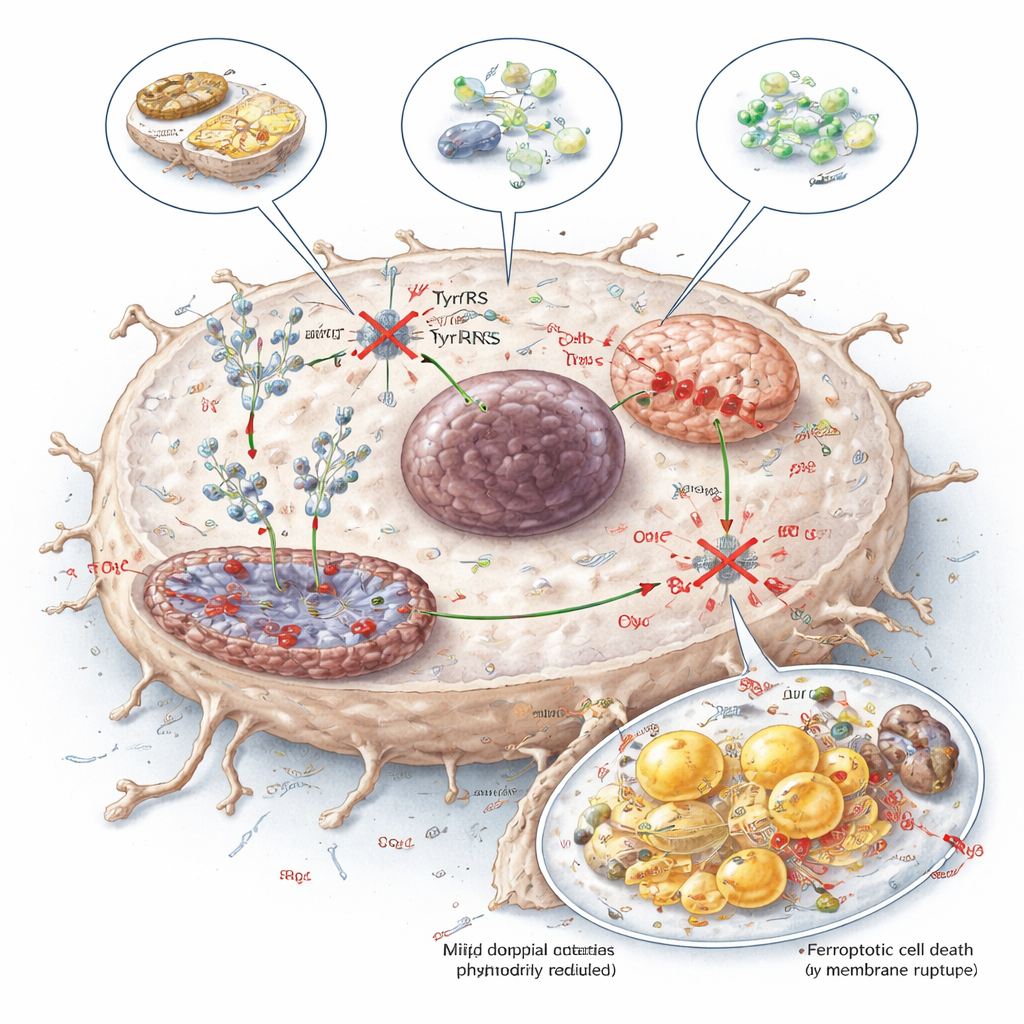
Преобразование метаболической слабости в терапию
Чтобы исследовать практические пути использования этой уязвимости, учёные проверили три подхода: диету с ограничением тирозина, фермент (TAL), который ферментативно разрушает тирозин, и малую молекулу тирозинол, конкурирующую с тирозином за связывание с YARS1. Все три снижали доступность тирозина для синтеза белков, уменьшали уровни NDUFB8 и SCD1, нарушали митохондриальную функцию и усиливали ферроптоз в опухолях печени, при этом вызывая контролируемые эффекты в нормальных тканях мышей. Для непрофессионала главный вывод таков: раки печени, по-видимому, зависят от тирозина не только как от питательного вещества, но и как от точного топлива для их белкового аппарата. Таргетирование этой зависимости — диетой, ферментами или лекарствами — открывает перспективный путь ослабления опухолей и усиления эффекта существующих методов лечения.
Цитирование: Zhang, H., Wang, Z., Zhao, Y. et al. Targeting tRNA-dependent tyrosine usage unveils a metabolic vulnerability in hepatocellular carcinoma. Nat Commun 17, 2244 (2026). https://doi.org/10.1038/s41467-026-70112-z
Ключевые слова: рак печени, метаболизм аминокислот, тирозин, митохондрии, ферроптоз