Clear Sky Science · ru
Систематическое выявление взаимодействий варианта-специфичной РНК-структуры с малыми молекулами на примере РНК G-квадруплексов
Почему крошечные изменения в РНК важны для будущих лекарств
Большинство из нас наследует небольшие различия в ДНК, которые делают нас уникальными. Эти крошечные изменения могут тонко перестраивать укладки молекул РНК внутри клеток. Новое исследование представляет метод, позволяющий увидеть, как такие генетические поправки изменяют «сцепление» экспериментальных препаратов, направленных на РНК. Это важно, потому что одно и то же лекарство может вести себя очень по-разному у разных людей, особенно при раке или генетических заболеваниях.
Новый способ увидеть, где препараты контактируют с РНК
Многие разработчики сейчас рассматривают РНК, а не только белки, как терапевтические мишени. Мелкие молекулы могут прикрепляться к специфическим формулам РНК и влиять на то, как читаются гены, но до сих пор большинство методов работали только с одной «эталонной» последовательностью РНК. Они во многом игнорировали бесчисленные однобуквенные изменения, встречающиеся у реальных пациентов. Авторы создали высокопроизводительный подход под названием BIVID-MaP, который позволяет одновременно проверить тысячи вариантов РНК и точно определить, где именно каждая малая молекула связывается — с разрешением до одной нуклеотидной позиции. 
Превращение химических меток в читаемый сигнал
BIVID-MaP работает в три основных этапа. Во‑первых, команда присоединяет реакционноспособную метку к малой молекуле, связывающейся с РНК. Когда этот помеченный препарат внедряется в предпочитаемую РНК‑структуру, например в компактный G‑квадруплекс, образующийся в гуанин-обогащённых последовательностях, метка формирует постоянную химическую связь с близлежащим основанием РНК. Во‑вторых, специальный фермент копирует модифицированную РНК в ДНК. Когда он сталкивается с такой химической меткой, он склонен «пропускать» одно основание, создавая крошечное делецированное расхождение в копии. В‑третьих, глубокое секвенирование считывает эти сигнатуры делеций по миллионам молекул. Поскольку почти весь окружающий контекст последовательности сохраняется, делеции можно точно отнести к конкретным генетическим вариантам в смешанной популяции.
Проверка метода на контролируемом примере
Чтобы подтвердить, что BIVID-MaP действительно обнаруживает вариант-специфическое связывание, исследователи изучили сегмент РНК гена CD44, который обычно образует G‑квадруплекс. Одна замена G→A разрушает эту структуру. В смеси, содержащей обе версии, только интактная форма показала сильные сигналы делеций вблизи свернутой области при воздействии на неё зонда на основе берберина, а независимые анализы подтвердили более сильное связывание там. Мутант, не способный сформировать ту же конфигурацию, дал гораздо меньше делеций и слабое связывание. Другие распространённые методы картирования либо пропустили это различие, либо дали запутывающий фон, что подчёркивает улучшенную чувствительность и специфичность нового подхода.
Просмотр мутаций, связанных с раком, в множестве генов
Затем команда масштабировала подход. Они построили библиотеку РНК 5′-нескодируемых участков (5′ UTR) из 283 генов, связанных с раком, каждую в паре с реальными соматическими мутациями, зарегистрированными в опухолях. Используя зонд, распознающий структуры, подобные G‑квадруплексам, BIVID-MaP выявил множество мутаций, которые либо усиливали, либо ослабляли связывание малыми молекулами. В генах, таких как DAXX и ING2, однобуквенные изменения в гуанин-обогащённых участках заметно изменяли связывание, что соответствовало независимым биофизическим тестам образования G‑квадруплексов и прямым измерениям связывания методом масс‑спектрометрии. В некоторых случаях мутации за пределами очевидных G‑тредов по‑прежнему сдвигали связывание, тонко меняя вероятность спаривания соседних оснований и перестраивая структурный «ансамбль» без грубого изменения предсказанной общей складки. 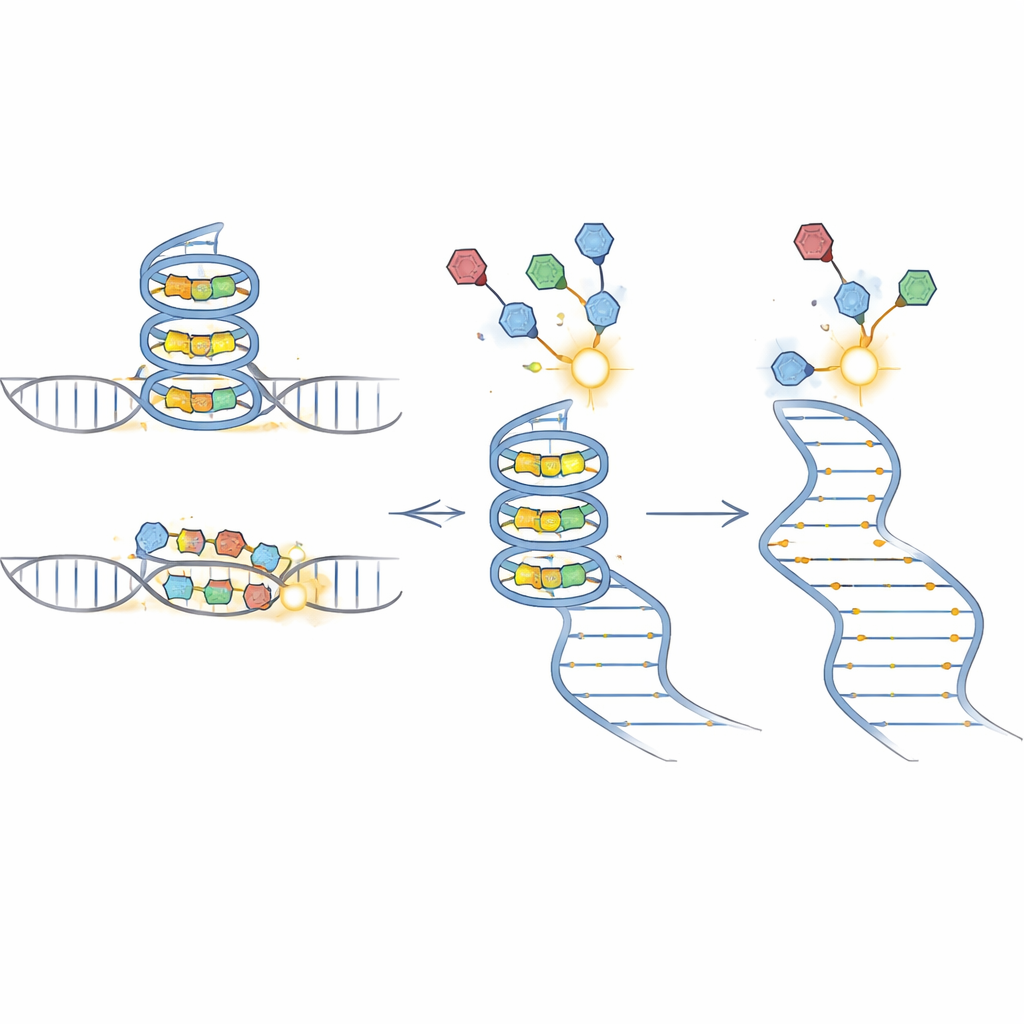
То, что пропускают компьютерные предсказания
Важно, что существующие инструменты предсказания структур РНК и G‑квадруплексов часто не смогли предсказать изменения, которые выявил BIVID-MaP. Некоторые варианты, почти не меняющие вычислительные оценки, в реальности вызывали большие различия в связывании. Другие, по-видимому, влияли на связывание в рамках семейства соединений, нацеленных на G‑квадруплексы, в то время как отдельные мутации имели эффект, специфичный для определённого препарата. Это показывает, что однонуклеотидные варианты могут настраивать ландшафт РНК‑укладок и контактов с лекарствами способами, которые трудно вывести только по последовательности.
Что это значит для персонализированных лекарств против РНК
Авторы заключают, что BIVID-MaP предлагает мощный путь для картирования того, как индивидуальные генетические различия перестраивают РНК‑структуры и их взаимодействия с малыми молекулами. Преобразуя локальные химические модификации в точные сигнатуры делеций, метод может параллельно обследовать тысячи вариантов и выделять те, которые существенно меняют связывание препаратов. В долгосрочной перспективе такие карты могут направлять разработку лекарств, нацеленных на РНК, которые будут эффективнее и безопаснее для разных пациентов, а также выявлять ранее скрытые РНК‑структуры, которые могут служить новыми терапевтическими мишенями.
Цитирование: Miyashita, E., Onizuka, K., Chen, Y. et al. Systematic identification of variant-specific RNA structure-small molecule interactions exemplified by RNA G-quadruplexes. Nat Commun 17, 2243 (2026). https://doi.org/10.1038/s41467-026-70097-9
Ключевые слова: Лекарства, нацеленные на РНК, G-квадруплекс, генетические варианты, связывание малыми молекулами, онкогенные мутации