Clear Sky Science · ru
Оптимизация пространственной организации колец FtsZ для масштабного стягивания в синтетических клетках
Почему маленькие кольца важны для создания синтетических клеток
Представьте себе конструирование простой искусственной клетки, которая может самостоятельно расти и делиться пополам. Для этого учёным нужно научиться контролируемо сжимать мягкую, похожую на мыльный пузырь мембрану, используя лишь несколько биологических компонентов. В этом исследовании показано, как бактериальному белку помогают образовывать большие стабильные кольца на гигантских липидных пузырях, позволяя этим модельным «клеткам» почти дойти до разделения. Работа раскрывает, какая архитектура белковых элементов необходима, чтобы изгибать и перестраивать мембрану в масштабе целой клетки.
Заимствование набора инструментов деления у природы
Многие бактерии делятся с помощью белка FtsZ, далёкого родственника тубулина, из которого построен внутренняя скелет наших клеток. FtsZ собирается в филаменты, которые формируют кольцо в середине клетки, отмечая место будущего расщепления. В живых бактериях множество вспомогательных белков прикрепляют это кольцо к внутренней мембране, позиционируют его по центру и связывают с ферментами, перестраивающими клеточную стенку. Предыдущие лабораторные попытки воссоздать этот аппарат в крупных везикулах размером с клетку умели образовывать кольца и вызывать небольшие вмятины в мембране, но не обеспечивали плавного прогрессивного стягивания, которое преобразовало бы гигантскую везикулу в две почти отдельные половины.
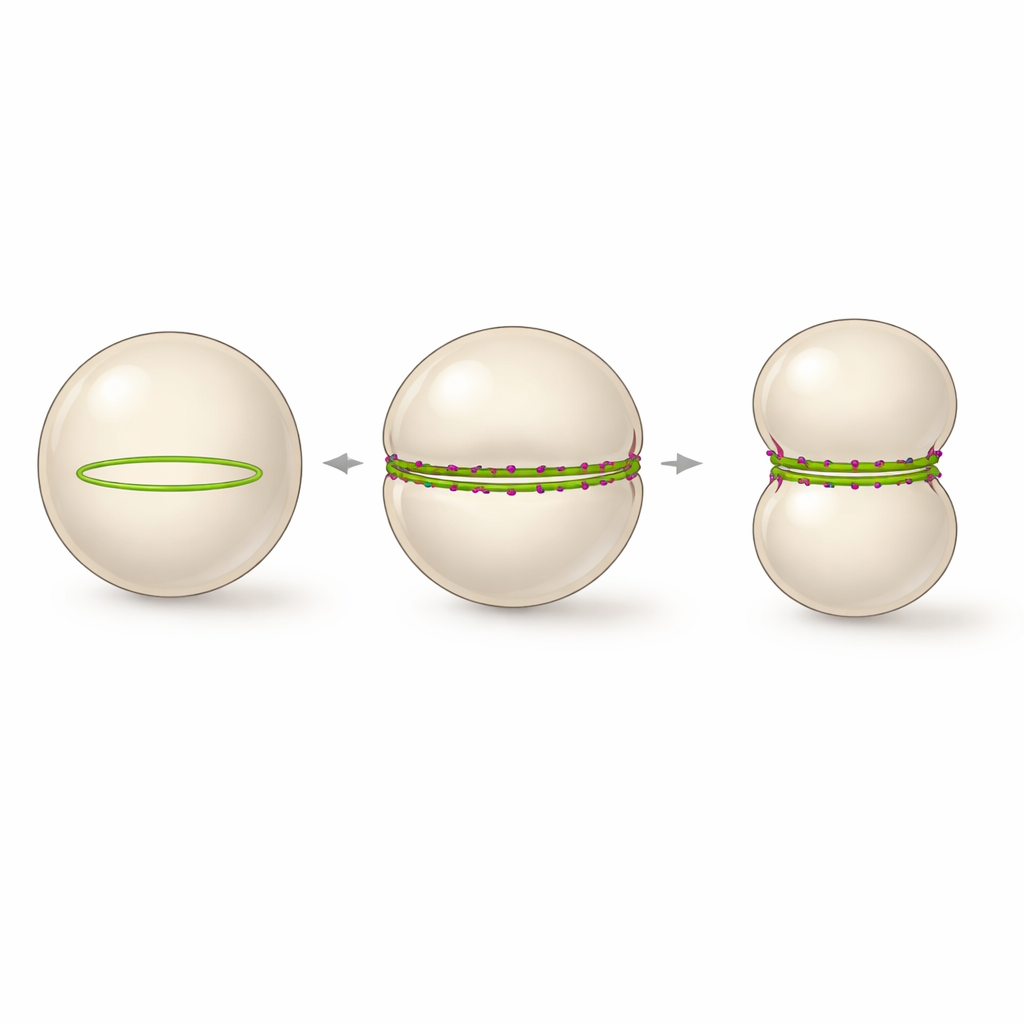
Минималистский подход к делящейся оболочке
Авторы поставили вопрос, можно ли упростить систему до двух компонентов: варианта FtsZ, способного напрямую прикрепляться к мембранам, и короткого положительно заряженного хвоста от другого белка деления, FtsN. Они инкапсулировали эти компоненты внутрь гигантских однослойных везикул — полых сфер липидов, напоминающих упрощённые клетки — и снабдили их энергетической молекулой GTP и медленно действующим аналогом GTP, чтобы настроить динамику белков. Без хвоста FtsN FtsZ образовывал множество мелких колец и пятен, вызывавших лишь локальные вмятины. При избытке фрагмента FtsN (называемого cytoFtsN) эти маленькие кольца реорганизовывались в единое большое кольцо, обёртывающее везикулу вблизи её экватора и способное стягиваться в течение нескольких часов.
От запутанной сети к единому сократительному кольцу
Чтобы понять, как эта маленькая пептидная часть так резко меняет поведение, команда наблюдала филаменты FtsZ на плоских поддерживающих мембранах с высоким разрешением. Как правило, FtsZ на таких поверхностях формирует закручивающиеся изогнутые вихри. Добавление растущих количеств cytoFtsN постепенно стирало эти спирали и заменяло их более прямыми, выровненными пучками. Количественный анализ изображений подтвердил, что сеть становилась более связной и упорядоченной по мере увеличения концентрации пептида. Эксперименты по восстановлению флуоресценции показали, что субъединицы внутри этих пучков обменивались медленнее, что указывает на то, что пептид стабилизирует филаменты и снижает их интенсивную динамику.

Электростатическое «липучка», блокирующее сдвиг филаментов
Биохимические измерения показали, что cytoFtsN и FtsZ взаимодействуют главным образом через противоположные электрические заряды: FtsZ в целом отрицателен, тогда как пептид несёт кластеры положительных зарядов. При более низкой солёности пептид связывался сильнее, способствовал образованию более толстых пучков FtsZ в растворе и замедлял распад филаментов, подавляя GTP‑азную активность белка. Когда исследователи заменяли ключевые положительно заряженные остатки в пептиде или повышали концентрацию соли, экранируя электростатическое притяжение, эффект агрегации и реорганизации исчезал. Это указывает на простый физический механизм, при котором положительно заряженный пептид действует как молекулярная «липучка», уменьшая отталкивание между филаментами FtsZ и позволяя им уплотняться бок о бок в жёсткие пучки.
Как единое кольцо перестраивает гигантскую везикулу
Внутри везикул стабилизированное пептидом образование пучков имеет яркое следствие. Вместо множества мелких изогнутых колец выпрямлённые пучки FtsZ вынуждены следовать за большой кривизной везикулы, собираясь в одно непрерывное кольцо, охватывающее всю окружность. Серийная съёмка показала, что всякий раз, когда такое полностью замкнутое кольцо образовывалось, везикула надёжно деформировалась из сферы в гантелеобразную форму с узкой талией в месте расположения кольца. Процесс можно было наблюдать в реальном времени: диаметр везикулы уменьшался, и стягивание углублялось, почти разъединяя компартмент на две части, хотя окончательного перерезания не происходило. Авторы предлагают, что стабильное кольцо FtsZ, охватывающее экватор и обладающее замедленным, но всё ещё активным обновлением субъединиц, является минимальной архитектурой, необходимой для масштабного стягивания мембраны в синтетической клетке.
Что это значит для будущей синтетической жизни
Показав, что мембранно‑якорённый вариант FtsZ в сочетании с коротким катионным пептидом может почти довести гигантские липидные везикулы до деления, эта работа устанавливает ясное правило проектирования для искусственных клеток: одно единое согласованное белковое кольцо, соответствующее размеру клетки и механически стабильное во времени, достаточно, чтобы сжать мягкую границу в клеточном масштабе. Для полного разрыва мембраны могут потребоваться более сложные факторы, но исследование демонстрирует, что управляемое масштабное стягивание не требует полного набора бактериальных белков деления. Вместо этого тщательная настройка организации и динамики филаментов может превратить простой белковый каркас в эффективное сократительное кольцо, приблизив создание по‑настоящему самоделящихся синтетических клеток.
Цитирование: Panevska, A., Šakanović, A., Paccione, G. et al. Optimizing spatial organization of FtsZ rings for large-scale constriction in synthetic cells. Nat Commun 17, 2320 (2026). https://doi.org/10.1038/s41467-026-70091-1
Ключевые слова: деление синтетической клетки, кольцо FtsZ, стягивание мембраны, минимальный дивизом, самоорганизация цитоскелета