Clear Sky Science · ru
Динамическое распределение тандемных генетических амплификаций в гетерорезистентной популяции Escherichia coli, выявленное с помощью ультраглубокого секвенирования длинных чтений
Скрытые карманы выживания
Когда врачи лечат бактериальные инфекции антибиотиками, они обычно предполагают, что всё сообщество микробов ответит одинаково. Но иногда небольшая доля популяции тихо сопротивляется, переживает лечение и создаёт почву для неудачи терапии или рецидива. В этом исследовании показано, как появляются такие редкие выжившие и как меняются со временем в Escherichia coli, а также предложен мощный метод для наблюдения этих генетических изменений на уровне отдельных молекул ДНК.
Малые генетические повторы, большие последствия
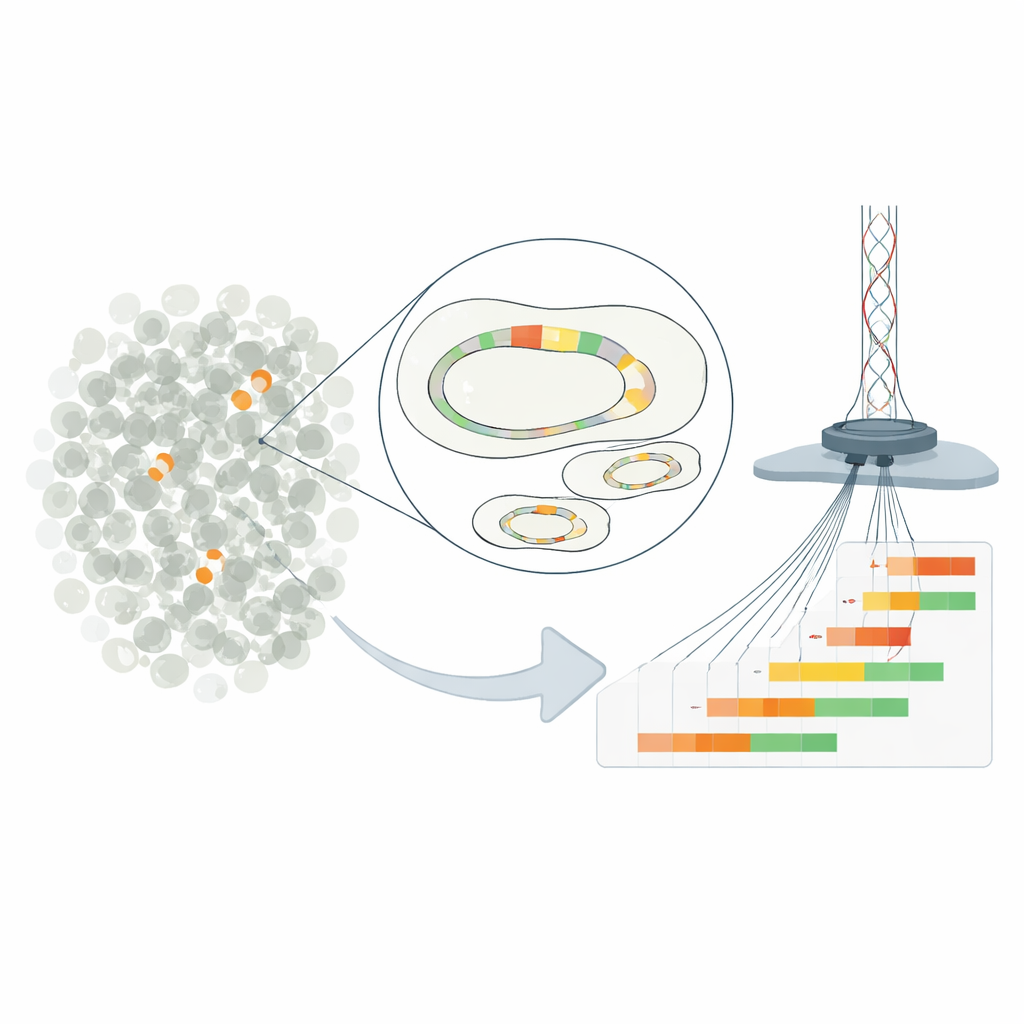
Работа посвящена «гетерорезистентности» — ситуации, когда большинство бактерий в образце кажутся чувствительными к препарату, но небольшое меньшинство выдерживает значительно более высокие дозы. В исследуемом штамме E. coli такое поведение объясняется повторяющимися копиями гена резистентности, находящегося на плазмиде — небольшой кольцевой ДНК, отделённой от основной хромосомы. Дублируя короткий сегмент ДНК с геном бета-лактамазы, бактерии могут увеличить выработку фермента, разрушающего антибиотик пиперациллин‑тазобактам. Чем больше повторов несёт клетка, тем больше фермента она синтезирует и тем выше её шансы выжить в присутствии препарата.
Чтение ДНК‑колец с беспрецедентной детализацией
Традиционные методы позволяют лишь оценить среднее число копий гена по всей бактериальной популяции, скрывая богатое разнообразие между отдельными клетками. Чтобы преодолеть это, исследователи модифицировали клиническую плазмиду так, чтобы её можно было разрезать в точном месте и затем изолировать от остального генома. Они использовали ультраглубокое Nanopore-секвенирование длинных чтений, чтобы прочитать полные молекулы плазмид от конца до конца и точно сосчитать, сколько повторяющихся единиц резистентности содержит каждая из них. Этот подход достиг разрешающей способности до одной клетки на 100 000, выявив плазмиды с нулём и более чем дюжиной копий гена, сосуществующие в той же культуре. Проверки другими методами подтвердили, что в среднем новый метод даёт точные оценки числа копий.
Как антибиотики перестраивают популяцию
С этим инструментом в распоряжении команда проследила, что происходило при воздействии на культуры E. coli возрастающих доз пиперациллин‑тазобактама, а затем при удалении препарата. По мере роста концентрации антибиотика распределение сдвигалось в сторону плазмид с большим числом копий гена резистентности, но клетки с меньшим числом копий никогда полностью не исчезали. После отмены препарата и культивирования в течение сотен поколений популяция только постепенно сдвигалась обратно к более низким числам копий и никогда полностью не возвращалась к исходному состоянию. Отдельные тесты роста показали, что каждая дополнительная копия гена давала измеримый шаг в увеличении толерантности к препарату, тесно связывая наблюдаемые генетические распределения с видимым паттерном гетерорезистентности в стандартных лабораторных анализах.

Защита от соседей и тихие издержки
Чтобы объяснить, почему клетки с малым числом копий сохранялись даже при сильном лечении, авторы построили математическую модель, объединяющую рост бактерий, разрушение антибиотика и случайные события, добавляющие или удаляющие копии гена. Моделирование показало, что ключевую роль играет «косвенная резистентность»: высокорезистентные клетки выделяют достаточно бета‑лактамазы, чтобы снизить концентрацию препарата в общем окружении, случайно защищая менее резистентных соседей. Пока дополнительные копии гена налагают лишь небольшие издержки на рост в отсутствие препарата, этот защитный эффект помогает поддерживать широкое распределение чисел копий, замедляя возврат к полностью чувствительной популяции. Модель также показала, как обычная адаптация к среде роста — не связанные с этим мутации, улучшающие рост — могут закреплять определённые состояния числа копий, делая некоторые субпопуляции более приспособленными, чем другие.
Почему это важно для пациентов и не только
Для неспециалистов важный вывод таков: бактериальная культура — не однородный враг, а постоянно меняющаяся смесь особей с разной способностью переживать антибиотики. Прямо считая копии гена на тысячах одиночных молекул ДНК, это исследование количественно связывает скрытое разнообразие с клинически значимой резистентностью. Такие выводы могут улучшить использование секвенирования геномов для предсказания трудно обнаруживаемой гетерорезистентности, помочь выявлять штаммы бактерий, особенно склонные к неэффективности лечения, и направить разработку более точных диагностических тестов. Поскольку тандемные амплификации генов также ускоряют адаптацию вирусов, опухолей и других организмов, тот же подход можно применить далеко за пределами E. coli, открывая новое окно в то, как повторяющиеся фрагменты ДНК помогают жизни обходить угрозы.
Цитирование: Jonsson, S., Guliaev, A., Berryhill, B.A. et al. The dynamic distribution of genetic tandem amplifications in a heteroresistant Escherichia coli population revealed by ultra-deep long read sequencing. Nat Commun 17, 2113 (2026). https://doi.org/10.1038/s41467-026-70044-8
Ключевые слова: гетерорезистентность к антибиотикам, амплификация генов, Escherichia coli, секвенирование длинных чтений, бета-лактамаза