Clear Sky Science · ru
Динамика одной молекулы показывает, что одно только связывание АТФ приводит к транспорту субстрата белком-переносчиком ABC
Почему важны крошечные клеточные насосы
Каждая клетка вашего организма полагается на микроскопические машины, которые перемещают молекулы через мембраны и определяют всё — от поглощения питательных веществ до иммунной защиты. Одна из основных семейств таких машин — ABC‑переносчики — использует химическое топливо клетки, АТФ, чтобы протолкнуть грузы «вверх по течению», против градиентов. В течение десятилетий учёные спорили о базовом вопросе: достаточно ли простого факта связывания АТФ, чтобы обеспечить шаг транспорта, или энергия выделяется только при гидролизе АТФ? Это исследование изучает один переносчик молекула за молекулой, чтобы разрешить спор.
Наблюдение за одним переносчиком за раз
Вместо измерения суммарного поведения миллионов молекул исследователи создали установку, которая позволяет отслеживать отдельные события транспорта в реальном времени. Они сосредоточились на TmrAB, бактериальном аналоге человеческого переносчика TAP, который загружает иммунные пептиды для представления цитотоксическим Т‑клеткам. TmrAB встраивается в мембрану и переносит короткие белковые фрагменты (пептиды) с одной стороны на другую, используя АТФ. Чтобы увидеть каждый шаг транспорта, команда захватила отдельную молекулу TmrAB в искусственной мембранной пузырьке (липосоме) и поместила внутрь специально сконструированный «сенсорный» белок, который меняет флуоресценцию при захвате пептида. С помощью высокочувствительного микроскопа они могли наблюдать точные моменты, когда пептид за пептидом попадал внутрь пузырька, в виде кратких скачков светового сигнала.
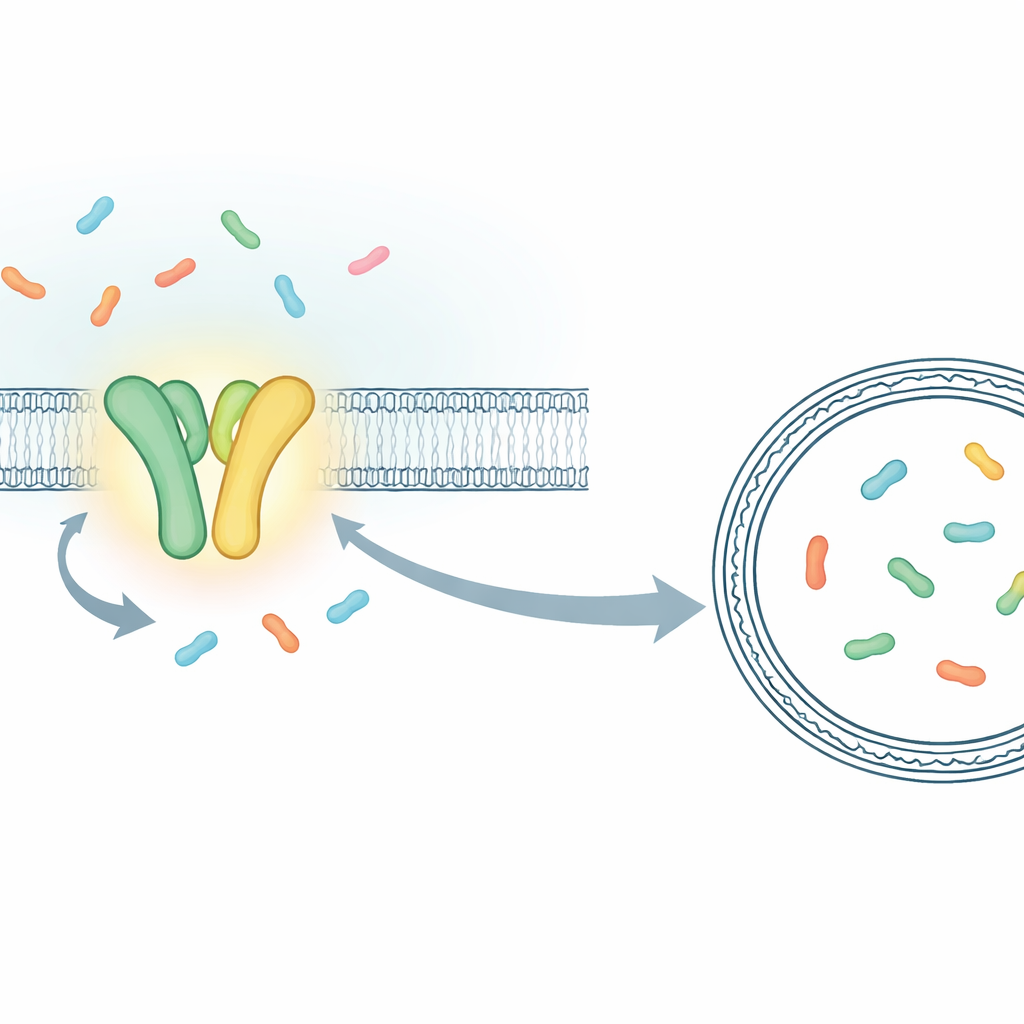
Доказательство: одно связывание АТФ перемещает один пептид
С этой одно-молекулярной методикой в руках исследователи сравнили нормальный TmrAB с модифицированным вариантом с медленным циклом, у которого стадии растянуты во времени. Медленный вариант позволил различать отдельные события, которые в противном случае сливались бы. Они показали, что при наличии АТФ и пептидов сенсор внутри липосомы переходил из «пустого» в «загруженное» состояние дискретными шагами, каждый из которых соответствовал переносу одного пептида. Проанализировав скорость закрывания сенсора вокруг пептидов и оценив крошечный объём внутри каждой липосомы, они даже перевели эти световые изменения в приближённые концентрации пептида. Числа соответствовали ожиданиям для накопления одного, затем двух пептидов в пузырьках диаметром около 100 нанометров, что подтверждало, что теперь они действительно считали события транспорта поштучно.
Само связывание АТФ переключает молекулярный механизм
Ключевой спор касался ионов магния (Mg2+), которые обычно сопровождают АТФ в клетках и необходимы для эффективного гидролиза АТФ. Некоторые модели предполагали, что Mg2+ может также требоваться для связывания АТФ или закрывания переносчика. Чтобы разделить эти роли, исследователи удалили Mg2+ с помощью хелатора, но при этом добавили АТФ. В этих условиях и нормальный, и медленный переносчик могли совершить ровно один шаг транспорта пептида на молекулу, а затем останавливались. Такое поведение указывает на то, что АТФ всё ещё может связываться и вынуждать переносчик перейти из внутрь-ориентированного в наружу-ориентированное состояние и переместить пептид даже без Mg2+. Однако без Mg2+ переносчик не может эффективно разложить АТФ и, следовательно, не может сброситься для следующего цикла.
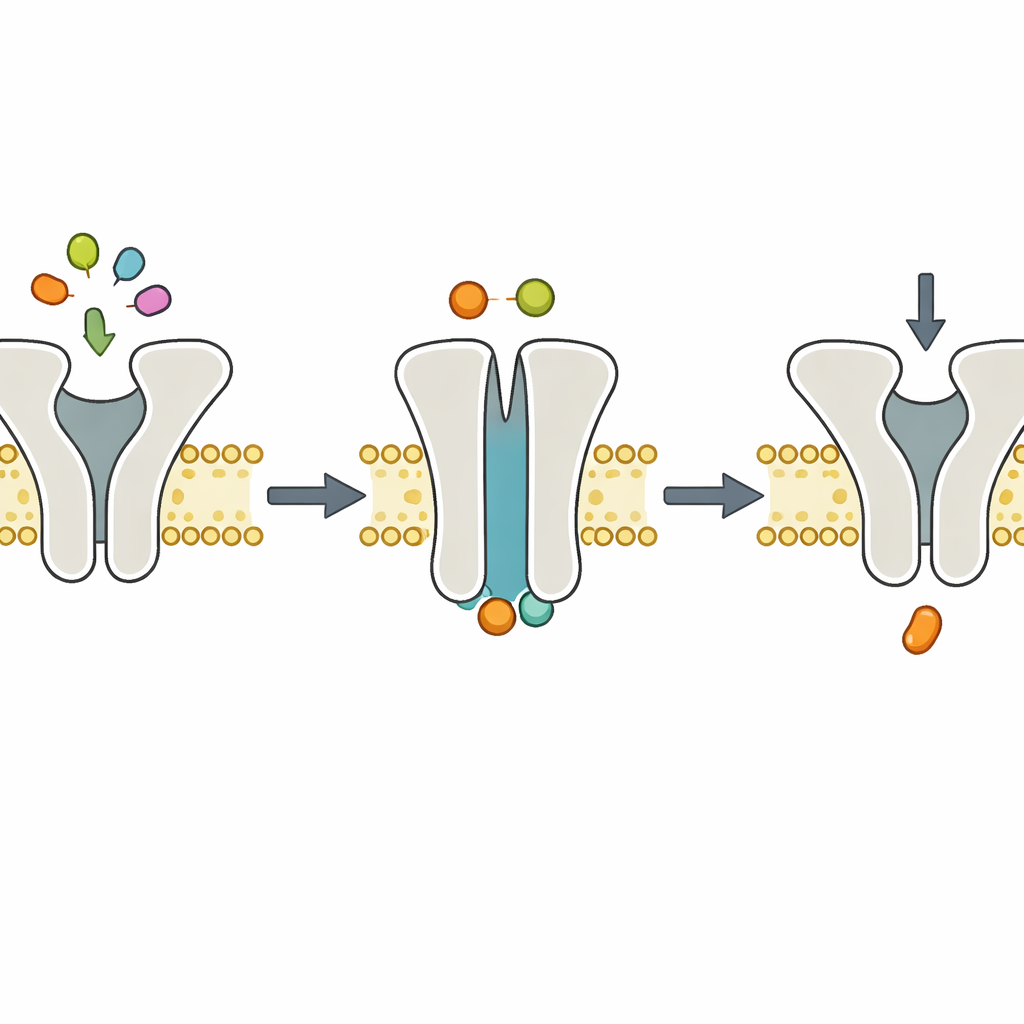
Структурные снимки подтверждают динамику
Чтобы увидеть, как выглядят молекулы в этом шаге без Mg2+, команда обратилась к крио‑электронной микроскопии, которая изображает замороженные молекулы с почти атомным разрешением. Они реконституировали TmrAB в липидных нандисках, добавили АТФ без Mg2+ и зафиксировали комплексы криозаморозкой. Полученные структуры показали TmrAB в наружно-ориентированной «окклюдированной» конформации с АТФ, вставшим в оба внутренних центры связывания, но без видимого Mg2+. Эти снимки практически не отличались от ранних структур, полученных при наличии и АТФ, и Mg2+. В сочетании с биохимическими тестами, показывающими, что гидролиз АТФ полностью останавливается без Mg2+, изображения поддерживают простое распределение ролей: связывание АТФ приводит к конформационному переключению, которое перемещает пептид, тогда как Mg2+‑зависимый гидролиз АТФ обеспечивает восстановление состояния переносчика.
Более ясная картина работы клеточных насосов
Наблюдая за одиночными переносчиками и определяя их структуры, эта работа разрешает давний вопрос об ABC‑переносчиках: механический «удар», перемещающий пептид, запускается самим связыванием АТФ, а не позднейшим химическим распадом АТФ. Mg2+ главным образом необходим, чтобы обеспечить гидролиз АТФ и тем самым вернуть переносчик в исходное состояние для повторной работы. Помимо прояснения фундаментального аспекта клеточной биологии, одно-молекулярный подход даёт шаблон для разбирательства с другими мембранными машинами, лежащими в основе иммунитета, лекарственной устойчивости и многих заболеваний — по одной молекуле и по одному шагу транспорта за раз.
Цитирование: Nocker, C., Pečak, M., Nocker, T. et al. Single-molecule dynamics reveal ATP binding alone powers substrate translocation by an ABC transporter. Nat Commun 17, 3038 (2026). https://doi.org/10.1038/s41467-026-70021-1
Ключевые слова: ABC-переносчики, связывание АТФ, одно-молекулярный FRET, мембранный транспорт, TAP и TmrAB