Clear Sky Science · ru
Наночастицы прусского синего, нацеленные на множественные PANoptosome-опосредованные пути PANoptosis для терапии ишемии‑реперфузии миокарда
Почему важно защищать сердце в период заживления
Когда человек переживает инфаркт, врачи стремятся как можно быстрее восстановить кровоток в перекрытой артерии. Этот спасительный шаг, однако, имеет скрытую цену: внезапное возвращение кислорода само по себе может повредить сердце, вызвав гибель клеток и подготовив почву для сердечной недостаточности. В этом исследовании рассматривается изобретательная наномедицина, нацеленная на защиту сердца в уязвимый период путем одновременного блокирования нескольких переплетенных путей гибели клеток, что потенциально обеспечивает более мягкое восстановление после инфаркта.
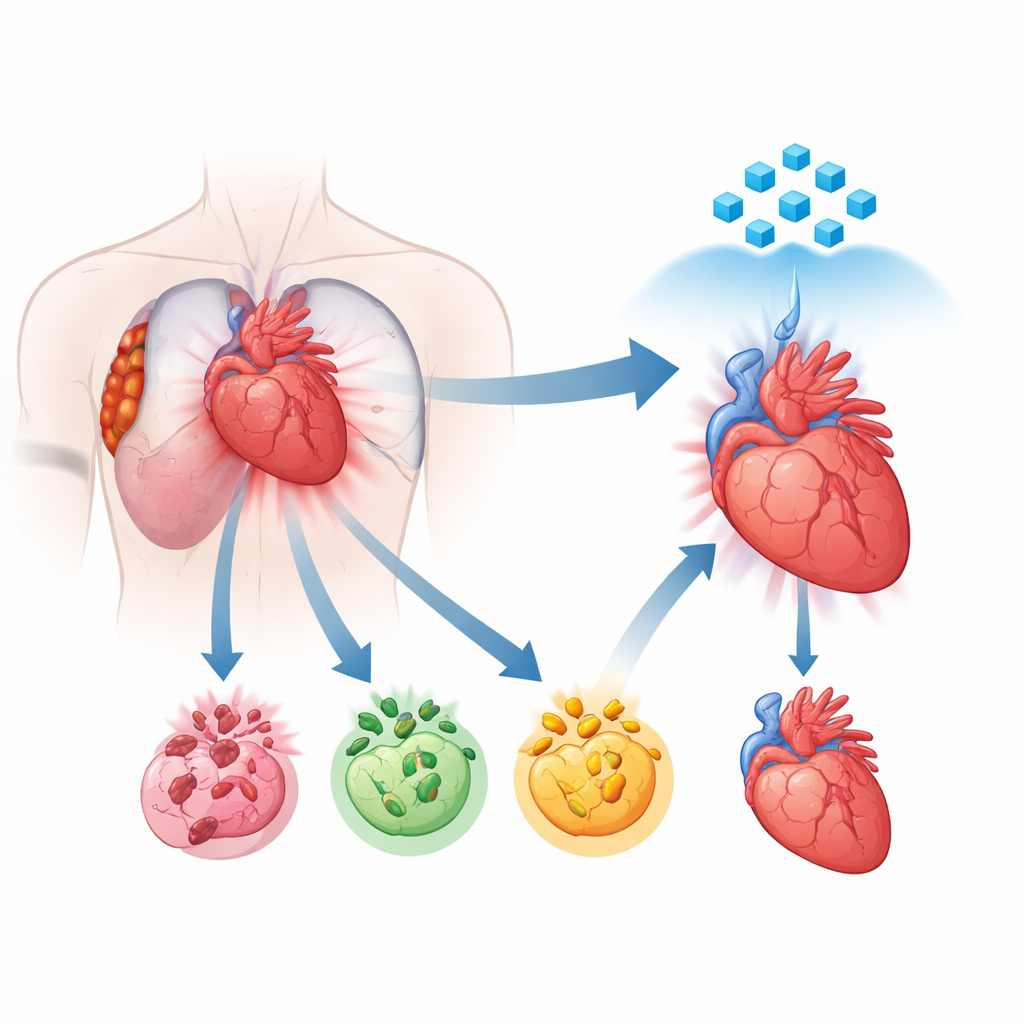
Новый взгляд на то, как гибнут клетки сердца
В течение многих лет ученым было известно, что поврежденные клетки сердца могут гибнуть через разные запрограммированные механизмы, включая апоптоз, некроптоз и пироптоз. Каждый из них следует собственной молекулярной «сценарной», но растет количество данных, показывающих, что эти пути не работают изолированно. Они взаимодействуют между собой и могут объединяться в комбинированный, неконтролируемый процесс, называемый PANoptosis. В таком состоянии несколько программ гибели запускаются одновременно, из‑за чего препараты, блокирующие только один путь, оказываются слабыми. Авторы использовали секвенирование отдельных ядер РНК (single‑nucleus RNA sequencing) на тканях человеческого сердца пациентов с недавним инфарктом, чтобы картировать, где и насколько мощно включаются эти программы гибели. Они обнаружили, что в наиболее поврежденных областях кардиомиоциты демонстрировали сдвиг в сторону этого комбинированного режима гибели, указывая на PANoptosis как на ключевой фактор повреждения.
Проектирование мини‑многоинструмента для поврежденного сердца
Чтобы справиться с таким сложным процессом, команда обратилась к прусскому синему — давно одобренному медицинскому соединению, наиболее известному как антидот при отравлениях некоторыми металлами. На наноуровне частицы прусского синего ведут себя как крошечные каталитические «роботы», которые могут нейтрализовать вредные молекулы и влиять на поведение клеток. С помощью компьютерного моделирования исследователи показали, что эти наночастицы могут непосредственно связываться с тремя ключевыми белковыми центрами — RIPK1, ZBP1 и AIM2 — которые участвуют в сборке молекулярного механизма PANoptosis. За счет связывания с этими узлами разными способами частицы, по прогнозам, способны нарушать формирование комплексов, индуцирующих гибель, координирующих три пути клеточной смерти.
Направление наночастиц прямо к поврежденной ткани сердца
Наночастицы работают только если достигают нужного места, поэтому командa покрыла частицы прусского синего естественными мембранами, полученными от тромбоцитов — клеток крови, ориентирующихся на поврежденные сосуды. Это покрытие создало PB@PM, биомиметический носитель, который циркулирует подобно тромбоциту, но доставляет терапевтический груз. У мышей, подвергнутых моделированному инфаркту с последующим восстановлением кровотока, визуализация показала, что PB@PM значительно сильнее накапливался в области повреждения сердца, чем непокрытые частицы, при этом в значительной степени избегая здоровых органов. Важно, что покрытые частицы хорошо переносились: анализы крови и исследования тканей не выявили очевидной токсичности, что поддерживает их потенциал для дальнейшей разработки.
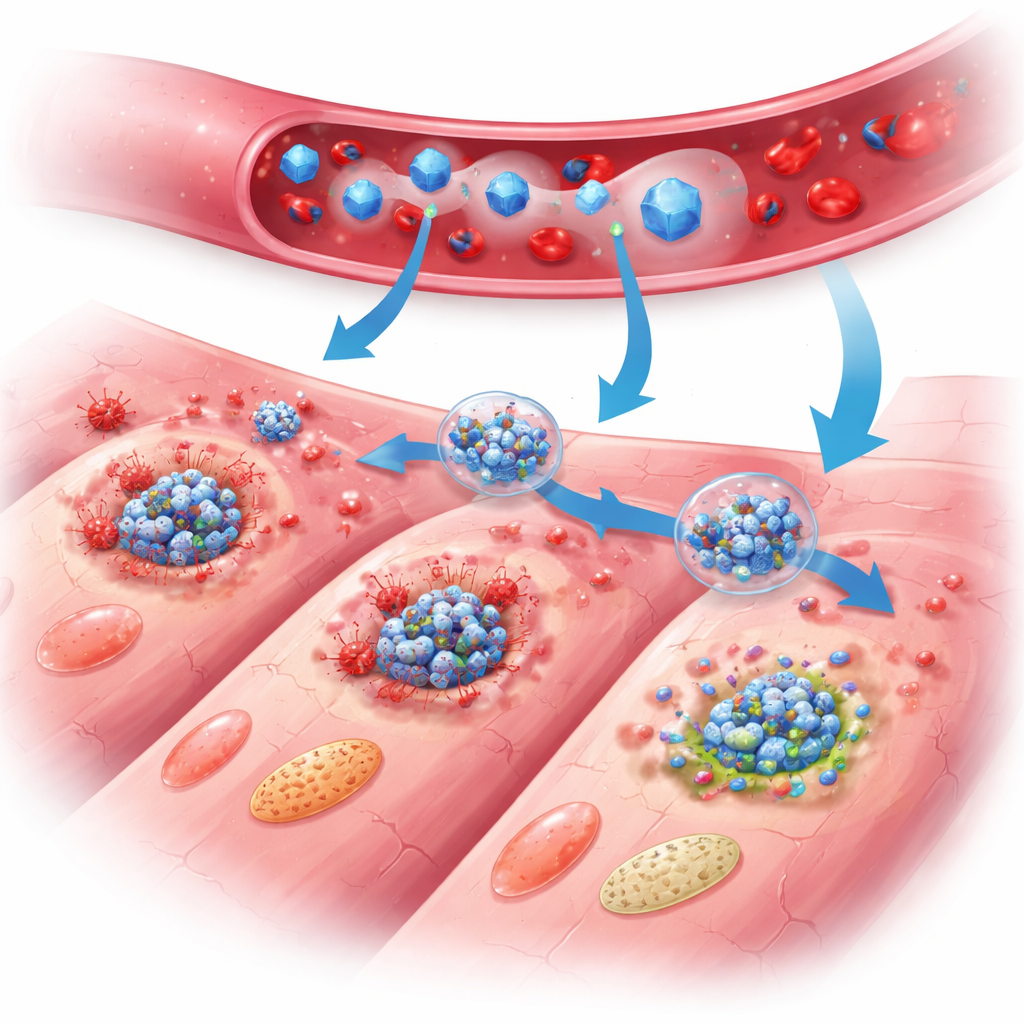
Как нано‑щит защищает сердце
У обработанных мышей преимущества PB@PM проявлялись в течение дней и недель. Функция сердечной сократимости улучшалась, размер рубца уменьшался, и утолщение стенки сердца было менее выраженным по сравнению с необработанными животными. Детальные исследования тканей показали меньше умирающих кардиомиоцитов, более спокойные воспалительные клетки и лучше структурированную рубцовую ткань с более здоровым ростом сосудов и меньшей аномальной гипертрофией выживших клеток. На молекулярном уровне широкое профилирование экспрессии генов и измерения белков показали, что PB@PM одновременно подавлял три основных запрограммированных пути гибели, нарушал сборку много-белковых комплексов PANoptosis и снижал уровни сигнальных молекул, подпитывающих воспаление. Частицы также захватывали вредные реактивные формы кислорода, стабилизировали митохондрии — энергетические станции клетки — и восстанавливали более нормальный энергетический метаболизм, устраняя ключевые триггеры, которые в противном случае толкали бы клетки к саморазрушению.
Что это может означать для будущей помощи при инфаркте
Проще говоря, работа показывает, что продуманно спроектированная наночастица может выступать как многогранный щит для сердца, ослабляя сеть разрушительных сигналов гибели, а не лавируя по одному пути за раз. Нацеливаясь на поврежденную ткань сердца, связывая ключевые регуляторные белки и снижая окислительный и воспалительный стресс, PB@PM резко сокращал цепную реакцию потери клеток и образования рубца, которая часто следует за восстановлением проходимости артерии. Хотя до клинического применения остается много испытаний, исследование предлагает доказательство концепции: целенаправленное подавление PANoptosis в целом — и выполнение этого с помощью интеллектуальных, биологически вдохновленных частиц — может открыть новую страницу в защите сердца после инфаркта.
Цитирование: Xu, L., Jiang, L., Wu, R. et al. Prussian blue nanoparticles targeting multiple PANoptosome-mediated PANoptosis for myocardial ischemia-reperfusion injury therapy. Nat Commun 17, 2329 (2026). https://doi.org/10.1038/s41467-026-70012-2
Ключевые слова: ишемия‑реперфузия миокарда, наночастичная терапия, запрограммированная гибель клеток, воспаление сердца, защита митохондрий