Clear Sky Science · ru
Таргетирование de novo синтеза пиримидинов открывает уязвимость к медь‑опосредованной инактивции ATR при резистентном к ингибиторам PARP раке яичников
Почему это исследование важно
Многих женщин с раком яичников лечат препаратами, которые подрывают способность опухолевых клеток восстанавливать повреждённую ДНК. Эти средства, называемые ингибиторами PARP, сначала часто действуют хорошо, но опухоли нередко адаптируются и рецидивируют. В этом исследовании показано, как препарат‑переносчик меди и ключевая метаболическая уязвимость могут заставить резистентные опухоли «перегрузиться», указывая путь к более эффективным комбинированным схемам и более длительным ответам на лечение.
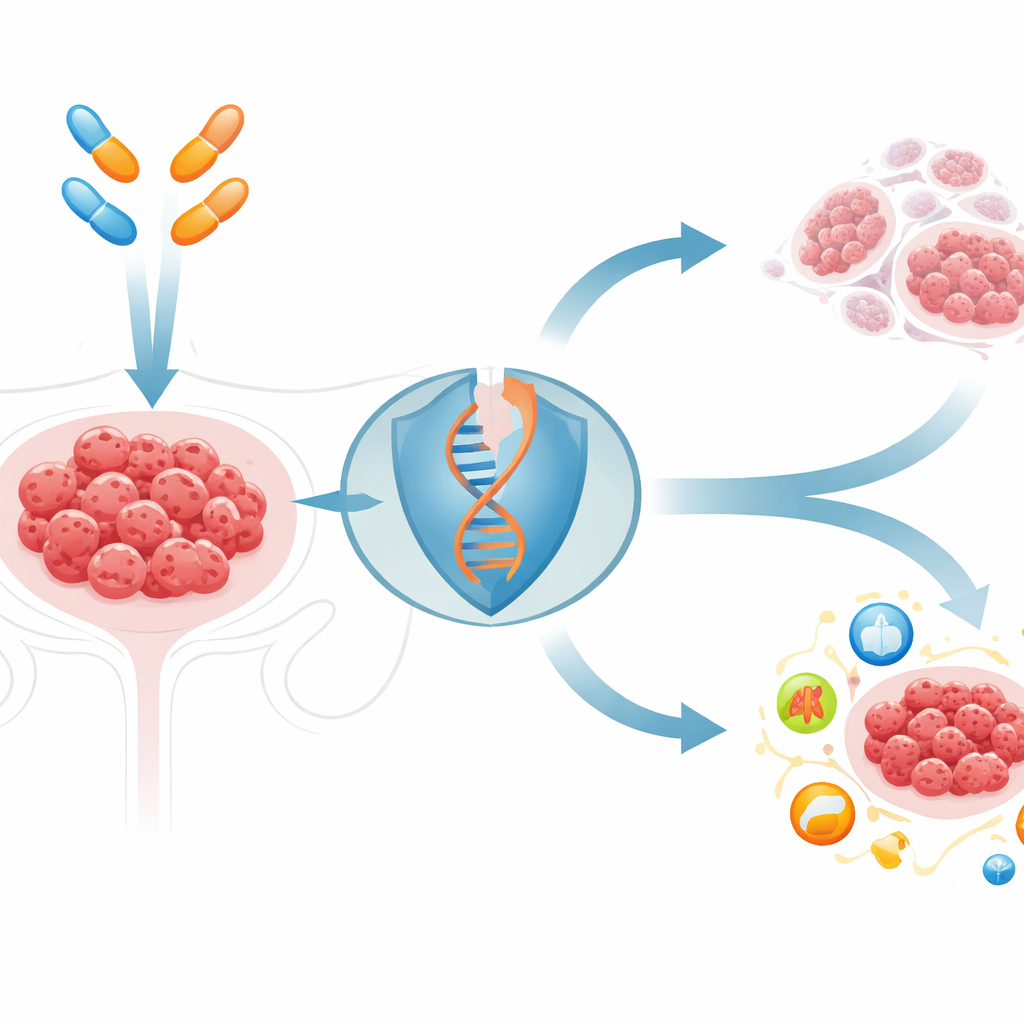
Как пробить упрямую защиту опухоли
Ингибиторы PARP эксплуатируют дефект в механизмах восстановления разрывов ДНК у некоторых опухолей. Они наиболее эффективны при опухолях с наследственными нарушениями генов BRCA, тогда как большинство раков яичников имеют целые BRCA и отвечают слабо или недолго. Исследователи просcreenировaли 144 соединения, связанных с гибелью клеток, в сочетании со стандартным ингибитором PARP и обнаружили, что одно вещество — элескломол — выделяется на фоне остальных. Элескломол доставляет медь в клетки. В сочетании с ингибиторами PARP в клеточных линиях рака яичников с нормальными BRCA и в мышиных опухолях это медь‑усиливающее средство резко увеличивало повреждение ДНК и сокращало размер опухолей гораздо сильнее, чем любой из препаратов по отдельности, не вызывая очевидной токсичности в здоровых органах.
Медь блокирует переключатель репарации ДНК
Чтобы понять, почему медь усиливала эффект блокады PARP, команда изучила ключевой сигнализационный путь ответа на повреждение ДНК, центром которого является белок ATR. Этот путь помогает клеткам выживать при стрессах репликации ДНК — именно такая ситуация создаётся ингибиторами PARP. В клетках опухолей, переживших первоначальное воздействие препаратов, ATR и его партнёр CHK1 были сильно активированы, в то время как родственный путь ATM‑CHK2 оставался тихим. Подробные биохимические испытания и компьютерное структурное моделирование показали, что медь напрямую связывается с белком‑помощником ATR, ATRIP, в конкретных сайтах цистеина. Это связывание искажает конформацию ATRIP, разрывает его взаимодействие с ATR и выключает сигнализацию ATR‑CHK1, оставляя повреждённую ДНК невосстановленной и делая клетки, обработанные PARP, намного более склонными к гибели.
Скрытая роль нуклеотидного топлива
Даже при одновременной инвалидизации ATR и PARP некоторые раковые клетки и остаточные опухоли умудрялись выживать. Чтобы понять, как, исследователи профилировали сотни малых молекул в клетках, адаптированных к лекарствам. Они обнаружили заметный рост концентраций строительных блоков ДНК — пиримидинов, особенно синтезируемых по пути de novo, когда клетки собирают эти компоненты с нуля. Трассерные эксперименты подтвердили, что резистентные клетки направляют больше атомов азота от глутамина в свежесинтезированные пиримидины, в то время как пуриновые блоки не демонстрировали аналогичного увеличения. Добавление в культуры дополнительных пиримидиновых компонентов, таких как уридин или тимидин, ослабляло убивающий эффект сочетания PARP с ингибиторами ATR или с медьсодержащим лечением, что указывает на то, что богатый запас строительных блоков ДНК помогает опухолям выдерживать в противном случае летальное повреждение ДНК.
Атака на метаболическую слабость
Команда затем проверила, можно ли закрыть этот путь ухода, блокируя поставку пиримидинов. Они использовали BAY‑2402234, экспериментальный ингибитор DHODH — ключевого фермента de novo синтеза пиримидинов. В клеточных линиях рака яичников и органоидах, полученных от пациентов, добавление ингибитора DHODH восстанавливало чувствительность к сочетанию PARP с ингибированием ATR или к медьсодержащей терапии, уничтожая ранее устойчивые клетки. В мышиных опухолях и в восьми моделях ксенотрансплантатов, полученных от пациентов, опухоли, резистентные к одному только PARP — и даже к PARP в сочетании с блокадой ATR или меди — демонстрировали сильное подавление роста при одновременном блокировании синтеза пиримидинов. Опухоли с изначально высокими уровнями пиримидинных метаболитов были труднее поддаваемы лечению на основе PARP, но отвечали на терапию при таргетировании этого метаболического пути.
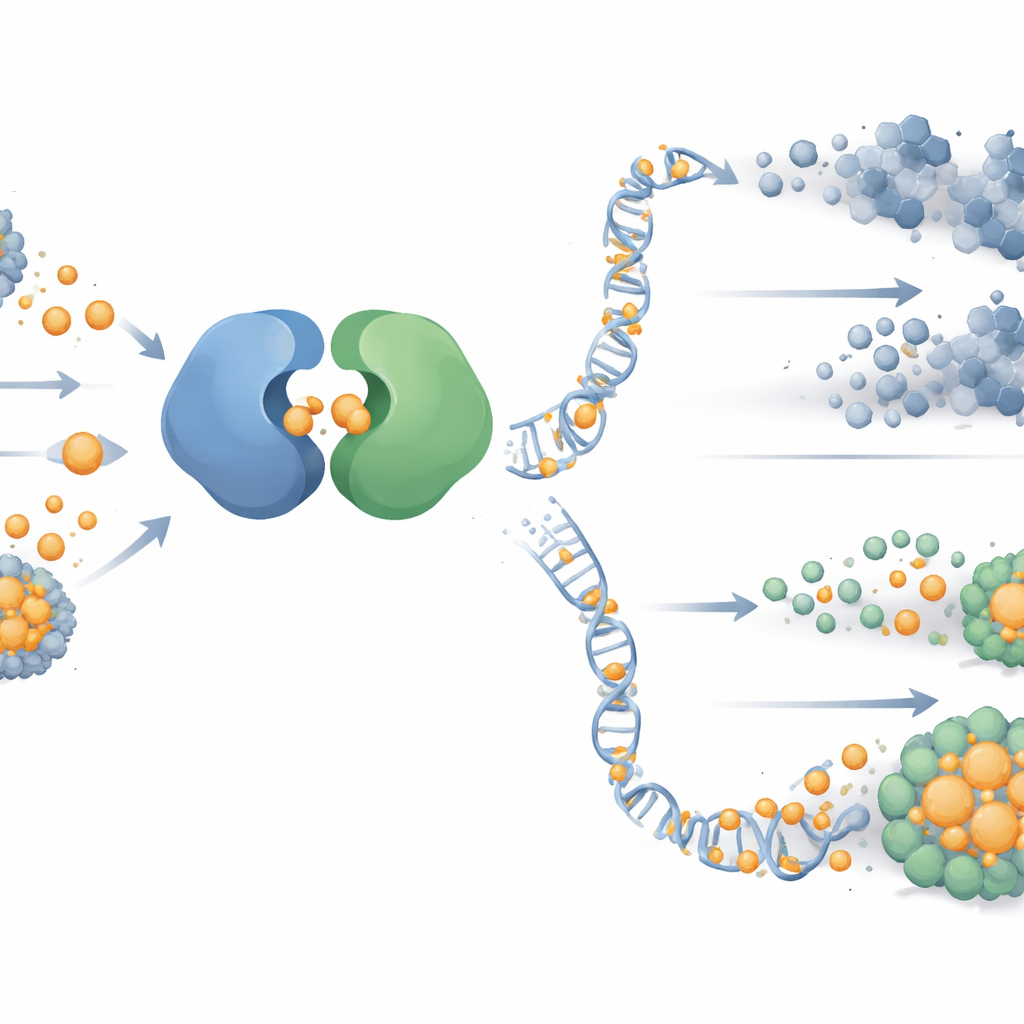
Что это может означать для пациентов
Исследование выявляет две связанные уязвимости при раке яичников, резистентном к ингибиторам PARP. Во‑первых, медь может выступать как точный инструмент для дезактивации ключевого переключателя ремонта ДНК — ATR — путем разрыва его взаимодействия с ATRIP, делая стандартные препараты, направленные на ДНК, более эффективными. Во‑вторых, опухоли, которые адаптируются путем наращивания производства пиримидинов, становятся зависимы от этого метаболического маршрута, и его блокада может вновь сделать их чувствительными к лечению. На практике эти результаты обосновывают персонализированные комбинированные подходы: ингибиторы PARP в паре с агентами, нацеленными на ATR, для опухолей с низкой зависимостью от пиримидинов, и тройная терапия с добавлением ингибитора синтеза пиримидинов для опухолей, метаболически подготовленных к сопротивлению. Хотя необходимы дальнейшие клинические испытания, работа прокладывает более понятную дорогу к преодолению одной из самых сложных форм лекарственной резистентности при раке яичников.
Цитирование: Nan, Y., Wang, K., Hu, M. et al. Targeting de novo pyrimidine synthesis confers vulnerability to copper-mediated ATR inactivation in PARP inhibitor-resistant ovarian cancer. Nat Commun 17, 3142 (2026). https://doi.org/10.1038/s41467-026-70001-5
Ключевые слова: рак яичников, ингибиторы PARP, терапия медью, репарация ДНК, метаболизм пиримидинов