Clear Sky Science · ru
Хиральные пептидогликановые мимики нацеливаются на синтез бактериальной стенки для вмешательства в деятельность патогенов
Новый способ охоты на вредные микробы
Инфекции, устойчивые к антибиотикам, растут во всем мире, однако у врачей по‑прежнему мало средств, способных точно обнаруживать и атаковать опасные бактерии, не повреждая наши клетки. В этом исследовании представлен хитрый молекулярный «приманка», имитирующая ключевой строительный блок бактериальной клеточной стенки. Эти специально разработанные молекулы могут как подсвечивать очаги инфекции для визуализации, так и доставлять антибиотики прямо к микроорганизмам, предлагая новую стратегию борьбы с трудноизлечимыми патогенами.
Имитируя бактериственную броню
Бактерии окружены прочной сетью — клеточной стенкой, состоящей из сахаров и необычных зеркальных аминокислот, которые в основном не используются нашими клетками. Исследователи воспользовались этим различием, создав длинные сахарные цепочки, украшенные специфической зеркальной формой аланина — распространённой аминокислоты. Эти цепочки, называемые хиральными пептидогликановыми мимиками, спроектированы так, чтобы близко напоминать природные компоненты, которые бактерии используют для построения стенки, но отсутствуют в тканях млекопитающих. Тонко регулируя количество присоединённого D‑аланина, команда получила варианты, которые значительно предпочитают бактерии перед клетками человека.
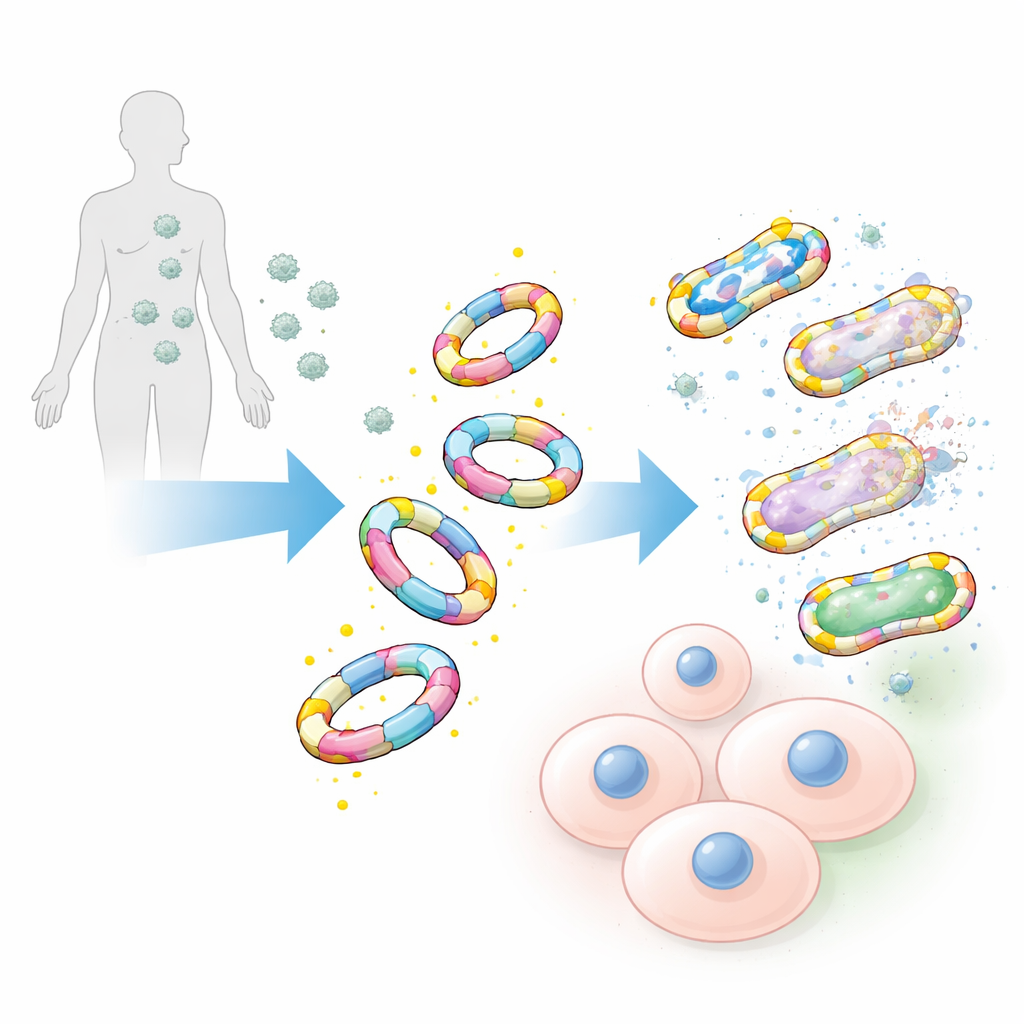
Прицеливание на бактерии, а не на наши клетки
При испытаниях против широкого круга патогенов, включая печально известные больничные штаммы, такие как метициллин‑устойчивый Staphylococcus aureus, и другие представители группы ESKAPE, мимики с D‑аланином связывались с поверхностью бактерий с поразительной эффективностью. Их зеркальные аналоги на основе L‑формы аланина, а также исходные сахарные цепочки в одиночку демонстрировали лишь слабое или пренебрежимо малое связывание. Команда также сравнила эти крупные мимики с традиционными малыми химическими зондами на базе одиночных молекул D‑аланина. Даже при том, что малые зонды сделали очень яркими, они по‑прежнему маркировали гораздо меньше бактерий и давали более слабые сигналы, что подчёркивает преимущества более крупной, более правдоподобной конструкции.
Перехват конвейера сборки клеточной стенки
Чтобы понять, как происходит столь сильное распознавание, учёные изучили взаимодействие мимиков с машиной сборки бактериальной стенки. Они обнаружили, что D‑аланиновые цепочки не просто прилипают снаружи; их захватывают как будто это настоящие строительные блоки и вводят в те же ферментативные стадии, которые обычно соединяют компоненты стенки. Химический анализ выявил новые промежуточные молекулы, возникающие только в присутствии этих мимиков, а компьютерные симуляции показали, что ключевые ферменты сборки стенки хватают мимики ещё плотнее, чем природные субстраты. В ходе нескольких циклов роста бактерий мимики накапливались в стенке, постепенно искажая её структуру и делая её проницаемой.
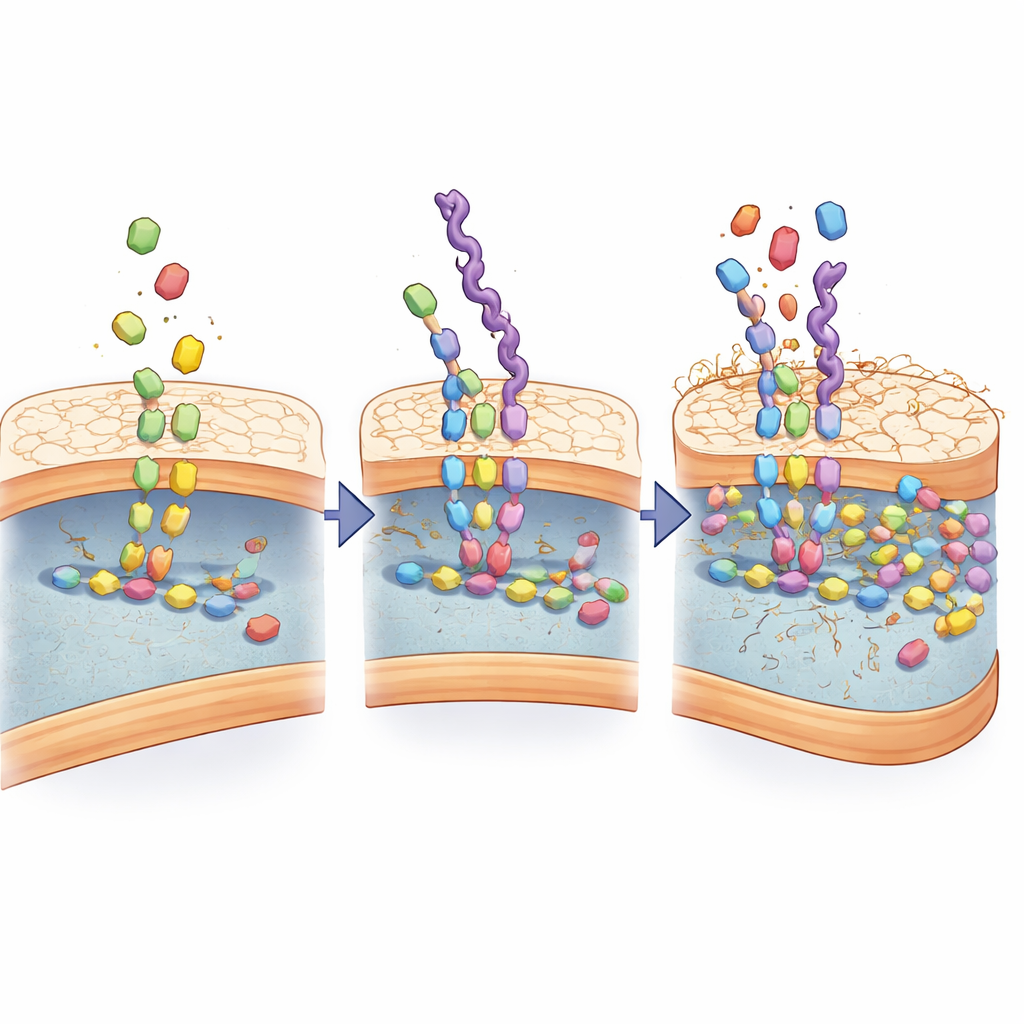
Преобразование мимиков в интеллектуальные носители лекарств
Поскольку эти цепочки естественным образом собираются в крошечные частицы в воде и несут множество химических участков для связывания, команда использовала их в качестве каркасов для красителей и антибиотиков. Флуоресцентные версии чётко обрисовывали бактерии в клеточных культурах, при этом практически не взаимодействуя с выращенными рядом клетками млекопитающих. Затем исследователи загрузили антибиотик тетрациклин в частицы на основе мимиков. В лабораторных тестах такая упаковка сделала тетрациклин в несколько раз более эффективным, убивая даже устойчивые штаммы при гораздо меньших дозах по сравнению со свободным препаратом. Микроскопия показала, что загруженные антибиотиком мимики скапливались на бактериях, проникали в их оболочки и вызывали обширную гибель клеток в сравнении с нетаргетированными формами.
Борьба с инфекциями внутри организма
Самые требовательные испытания проводились на мышиных моделях локализованных ран и жизнеугрожающих абдоминальных инфекций. В инфицированных ранах флуоресцентные мимики устремлялись к бактериям, расположенным глубоко в ткани, и при переносе тетрациклина почти полностью очищали очаги микробов. Это приводило к ускорению заживления, образованию более толстой новой кожи, более упорядоченной депозиции коллагена и более интенсивному росту мелких сосудов. В моделях системных инфекций мимики накапливались специально в инфицированных органах, таких как селезёнка и лёгкие, где при загрузке антибиотиком они резко снижали число бактерий. Важно, что высокие дозы самих мимиков показали хорошую безопасность — без очевидного повреждения основных органов или нарушений в биохимии крови.
Что это может значить для будущих методов лечения
Создав близкий химический двойник ингредиентов бактериальной клеточной стенки, эта работа демонстрирует новый способ «вписаться» в метаболизм патогена вместо того, чтобы просто атаковать его снаружи. Эти хиральные мимики служат одновременно высокоточными маяками для визуализации и умными транспортными средствами, которые направляют антибиотики непосредственно к их микробным целям, включая устойчивые штаммы, щадя при этом клетки млекопитающих. Если такие биомиметические платформы будут переведены в клинику, они могут помочь врачам точно увидеть, где прячутся инфекции, и лечить их эффективнее при более низких дозах препаратов, предлагая многообещающее средство в борьбе с растущей проблемой антимикробной резистентности.
Цитирование: Deng, K., Zou, D., Zeng, Z. et al. Chiral peptidoglycan mimics target bacterial wall biosynthesis for pathogen intervention. Nat Commun 17, 3258 (2026). https://doi.org/10.1038/s41467-026-69967-z
Ключевые слова: устойчивость к антибиотикам, бактериальная клеточная стенка, целевые доставки лекарств, молекулярная визуализация, наномедицина