Clear Sky Science · ru
Мультимодальное расслоение клеточно-типоспецифичной патологии TDP-43 в моторной коре
Почему это исследование важно для людей
Боковой амиотрофический склероз (БАС) и лобно‑височная деменция (ЛВД) — разрушительные заболевания мозга, которые лишают людей способности двигаться, говорить и сохранять черты личности. У большинства пациентов с БАС и у многих с ЛВД есть общая микроскопическая черта: скопления белка TDP-43 в тех местах, где его быть не должно. В этом исследовании задаются два практических вопроса с большими последствиями для будущих терапий: какие именно клетки мозга страдают сильнее всего от нарушений TDP-43 и что именно в них идет неправильно на уровне регуляции ДНК и активности генов?
Отслеживание повреждений в центре управления движением
Исследователи сосредоточились на первичной моторной коре — полосе ткани мозга, контролирующей произвольные движения. Используя посмертно пожертвованные образцы мозга людей с БАС, БАС‑ЛВД и неврологически здоровых доноров, они выделяли отдельные ядра клеток и измеряли одновременно, какие гены активны и насколько открыта местная хроматиновая структура. Такой «мультиомный» подход, примененный к более чем 180 000 ядрам, позволил рассортировать клетки по точным типам: несколько классов возбуждающих и ингибирующих нейронов, а также клетки‑опоры — астроциты, олигодендроциты и микроглия. Затем эти данные сопоставили с пространственными картами экспрессии генов из другого набора человеческих данных, чтобы вернуть типы клеток в знакомую слоистую структуру коры.
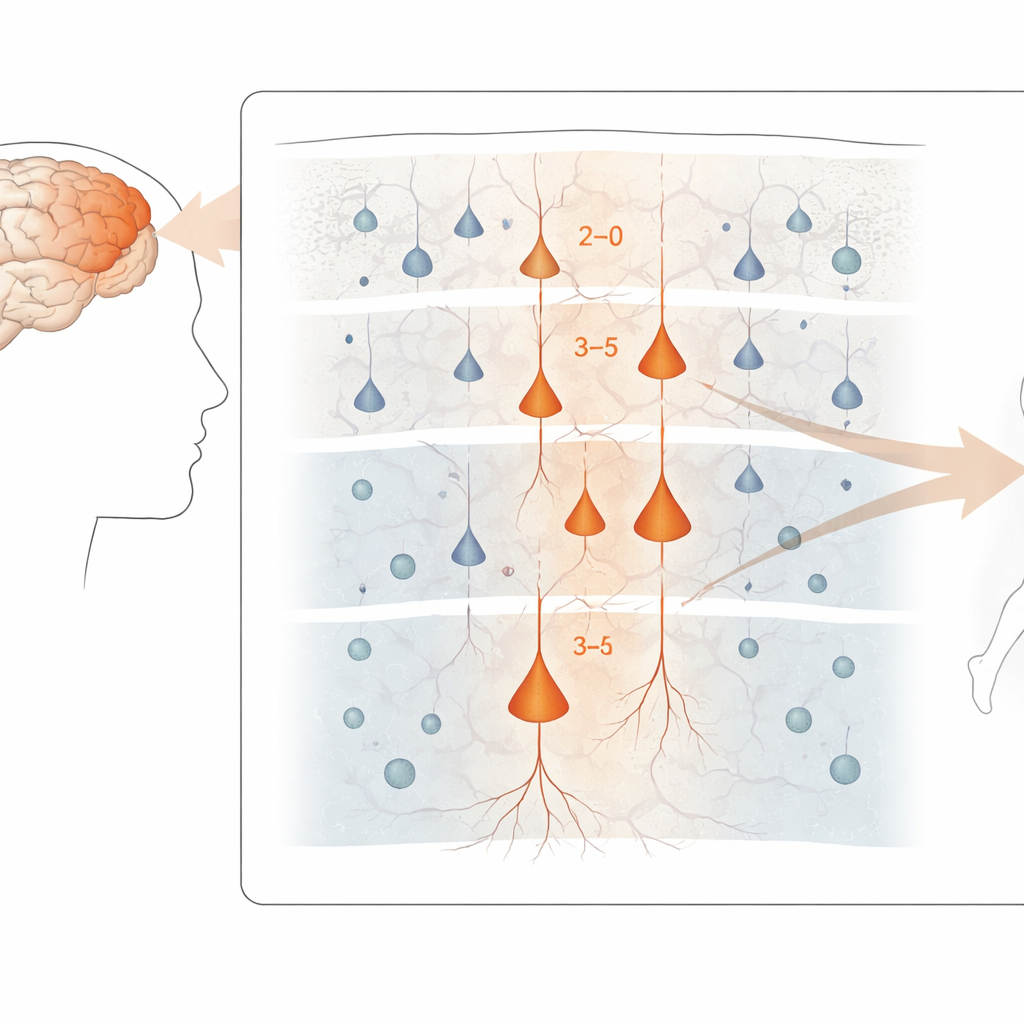
Выявление наиболее уязвимых нейронов
По всей моторной коре наиболее выраженные изменения, связанные с болезнью, наблюдались в возбуждающих нейронах — клетках, которые продвигают активность вдоль мозговых цепей. В частности, нейроны верхних и средних слоев, соединяющиеся внутри коры, а также некоторые глубокослойные клетки, посылающие сигналы за пределы коры — включая крупные «клетки Бец» (Betz), контролирующие спинальные моторные нейроны — демонстрировали самые выраженные изменения. Напротив, ингибирующие интернейроны и многие глиальные клетки в меньшей степени затрагивались на уровне экспрессии генов, хотя у некоторых из них отмечались более тонкие сдвиги. Несмотря на этот молекулярный хаос, общий состав основных типов клеток в ткани оказался удивительно схож у пациентов и контролей, что указывает на то, что ущерб больше связан с нарушением функции клеток, а не только с их гибелью.
Как TDP-43 перестраивает активность генов изнутри
Чтобы отделить эффекты, напрямую вызванные TDP-43, от других патологических процессов, команда применила умную стратегию сортировки. Они мечтали ядра антителами к TDP-43 и нейрональному маркеру, а затем с помощью проточной цитометрии разделили нейроны, чьи ядра утратили TDP-43 (признак патологии), от тех, кто его сохранил. Секвенирование более 12 000 таких ядер показало, что потеря TDP-43 происходит подавляюще в возбуждающих нейронах, особенно в определенных подтипах слоев 2–3, 3–5, 5 и 6. В этих уязвимых нейронах сотни генов были неправильно регламентированы, включая многие уже связанные с БАС. Классические молекулярные признаки дисфункции TDP-43 — например, появление «криптических» дополнительных фрагментов в транскриптах STMN2 и KALRN и смещения в местах среза и полиаденилирования РНК — были явно обогащены в ядрах, лишенных TDP-43.
Эпигенетическое ремоделирование: не все изменения вызваны TDP-43
Поскольку авторы измеряли одновременно активность генов и открытость хроматина в одних и тех же ядрах, они смогли выяснить, какие изменения связаны со сдвигами в упаковке ДНК. Они обнаружили десятки тысяч участков в геноме, где локальная доступность хроматина коррелировала с экспрессией генов. Многие из генов, измененных при БАС и БАС‑ЛВД, находились в таких регионах, что указывает на то, что часть сигнатуры болезни отражает более широкое эпигенетическое ремоделирование, а не прямые последствия утраты TDP-43. Интересно, что эти связанные с хроматином изменения часто сходились на сигнальных путях, вовлеченных в клеточную коммуникацию и направляющие механизмы аксонов, и они были особенно сильны в определенных возбуждающих нейронах и олигодендроцитах. При сравнении изменений экспрессии, связанных с патологией TDP-43, и изменений, связанных со сдвигами хроматина, исследователи выявили частичное совпадение, но в целом это были разные уровни нарушения.
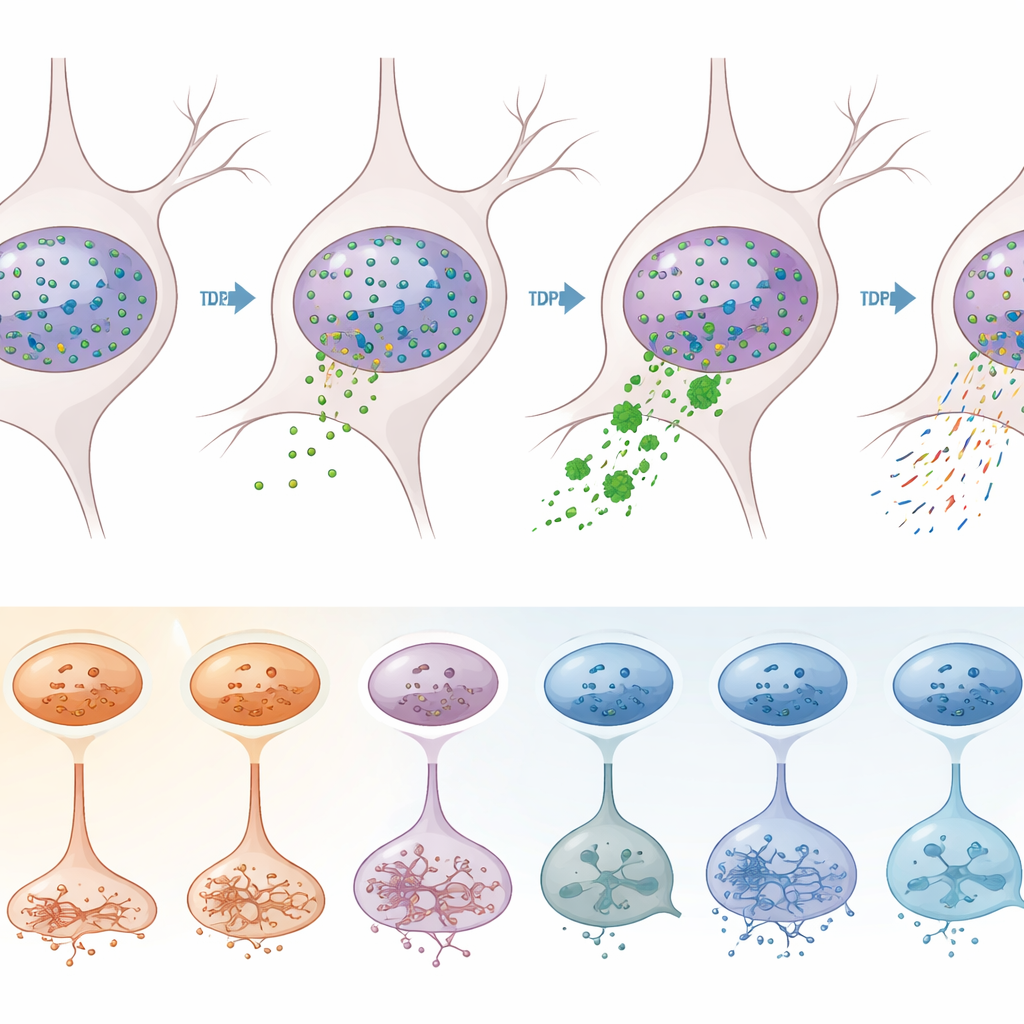
Что это означает для будущих терапий
Для неспециалиста ключевая мысль заключается в том, что БАС и БАС‑ЛВД не поражают моторную кору равномерно. Вместо этого они атакуют определенные типы возбуждающих нейронов и, в меньшей степени, некоторые клетки‑опоры, изменяя их генетические программы такими способами, которые зависят как от неисправного поведения TDP-43, так и от более широких изменений в упаковке и чтении ДНК. Эти результаты указывают на то, что эффективные терапии, вероятно, должны быть как клеточно‑типоспецифичными, так и нацеливаться на конкретные пути — например, восстановление функции TDP-43 или исправление его ошибок сплайсинга в наиболее уязвимых нейронах при параллельной коррекции эпигенетических и сигнальных изменений, общих для нескольких типов клеток. Детальная карта этого сложного ландшафта, представленная в исследовании, служит чертежом для разработки более точных вмешательств, направленных на замедление или предотвращение утраты контроля над движением при БАС и БАС‑ЛВД.
Цитирование: Ruf, W.P., Kühlwein, J.K., Meier, L. et al. Multi-modal dissection of cell-type specific TDP-43 pathology in the motor cortex. Nat Commun 17, 2406 (2026). https://doi.org/10.1038/s41467-026-69944-6
Ключевые слова: БАС, лобно-височная деменция, TDP-43, нейроны моторной коры, single-nucleus multiomics