Clear Sky Science · ru
Клеткам Th17 требуется датчик повреждений ДНК xeroderma pigmentosum группы C для контроля окислительных повреждений ДНК в модели на мышах
Сторожа наших иммунных защитников
Т-хелперы 17 типа, или клетки Th17, — это особый тип белых кровяных клеток, патрулирующих барьеры организма, такие как кишечник и кожа, чтобы отражать бактерии и грибы. Но они также участвуют в аутоиммунных заболеваниях, когда их ответы выходят из-под контроля. В этом исследовании задают на первый взгляд простейший вопрос: как эти высокоактивные клетки защищают собственную ДНК от химического стресса, который они сами создают при борьбе с инфекцией? Ответ сосредоточен вокруг сенсора повреждений ДНК, называемого XPC, наиболее известного своей ролью в защите кожных клеток от воздействия солнечного света. Здесь исследователи показывают, что XPC также критичен для поддержания Th17 клеток здоровыми, энергичными и эффективными.
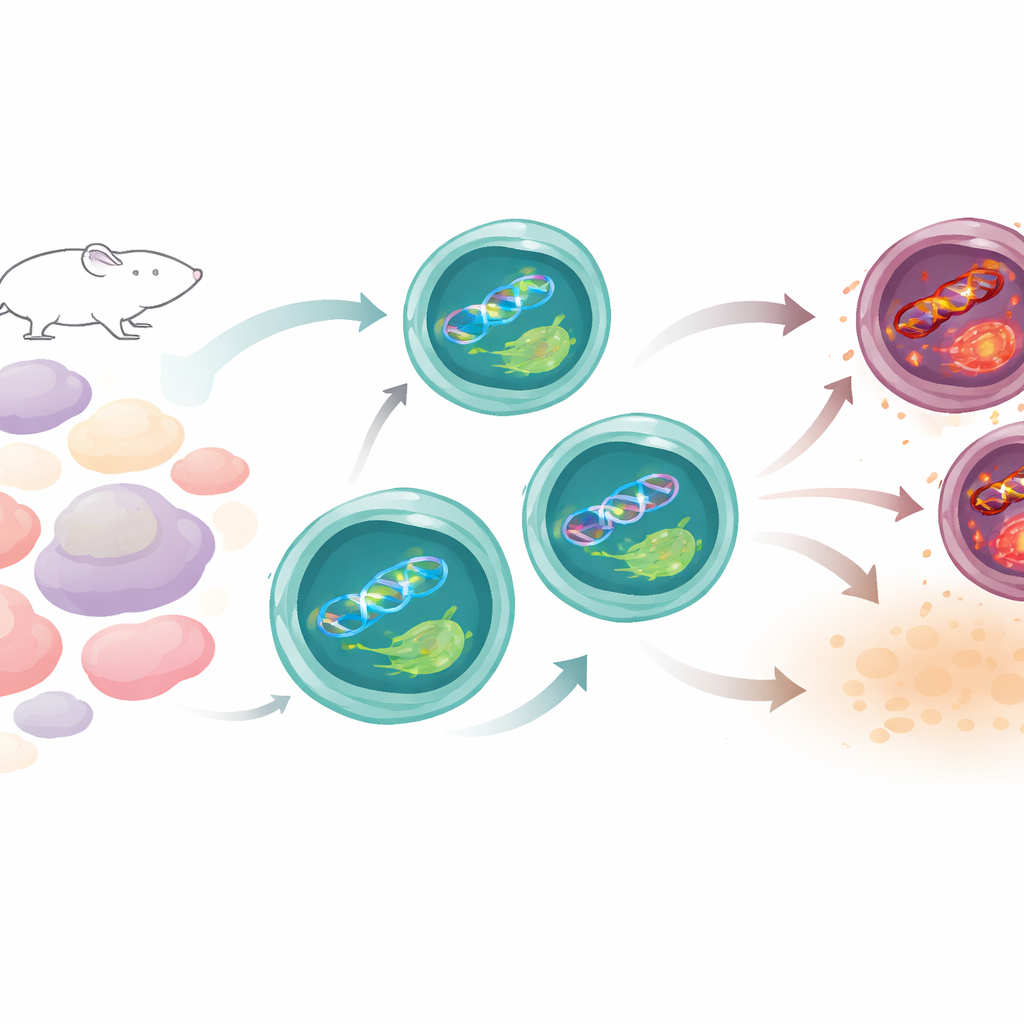
Как Th17-клетки обычно сохраняют равновесие
Жизнь Th17-клеток опасна. Чтобы функционировать, они усиливают свой метаболизм и производят реактивные формы кислорода — химически активные молекулы, которые могут повреждать ДНК. Команда сравнила Th17-клетки с другими типами Т-клеток у мышей и обнаружила, что, несмотря на высокую активность, Th17-накапливают меньше повреждений ДНК, чем многие их «родственники». Важной подсказкой стало то, что гены, участвующие в ремонте ДНК, особенно из пути, обычно исправляющего повреждения, вызванные солнцем, были сильнее активированы в Th17-клетках. Среди них оказался XPC — белок, сканирующий ДНК в поисках структурных повреждений. По мере созревания Th17 уровень XPC рос и локализовался в местах повреждений в ядре, что предполагает его постоянное патрулирование для поддержания генетической целостности.
Что происходит, когда датчика повреждений ДНК нет
Чтобы выяснить, насколько важен XPC, исследователи использовали мышей, генетически лишённых этого белка. На первый взгляд их иммунная система выглядела в целом нормальной: общее число Т-клеток и многие подтипы не изменились. Но при фокусировке на Th17 выявился заметный дефект. Без XPC значительно меньше клеток продуцировали характерную молекулу Th17 — IL-17, а ключевые маркеры идентичности и сигнальные переключатели, запускающие программу Th17, были подавлены. В культурах на чашках Петри наивные Т-клетки из этих мышей с трудом превращались в полноценные Th17-клетки. В стандартной модели, где переданные Т-клетки вызывают воспаление кишечника, T-клетки, лишённые XPC, не вызывали колита, что отражает ослабленную воспалительную способность. Одновременно регуляторные Т-клетки, которые смягчают иммунные ответы, становились более многочисленными, намекая на смещение равновесия между атакой и сдерживанием.
Повреждение ДНК, энергетические фабрики и химический стресс
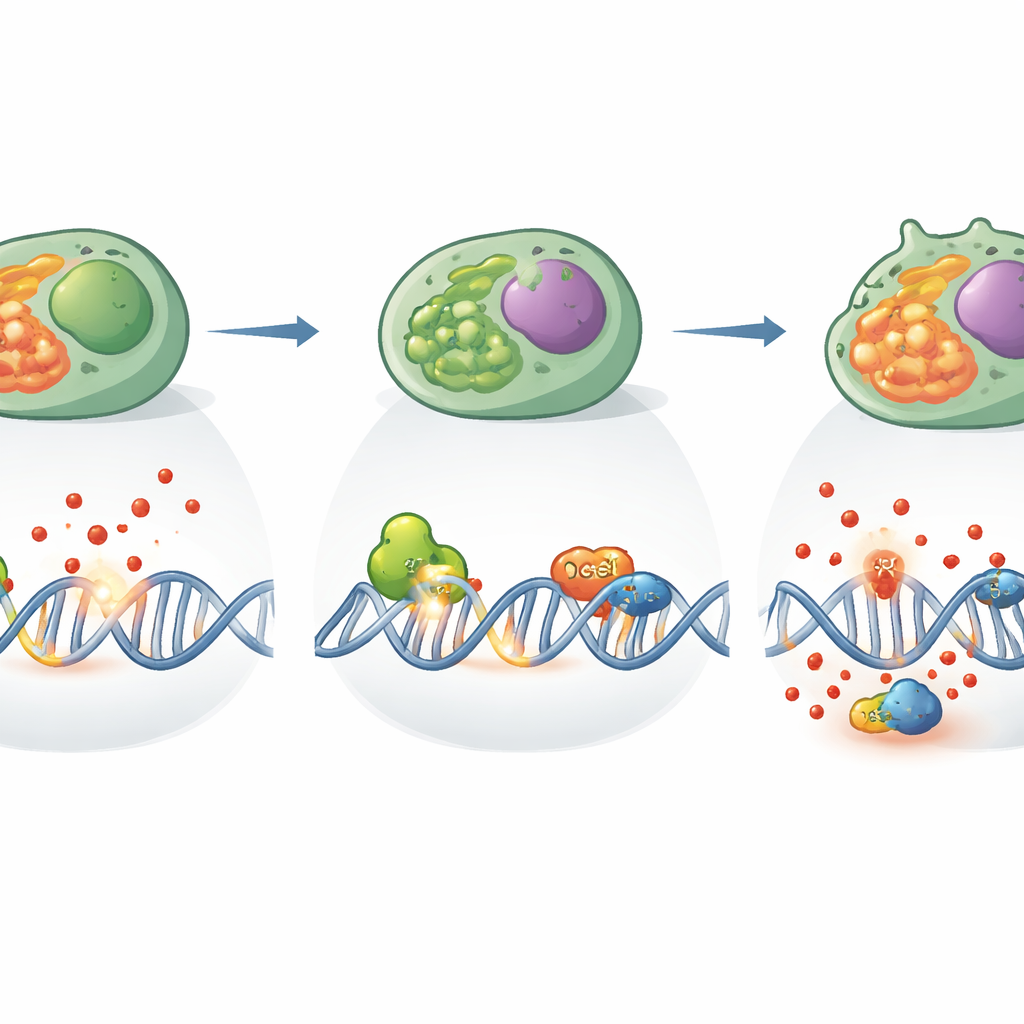
Глубже изучив явление, команда обнаружила, что у Th17-клеток без XPC было больше разрывов цепей ДНК и больше окислённых оснований ДНК — признаки атаки реактивными формами кислорода. Гены, которые обычно обнаруживают повреждение ДНК и останавливают клеточный цикл, также были снижены, что свидетельствует о ослабленной системе тревоги. Энергетический метаболизм клеток изменился: они утратили часть способности использовать быстро сгорающие пути переработки сахаров и стали более зависимыми от митохондрий — крошечных электростанций внутри клетки. Тем не менее эти митохондрии утечали больше реактивных форм кислорода и демонстрировали признаки перегрузки, создавая порочный круг нарастающего химического стресса и роста повреждений ДНК. Примечательно, что лечение клеток антиоксидантом восстановило продукцию IL-17 и уменьшило повреждения ДНК, напрямую связав окислительный стресс с выявленной функциональной дефективностью.
Командная работа при ремонте повреждённой ДНК
Помимо своей классической роли, XPC также работал в связке с другим белком репарации — OGG1, который распознаёт распространённое окисленное основание ДНК. Исследователи показали, что эти два белка физически ассоциируются в Th17-клетках, помогая координировать удаление повреждённых оснований. Когда XPC отсутствовал, активность разреза OGG1 фактически возросла, словно пытаясь компенсировать избыток повреждений. Но эта гиперактивность происходила на фоне высокого окислительного стресса и нарушенных ремонтных сетей, и её было недостаточно, чтобы восстановить нормальную функцию Th17. Генетический и структурный анализы указывали, что XPC действует как узел, соединяющий разные пути репарации и редокс-контроль, обеспечивая, чтобы повреждения не только обнаруживались, но и обрабатывались таким образом, чтобы клетка могла продолжать делиться и производить защитные молекулы.
Почему это важно для болезней и терапии
Для неспециалиста ключевая мысль такова: иммунным клеткам нужны собственные телохранители, чтобы оставаться в форме, пока они нас защищают. Исследование демонстрирует, что XPC, ранее известный защитой кожных клеток от УФ-излучения, также является жизненно важным хранителем Th17-клеток, сохраняя их ДНК целой и энергетические системы в равновесии при окислительном стрессе. Когда XPC отсутствует, Th17-клетки становятся генетически и метаболически уязвимыми, производят меньше воспалительных молекул и могут смещать иммунный баланс в сторону регуляции, а не атаки. Поскольку Th17-клетки центральны при таких состояниях, как воспалительные заболевания кишечника, псориаз и рассеянный склероз, пути, контролируемые XPC, могут стать новыми целями для тонкой настройки иммунных ответов — как для успокоения вредного воспаления, так и для усиления защиты там, где она недостаточна, путем модуляции того, как эти клетки ремонтируют ДНК и справляются с окислительным стрессом.
Цитирование: Leite, J.A., Bos, N.N., Menezes-Silva, L. et al. Th17 cells require the DNA repair sensor xeroderma pigmentosum complementation Group C to control oxidative DNA damage in a murine model. Nat Commun 17, 3157 (2026). https://doi.org/10.1038/s41467-026-69914-y
Ключевые слова: Клетки Th17, Ремонт ДНК, Окислительный стресс, Белок XPC, Аутоиммунное заболевание