Clear Sky Science · ru
Фактор инициации эукариот eIF6 модулирует пластичность мелкоклеточной карциномы легкого через ось интегрин–FAK
Почему это исследование рака легкого важно
Мелкоклеточная карцинома легкого (SCLC) — одна из самых смертоносных форм рака легкого. Первоначально она обычно хорошо реагирует на химиотерапию, но почти всегда возвращается, быстро и агрессивно. В этом исследовании ставится ключевой вопрос: что позволяет клеткам SCLC «менять личность» и становиться устойчивыми к лекарствам, и можно ли замедлить или блокировать это изменение?
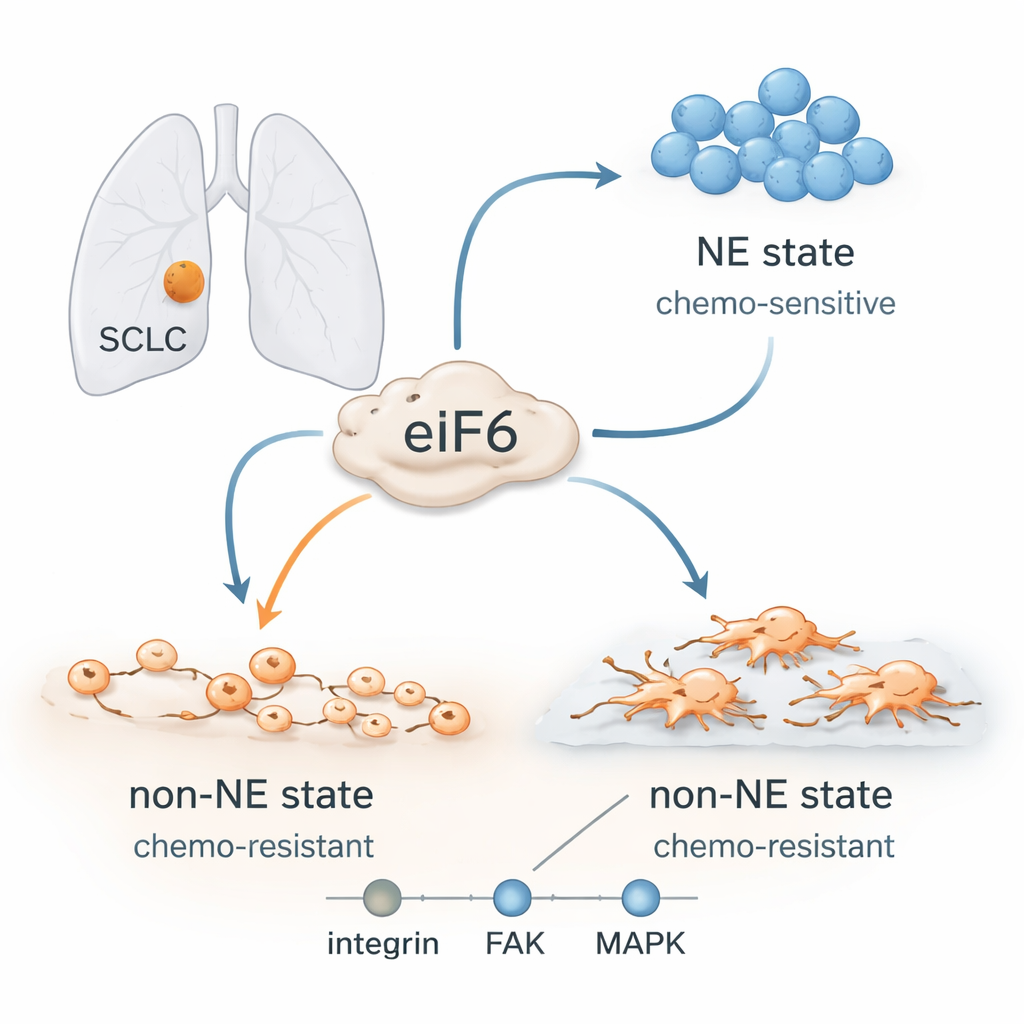
Клетки-«филлеры» — меняющие форму
Раньше врачи считали, что SCLC — однородное заболевание, но теперь ясно, что эти опухоли содержат разные типы клеток. Некоторые клетки обладают ярко выраженной «нейроэндокринной» идентичностью: они растут в плотных плавающих скоплениях, хорошо реагируют на препараты на основе платины и богаты определенными белками, похожими на нервные. Другие теряют эту идентичность и принимают «не-нейроэндокринное» состояние: они расползаются, прикрепляются к окружающей ткани, демонстрируют признаки более подвижных, инвазивных клеток и гораздо труднее поддаются лечению. Опухоли пациентов часто эволюционируют от чувствительного состояния к резистентному во время или после лечения, хотя их ДНК меняется незначительно. Это указывает на гибкие клеточные программы, а не на новые мутации, как на движущую силу рецидива.
Фактор трансляции с двойной ролью
Авторы сосредоточились на белке eIF6, наиболее известном своей ролью в сборке рибосом — фабрик по синтезу белка в клетке. Изучая образцы пациентов, мышиные модели и несколько человеческих клеточных линий SCLC, они обнаружили, что уровни eIF6 стабильно повышаются, когда клетки переходят в резистентное, не-нейроэндокринное состояние. Удивительно, но это увеличение сопровождалось общим снижением суммарного синтеза белка, что намекало на то, что eIF6 может выполнять функции, выходящие за рамки учебника. Детальные анализы прикрепления мРНК к рибосомам показали, что базовые рибосомные компоненты мало изменялись. Вместо этого был перестроен отбор и обработка сообщений для трансляции при смене идентичности клеток.
Отрыв и подключение к сигнaлам выживания
Углубившись, команда обнаружила, что в резистентных клетках часть eIF6 отрывается от рибосом и ассоциируется с поверхностным сигнальным узлом, построенным вокруг интегринов и белка, называемого фокальной адгезионной киназой (FAK). Интегрины помогают клеткам ощущать и прикрепляться к окружению; FAK передаёт эти сигналы внутрь клетки, часто активируя пути, поддерживающие подвижность, выживание и устойчивость к лекарствам. Биохимические вытягивания и внутриклеточные тесты на близость показали, что eIF6 физически взаимодействует с партнёром интегрина CD104 и с FAK, и что эти комплексы более многочисленны в не-нейроэндокринных клетках. Сборка eIF6–интегрин–FAK, в свою очередь, усиливает активность пути MAPK, хорошо известного драйвера роста и стрессоустойчивости.
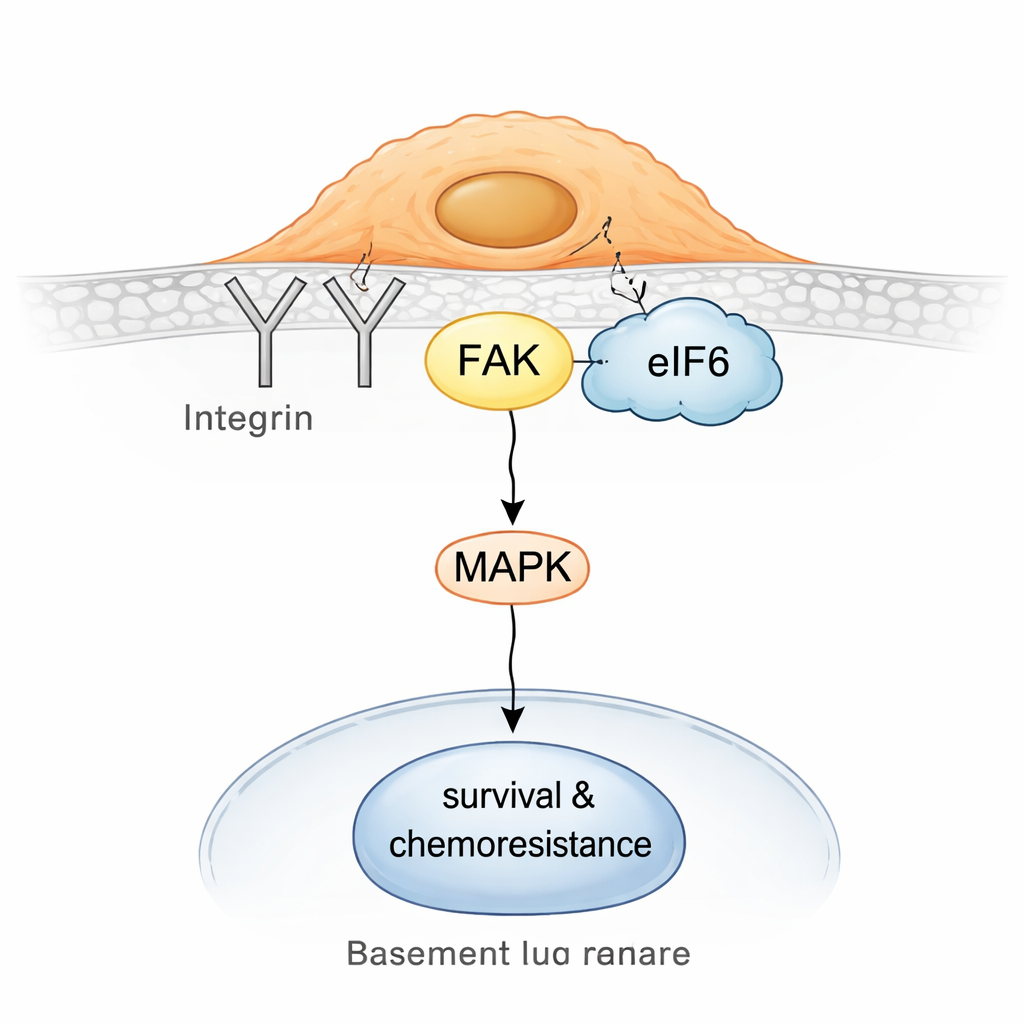
Делая резистентные опухоли снова уязвимыми
Затем исследователи проверили, может ли манипуляция eIF6 изменить поведение SCLC. При снижении уровней eIF6 в резистентных клетках гены, связанные с программой подвижности и формирования рубцов (эпителиально–мезенхимальной), были подавлены, тогда как классические нейроэндокринные гены частично восстановились. Эти изменения не полностью обращали процесс, но замедляли переход к резистентному состоянию. Важно, что клетки с пониженным eIF6 становились более чувствительными к стандартной химиотерапии карбоплатином–этопозидом в культуре и в мышиных опухолях, оставляя меньше выживших колоний и обеспечивая более стойкое сжатие опухолей. Поскольку для самого eIF6 пока нет специфических препаратов, команда протестировала ингибиторы FAK, которые уже находятся в клинической разработке. Блокирование сигнaла FAK повторно делало резистентные клетки чувствительными к химиотерапии, и у мышей комбинация лечения дала наилучший контроль опухоли.
От лабораторного открытия к будущим клиническим инструментам
Наконец, авторы проанализировали образцы опухолей пациентов с ограниченной стадией SCLC, перенёсших операцию. С помощью чувствительного метода окрашивания, который выявляет белки только когда они находятся рядом друг с другом, они измеряли, как часто eIF6 образует комплексы с CD104 или FAK внутри опухолевых клеток. Высокие уровни этих комплексов — в большей степени, чем сам eIF6 — связывались с более ранним рецидивом и сокращённой выживаемостью, что делает их перспективными прогностическими маркерами. В сумме эта работа показывает, что eIF6 может «подрабатывать» вне рибосом, помогая подключать клетки рака к мощным сигнальным контурам выживания. Отслеживание оси eIF6–интегрин–FAK предлагает пути для выявления пациентов с повышенным риском рецидива и обосновывает комбинирование ингибиторов FAK с химиотерапией для противодействия опасной пластичности SCLC.
Цитирование: Peng, H., Wang, Z., Wang, M. et al. Eukaryote initiation factor 6 modulates small-cell lung carcinoma plasticity via the integrin-FAK signaling axis. Nat Commun 17, 2048 (2026). https://doi.org/10.1038/s41467-026-69899-8
Ключевые слова: мелкоклеточный рак легкого, устойчивость к препаратам, клеточная пластичность, eIF6, сигнaling интегрин–FAK