Clear Sky Science · ru
Зависимое от контекста ингибирование трансляции как терапевтический подход при раке
Обратить фабрики белков против рака
Раковые клетки выживают, постоянно синтезируя большое количество короткоживущих «двигающих» белков, которые поддерживают их рост и деление. В этом исследовании рассматривается новый способ борьбы с раком — тонкая блокада белково‑синтезирующих машин клетки, рибосом, только когда они пытаются собрать конкретные белковые последовательности, особенно те, что встречаются в труднолекарственных онкогенах, таких как MYC. Такое селективное вмешательство может убивать опухолевые клетки, одновременно щадя большую часть нормального синтеза белков.
Как клетки строят белки — и где может случиться сбой
Каждая клетка зависит от рибосом, крошечных молекулярных фабрик, которые читают генетические сообщения (мРНК) и связывают аминокислоты в белки. Большинство существующих лекарств, направленных на рибосомы, например антибиотики или старые противоопухолевые средства, действуют грубо: они широко отключают синтез белка, что может повреждать здоровые клетки и вызывать серьезные побочные эффекты. Авторы исходили из того, что у каждой новообразуемой белковой цепочки есть уникальная последовательность и химические свойства, поэтому возможно создать малые молекулы, которые блокируют рибосому только тогда, когда в ней присутствует определённая последовательность, оставляя остальной синтез белка в клетке в значительной мере нетронутым.
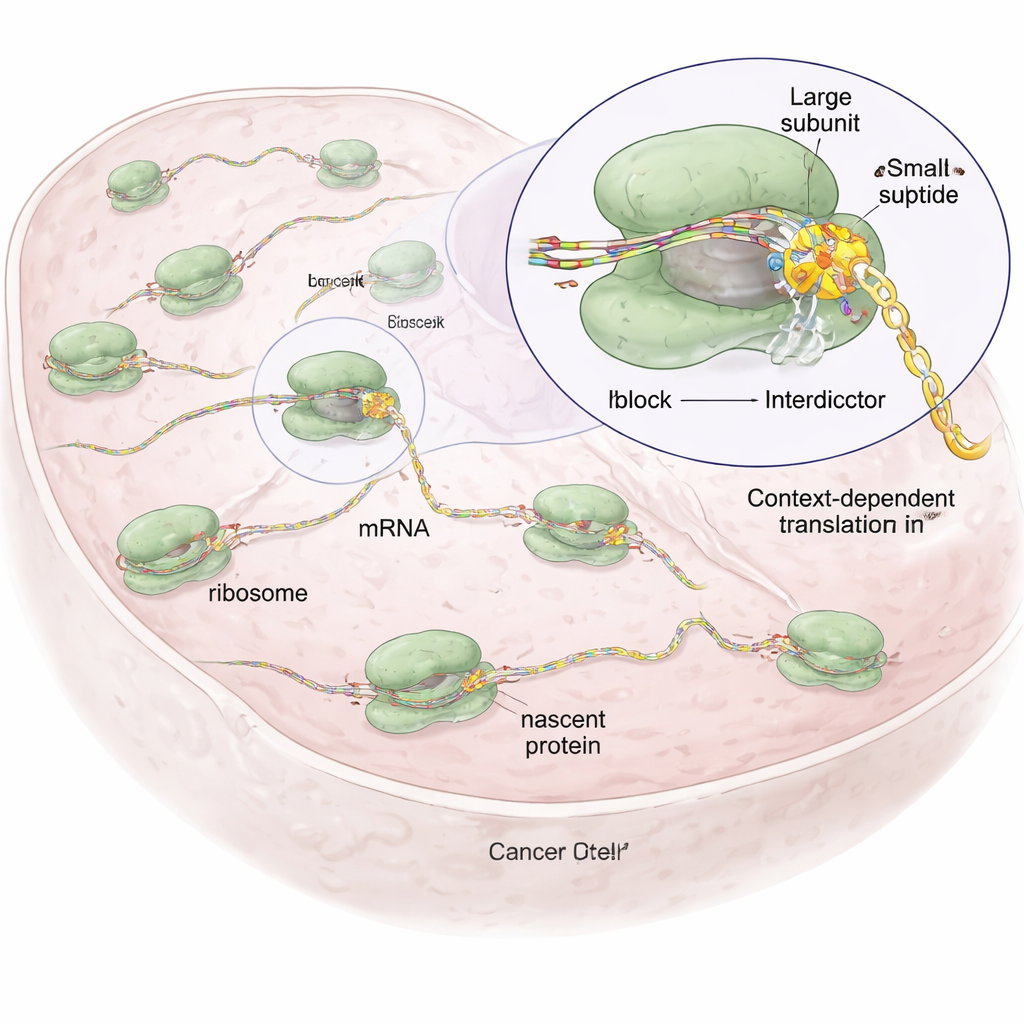
Дизайнерские молекулы, которые останавливают только определённые белковые последовательности
Опираясь на природное соединение антисомицин (anisomycin), которое связывается с каталитическим центром рибосомы, где формируются пептидные связи, исследователи создали семейство синтетических молекул, называемых «интердикторами». Все они имеют общий каркас, фиксирующий их внутри рибосомы, но различаются боковыми группами, направленными к растущей белковой цепочке. Эти боковые группы настроены на предпочтение определённых типов аминокислот — например, один интердиктор (IDB‑001) притягивается к отрицательно заряженным остаткам, тогда как другой (IDB‑002) предпочитает небольшие гидрофобные остатки. Используя метод профильного картирования рибосом (ribosome profiling), позволяющий глобально определить места пауз рибосом на мРНК в клетках, команда показала, что каждое соединение вызывает остановки на характерных коротких мотивах в нарастающей цепочке, часто на предпоследней (−1) аминокислоте, что демонстрирует действие, зависимое от последовательности, а не бесселективное подавление.
Наблюдение взаимодействия лекарства и рибосомы атом за атомом
Чтобы понять физическую основу этой селективности, авторы заморозили человеческие рибосомы в процессе трансляции заданных пептидных последовательностей и визуализировали их методом криоэлектронной микроскопии с почти атомным разрешением. Они наблюдали интердиктор в активном центре рибосомы, устанавливающий точные контакты с последними несколькими аминокислотами нарастающей цепи. В одной структуре гидрофобная боковая группа IDB‑002 уютно располагается рядом с небольшими негабаритными остатками пептида, что объясняет, почему более крупные боковые цепи там не благоприятны. В другой структуре кислый боковой остаток, происходящий из фрагмента MYC, образует сольвый мост с положительно заряженной группой на IDB‑001. Наличие препарата также смещает близлежащие основания рибосомной РНК в новые положения, которые сужают активный центр и частично препятствуют входу следующей тРНК, что помогает зафиксировать удлинение на этих предпочтительных последовательностях.
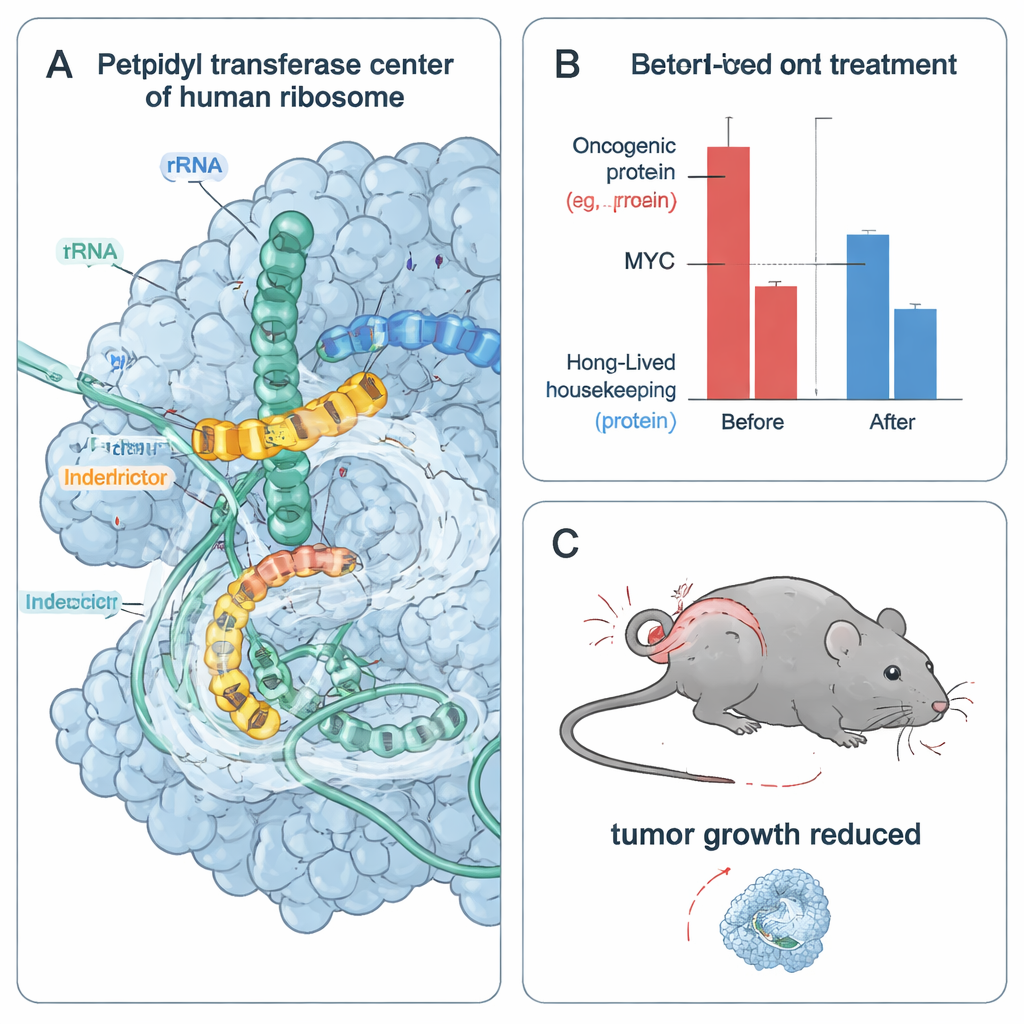
От застрявших рибосом до стрессовых и гибнущих опухолевых клеток
Поскольку быстро делящиеся раковые клетки сильно зависят от короткоживущих онкопротеинов, таких как MYC и CCND1, команда проверила воздействие интердикторов на выживаемость опухолевых клеток. В нескольких клеточных линиях, зависимых от MYC, IDB‑001 и IDB‑002 снижали жизнеспособность при наномолярных — низкомикромолярных концентрациях. Дополнительно оптимизированный аналог, IDB‑003, оказался ещё более мощным и пригодным для приема внутрь. В клетках эти соединения быстро истощали MYC и другие быстро распадающиеся онкопротеины, в то время как долгоживущие белки домашнего хозяйства оставались относительно стабильными в тот же временной интервал. Лекарства также вызывали клеточные стресс‑ответы, связанные со столкновениями рибосом, но блокирование этих сигнальных путей не устраняло потерю жизнеспособности, что указывает на то, что прямое лишение важных онкогенных белков является главным фактором гибели опухолевых клеток.
Демонстрация концепции в сложной модели рака молочной железы
Чтобы проверить работоспособность подхода у животных, авторы лечили мышей с трансплантатами человеческого тройного негативного рака молочной железы перорально вводимым IDB‑003. В течение 28 дней рост опухолей у обработанных животных был значительно замедлен по сравнению с контрольной группой, с ингибированием роста опухолей до 80% при более высоких дозах и без зарегистрированной в этом исследовании тяжелой токсичности. Анализ экспрессии генов опухолей показал сильное понижение программ генов‑мишеней MYC, что согласуется со сниженной активностью MYC in vivo. В совокупности эти результаты указывают, что селективная остановка рибосом на конкретных белковых последовательностях может ослаблять опухоли, зависящие от нестабильных онкогенных драйверов, и при этом потенциально избегать широкой токсичности классических ингибиторов трансляции.
Почему это важно для будущих методов лечения рака
Эта работа вводит новый класс малых молекул: таких, которые действуют не за счёт связывания с уже сформированным белком, а перехватывают его в процессе синтеза и только если присутствует короткая «адресная метка» последовательности. Поскольку многие протеины, способствующие раку, гибки, короткоживущи или не имеют очевидных карманов для традиционных лекарств, направленное вмешательство в их синтез на уровне рибосомы может открыть путь к лечению опухолей, вызванных ныне «нелекарственными» генами, такими как MYC. Исследование также предлагает, что путём настройки химии интердикторов будущие препараты можно будет направлять на разные последовательностные мотивы и терапевтические цели, расширяя эту стратегию за пределы онкологии на другие состояния, где подавление отдельных белков может восстановить здоровье.
Цитирование: Diamond, P.D., Sauer, P.V., Holm, M. et al. Context-dependent translation inhibition as a cancer therapeutic modality. Nat Commun 17, 1963 (2026). https://doi.org/10.1038/s41467-026-69891-2
Ключевые слова: терапия рака, направленная на рибосомы, ингибирование трансляции, опухоли, управляемые MYC, молекулы с контекст-зависимым действием, тройной негативный рак молочной железы