Clear Sky Science · ru
Радиомечение олигопептидов посредством селективного обмена изотопов водорода на дейтерий и тритий в водных буферах
Отслеживание лекарств на атомном уровне
Современные лекарства всё чаще включают сложные биологические молекулы, такие как пептиды и малые белки. Чтобы понять, куда эти препараты попадают в организме и как долго сохраняются, учёные нередко заменяют несколько обычных атомов на редкие или радиоактивные, которые можно отслеживать. В этой статье предложен метод «маркировки» пептидных препаратов такими отслеживаемыми атомами непосредственно в водных растворах, что гораздо ближе к реальным биологическим условиям, чем большинство ранних методов.
Почему важны крошечные замены атомов
Замена обычного водорода на более тяжёлые изотопы, такие как дейтерий или тритий, превращает обычные молекулы в мощные научные трассеры. Такие меченые варианты ведут себя почти так же, как исходное лекарство, но их можно отслеживать чувствительными приборами, фиксирующими массу или излучение. Для малых лекарственных молекул химики создали богатый набор методов для получения подобных меток. В отличие от этого, подходы к маркировке более крупных и хрупких биологических молекул — например пептидов и белков — редки, часто сложны и плохо приспособлены к водным средам, подобным крови или клеточной жидкости. Авторы поставили себе цель заполнить этот пробел: предложить простой и селективный способ введения дейтерия или трития в строительные блоки пептидов прямо в водных буферах.
Одношаговая стратегия метки в воде
Команда сосредоточилась на реакции, называемой обменом изотопов водорода, при которой атом водорода в молекуле меняют на более тяжёлый из аналога из газа, например дейтерия (D2) или трития (T2). Они сформировали ин ситу катализатор на основе иридия и специально подобранной фосфиновой вспомогательной молекулы. При смешении в слабо щелочном буфере и нагревании эта система активирует определённые связи C–H в аминокислотах и коротких пептидах и заменяет эти атомы водорода на дейтерий или тритий из газа. Существенно, что это выполняется в один этап, в водной среде и при очень низком содержании металла — условия, более благоприятные для деликатных пептидных лекарств и для практических лабораторных процедур. 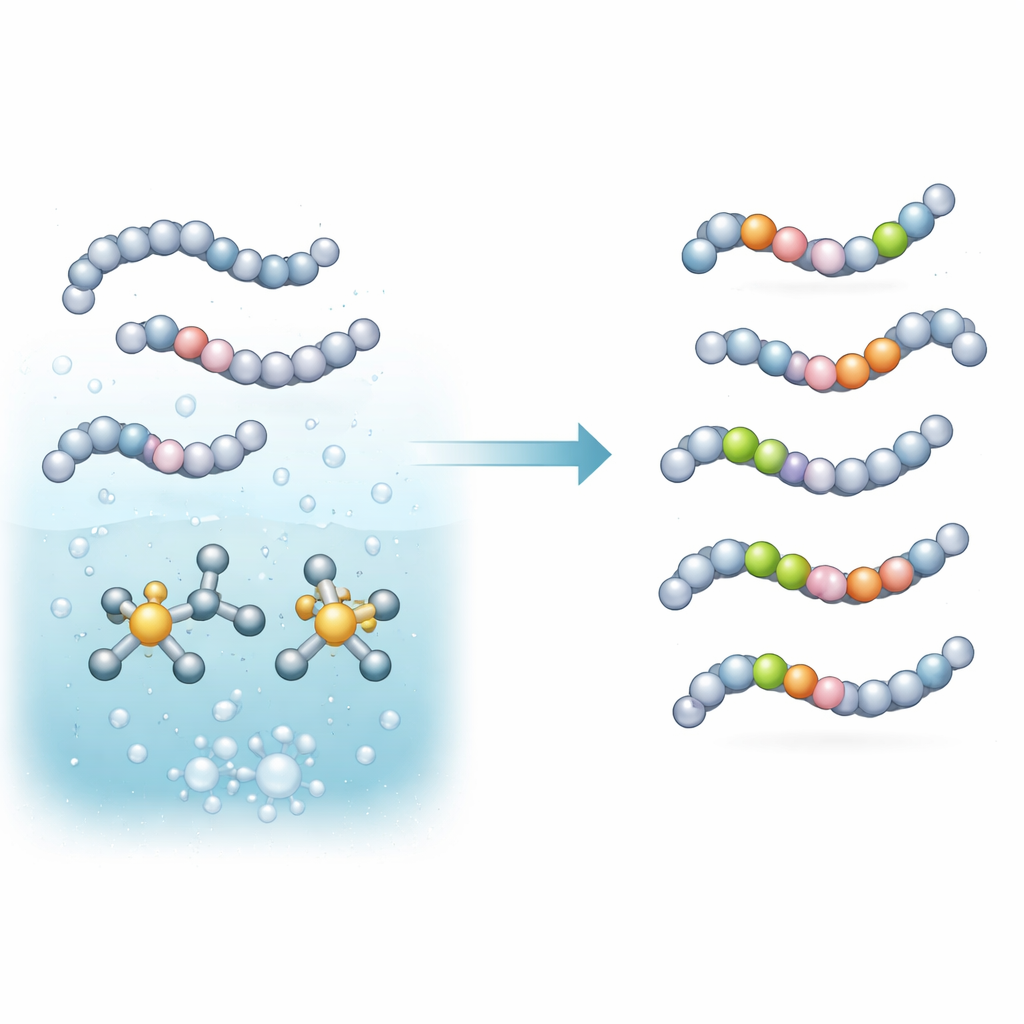
Выбор именно тех участков на пептидах
Не каждый атом водорода в пептиде одинаково полезен в качестве метки. Некоторые легко теряются в ходе метаболизма, что стирает радиоактивную «бирку». Авторы внимательно изучили, где их катализатор предпочитает действовать. Они обнаружили, что особенно хорошо подходят незашитые (незащищённые) аминокислоты, такие как лизин и аргинин. В лизине метод селективно мечет углерод в боковой цепи (так называемую гамма-позицию) — участок, который считается «неактивированным» и с большей вероятностью остаётся стабильным в организме. У аргинина наблюдается похожее поведение в близлежащих положениях боковой цепи. Испытания серии родственных молекул, включая короткие цепи с двумя аминогруппами, показали, что наличие двух азотистых центров, расположенных в нужной геометрии, помогает металлическому катализатору «захватить» молекулу и добраться до целевой C–H-связи.
Заглядывая в устройство катализатора
Чтобы понять, почему возникает такая селективность, исследователи сочетали эксперименты с детальными компьютерными моделями на основе теории функционала плотности. Эти расчёты отображают энергетический ландшафт по мере образования иридиевого комплекса из димерного прекурсора, его связывания с водой, затем с аминокислотой и, наконец, встраивания в конкретную C–H-связь. Модели показывают, что разрыв исходного иридиевого димера энергетически осуществим в воде для одного типа прекурсора, но не для близкого по строению аналога, что объясняет, почему эффективны лишь некоторые исходные комплексы. Они также показывают, что сам субстрат способствует стабилизации активного металлического центра и предотвращает его агрегацию в неактивные частицы. Наиболее благоприятный путь включает связывание аминокислоты через два атома азота, формируя «пинцетоподобный» захват, который позиционирует один C–H для обмена на дейтерий или тритий.
От простых блоков к реальным пептидным препаратам
Имея представление о механизме, команда расширила метод от отдельных аминокислот до коротких пептидов длиной до семи остатков, а затем до более сложных последовательностей, похожих на терапевтические, содержащих до 13 аминокислот. Во всех случаях метка возникала в боковых цепях лизина или аргинина на конце пептида, а сами пептиды в основном сохраняли целостность при условиях реакции. Для тритиевых меток оптимизировали процесс при низком давлении газа, чтобы безопасно добиться высокой удельной активности — т. е. высокой доли молекул, несущих по крайней мере один атом трития. Эти тритиевые пептиды были получены в одну ёмкость и готовы к использованию в качестве трассеров в in vitro и потенциально in vivo исследованиях. 
Что это значит для будущих лекарств
Работа демонстрирует, что возможно селективно присоединять дейтерий или тритий к реалистичным пептидным препаратам в простой водной одношаговой процедуре, при этом нацеливаясь на метаболически устойчивые позиции ключевых аминокислот. Для разработчиков лекарств это означает более лёгкий доступ к точно меченым трассерным версиям пептидных терапий, необходимых для измерения всасывания, распределения и метаболизма. Помимо производства трассеров, механистические выводы о взаимодействии иридиевого катализатора с аминокислотами могут вдохновить новые подходы к точной настройке того, где и как модифицируются сложные биомолекулы, открывая путь к более точному химическому контролю над будущими биологическими лекарствами.
Цитирование: Martinelli, E., Weck, R., Güssregen, S. et al. Radiolabeling of oligopeptides by selective hydrogen isotope exchange with deuterium and tritium in aqueous buffers. Nat Commun 17, 2317 (2026). https://doi.org/10.1038/s41467-026-69850-x
Ключевые слова: радиомеченые пептиды, обмен изотопов водорода, метки дейтерием и тритием, пептидные терапевтические средства, иридиевая катализация