Clear Sky Science · ru
Использование биореактора из кишечника мыши без микробов для направленной эволюции пробиотиков против неалкогольной жировой болезни печени
Почему эта история кишечника важна для вашей печени
Неалкогольная жировая болезнь печени (NAFLD) сегодня затрагивает сотни миллионов людей и тесно связана с питанием и состоянием кишечника. В этом исследовании рассматривается нестандартная идея: использовать сам кишечник как живую «фабрику» для «обучения» полезных бактерий, чтобы они становились более эффективными лекарствами. Позволяя пробиотикам эволюционировать внутри мышей без микробов на диете с высоким содержанием жиров, исследователи сформировали бактериальную линию, которая эффективнее справляется с жёлчными кислотами — молекулами, похожими на моющие вещества, которые связывают то, что мы едим, с тем, как печень хранит жир. Работа предлагает новый способ создания пробиотиков следующего поколения, настроенных на организм по‑натуральному, а не только разработанных в пробирке.
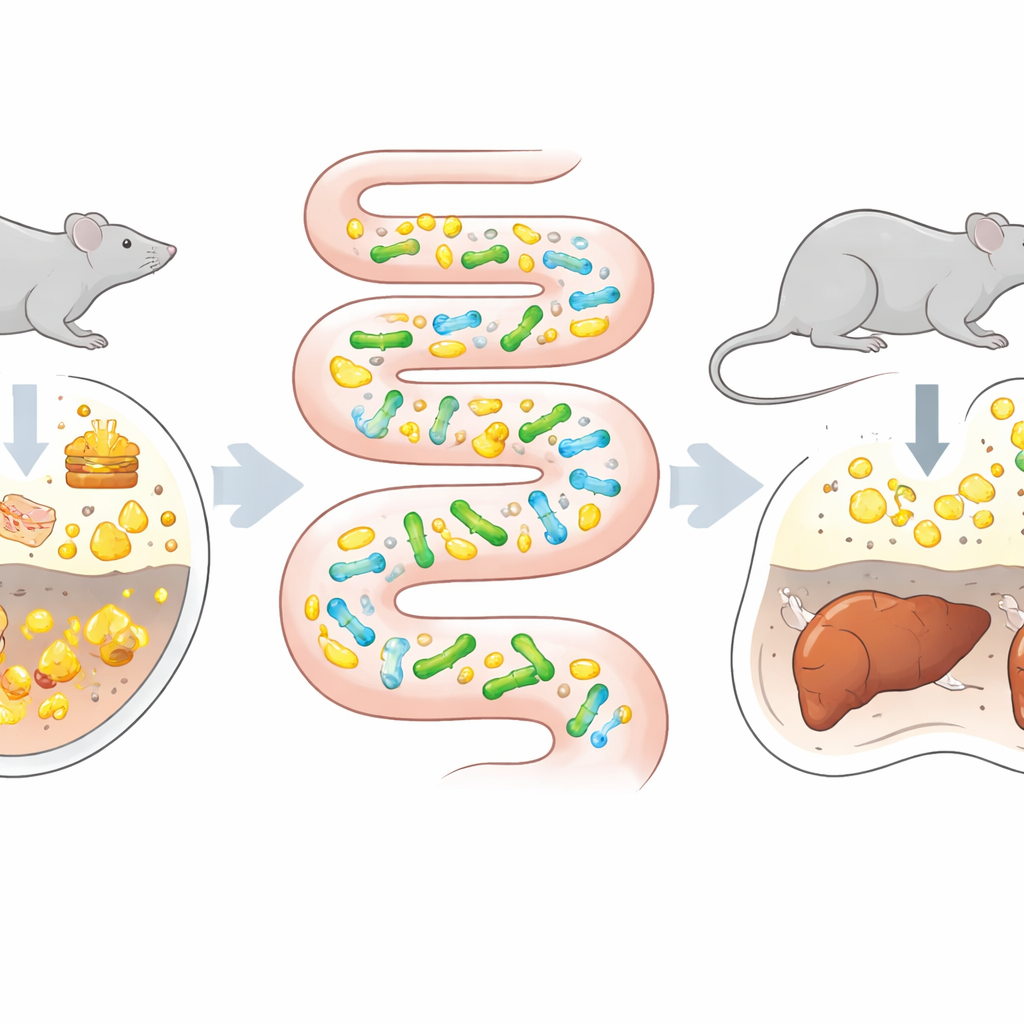
Превращение кишечника в камеру для эволюции
Традиционная направленная эволюция — индуцирование мутаций у микробов и отбор лучших вариантов — обычно проводится в лабораторных колбах. Это хорошо работает для ферментов или промышленных микроорганизмов, но часто не годится для пробиотиков, которым приходится справляться со сложной химией, иммунными сигналами и физическими факторами кишечника. Авторы задались вопросом: а что если использовать сам кишечник со всеми его естественными отборами в качестве селективной среды? Они выбрали вид пробиотика Bifidobacterium animalis subsp. lactis, который уже способен частично расщеплять жёлчные кислоты. Мышей без микробов, не несущих других микроорганизмов, колонизировали этой линией и кормили постепенно всё более жирной и богатой холестерином диетой, что известно своим эффектом повышения уровня жёлчных кислот в кишечнике. Параллельно ту же штамм направляли адаптироваться в стандартной лабораторной среде с добавлением жёлчных кислот, что позволило напрямую сравнить эволюцию in vitro и in vivo.
Кишечно‑обученный пробиотик превзошёл своего лабораторно‑обученного родственника
После многократных переносов в колбах лабораторно эволюционировавшие бактерии не показали значимого улучшения в способности перерабатывать жёлчные кислоты. В резком контрасте изоляторы, взятые из кишечников мышей на высокожировой диете, продемонстрировали широкий разброс по эффективности; примерно четверть имела явно усиленную способность разрушать жёлчные кислоты. Выделившийся вариант, названный W5S9, метаболизировал жёлчные кислоты на 77 процентов эффективнее, чем родительский штамм. Это разнообразие, а также наличие и «победителей», и «проигравших», подчеркнуло, как богатая и многогранная селекция хозяина в кишечнике не имитируется простой лабораторной средой. Это также подтвердило, что кишечник может выступать мощным «биореактором», постоянно генерируя и тестируя генетические варианты в условиях, близких к реальной жизни.
Вглядываясь в мутации, которые имеют значение
Чтобы понять, что изменилось в W5S9, команда секвенировала его геном и измерила изменения активности генов по сравнению с исходным штаммом. Среди сотен небольших различий в ДНК выделились две ключевые мутации. Одна располагалась непосредственно вверх по потоку от гена cbh, кодирующего фермент, расщепляющий желчные соли; это изменение действовало как более сильный переключатель, повышая продукцию фермента при жёлчном стрессе. Вторая мутация изменила структуру и активность транспорта‑белка (MDR), выкачивающего переработанные жёлчные кислоты из клетки. Лабораторные тесты показали, что эти изменения улучшили способность пробиотика и расщеплять конъюгированные жёлчные кислоты, и экспортировать продукты расщепления, повышая его выживаемость в суровых условиях, богатых желчью. Иными словами, эволюция внутри кишечника тонко настроила и «ножницы», и «выходную дверь» пути переработки жёлчных кислот.
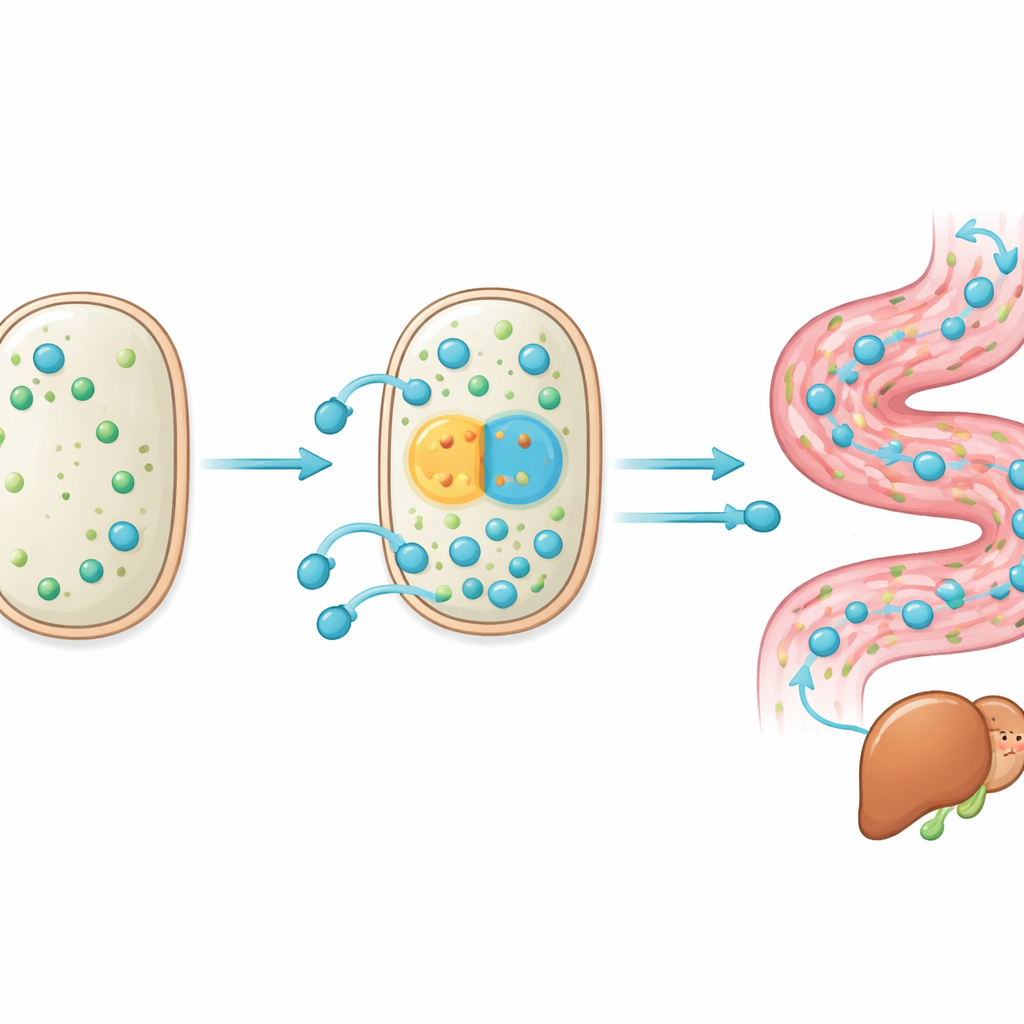
Защита жирной печени в организме под стрессом диеты
Ключевое испытание заключалось в том, сможет ли этот кишечно‑обученный штамм действительно защитить животное от повреждения печени. Исследователи использовали модель мыши NAFLD, при которой длительная диета с высоким содержанием жиров вызывает набор веса, накопление жира в печени и воспаление. Мышей разделили на четыре группы: нормальная диета, только высокожировая диета, высокожировая диета плюс исходный пробиотик и высокожировая диета плюс адаптированный штамм W5S9. Обе группы, получавшие пробиотики, показали улучшения по сравнению с группой на высокожировой диете, но W5S9 последовательно проявлял себя лучше. Эти мыши набирали меньше веса, имели более здоровые липидные профили, показывали более низкие маркеры повреждения печени и воспаления и визуально имели меньше жировых капель в тканях печени. Подробный химический анализ фекалий показал, что W5S9 сильнее снижает уровни связанных с болезнью жёлчных кислот и смещает пул жёлчных кислот в сторону более здорового баланса, не изменяя при этом радикально общий состав сообщества кишечных микробов.
Что это значит для будущих пробиотических лекарств
Для неспециалистов ключевое сообщение таково: исследователи не просто нашли «хороший» пробиотик — они использовали сам организм, чтобы вылепить более эффективный штамм. Позволив естественному отбору действовать внутри мышей без микробов в строго спроектированной среде с высоким содержанием жира и жёлчных кислот, они получили штамм, который эффективнее управляет жёлчными кислотами и, как следствие, лучше защищает печень от диет‑индуцированного повреждения. Поскольку не был добавлен чужеродный ДНК, эти эволюционировавшие микроорганизмы остаются не‑ГМО, что может упростить регуляторное одобрение и повысить общественное принятие. Более широкое значение состоит в том, что аналогичные стратегии эволюции, направляемой хозяином, могут быть адаптированы под другие состояния — от воспалительных заболеваний кишечника до метаболических и даже неврологических расстройств, открывая путь к персонализированным, функционально настроенным живым микробным терапиям.
Цитирование: Han, Z., Sun, Z., Liu, X. et al. Harnessing a germ‑free mouse gut bioreactor for directed evolution of probiotics to combat non-alcoholic fatty liver disease. Nat Commun 17, 3133 (2026). https://doi.org/10.1038/s41467-026-69823-0
Ключевые слова: пробиотики, кишечный микробиом, жёлчные кислоты, жировая болезнь печени, направленная эволюция