Clear Sky Science · ru
Холецистокинин, вырабатываемый β-клетками, способствует развитию аденокарциномы поджелудочной железы, связанной с ожирением
Когда лишний вес «разговаривает» с поджелудочной
Известно, что ожирение повышает риск рака поджелудочной железы — одного из наиболее смертельных онкологических заболеваний, — но биологическая «беседа», связывающая лишний жир с опухолями, долгое время оставалась неясной. В этом исследовании выявлен неожиданный носитель сигнала: пищеварительный гормон холецистокинин (ХЦК), который синтезируется внутри клеток поджелудочной, производящих инсулин. Проследив, как эти клетки меняются при метаболическом стрессе, авторы показывают, как гормон, предназначенный помочь организму справиться с нагрузкой, может вместо этого подпитывать рак, и предлагают новые способы перехватить болезнь на ранних этапах.
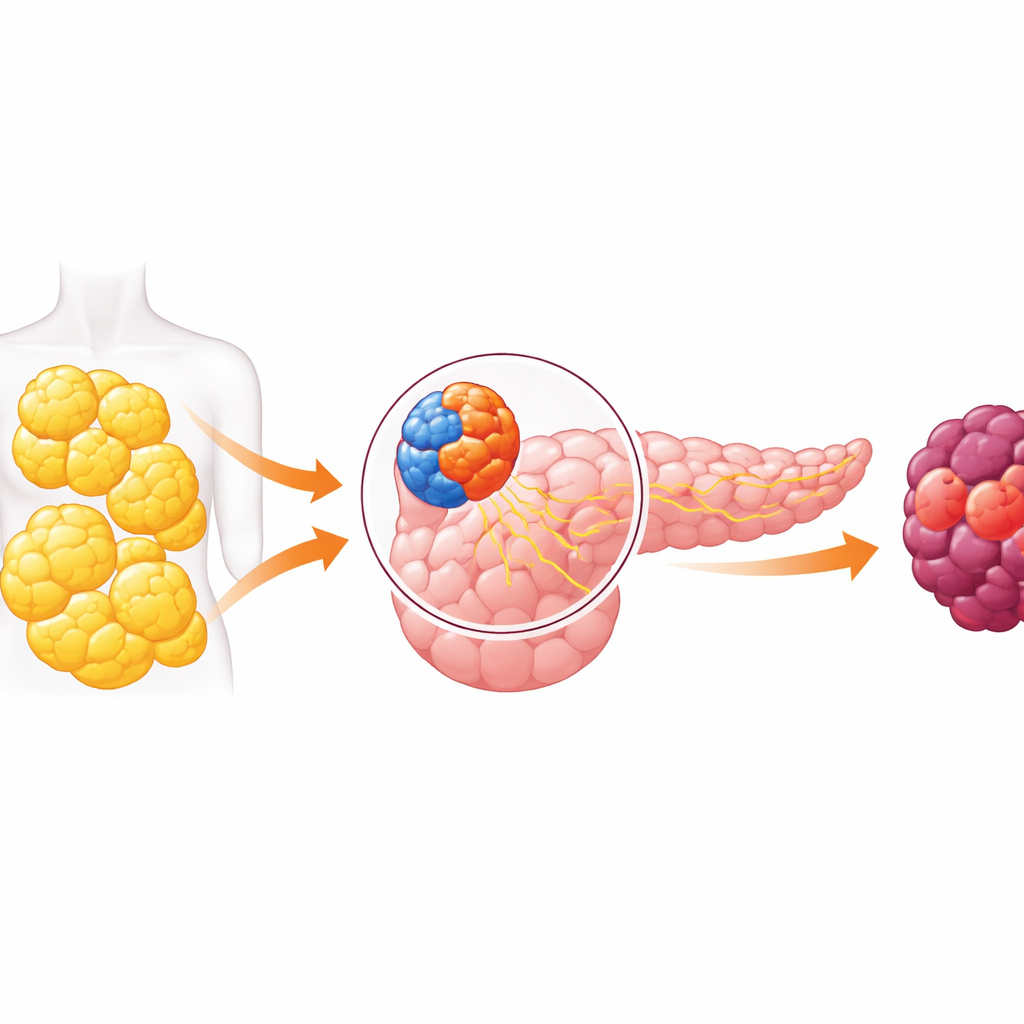
Двухсоставной орган и опасный диалог
У поджелудочной железы две основные функции. Одна — эндокринная — содержит крошечные островки клеток, выделяющие гормоны вроде инсулина для контроля уровня сахара в крови. Другая — экзокринная — вырабатывает пищеварительные соки и включает клетки, из которых чаще всего развивается рак поджелудочной. Годы исследований внушали идею, что эти отделы в значительной степени автономны. Недавние работы опровергли это представление, показав, что сигналы от гормонопродуцирующих клеток могут влиять на соседние экзокринные клетки. В этой статье подробно изучается такое перекрестное общение и показано, что при ожирении оно может сдвигать экзокринную часть поджелудочной в сторону рака.
Стресс в гормональных клетках порождает новый сигнал
При ожирении β-клетки, производящие инсулин, постоянно испытывают давление, пытаясь обеспечить повышенную потребность организма в инсулине. Используя секвенирование РНК по одной клетке и продвинутые вычислительные методы, исследователи проследили судьбу отдельных β-клеток у мышей по мере перехода от худых к избыточному весу и тяжелому ожирению. Они обнаружили, что подмножество незрелых β-клеток расширялось и постепенно теряло свою специализированную инсулинопродуцирующую идентичность. По мере того как эти клетки испытывали стресс, повышались маркеры напряжения в сворачивании белков и клеточных повреждений, а производство инсулина снижалось. Одновременно эти клетки начинали вырабатывать большие количества ХЦК — гормона, обычно связанного с кишечником, который может стимулировать рост и трансформацию экзокринных клеток.
От полезного гормона до топлива для рака
Чтобы проверить, является ли вновь синтезируемый ХЦК просто побочным продуктом стресса или активным драйвером болезни, команда создала мышей, чьи β-клетки производили дополнительный ХЦК даже без ожирения. У этих животных развивались предраковые изменения поджелудочной и инвазивные опухоли в степени, сопоставимой с ожиревшими мышами, несмотря на нормальный вес и уровень сахара в крови. Напротив, при удалении ХЦК специально из поджелудочной у ожиревших мышей бремя опухоли резко уменьшалось, хотя животные оставались тяжелыми и с повышенным уровнем инсулина. В разных мышиных моделях уровни ХЦК в поджелудочной тесно коррелировали с размерами опухоли, тогда как уровни инсулина, как правило, двигались в противоположном направлении. Это указывает на то, что именно ХЦК — а не инсулин — выступает доминирующим гормоном, связывающим ожирение с раком поджелудочной в этих системах.
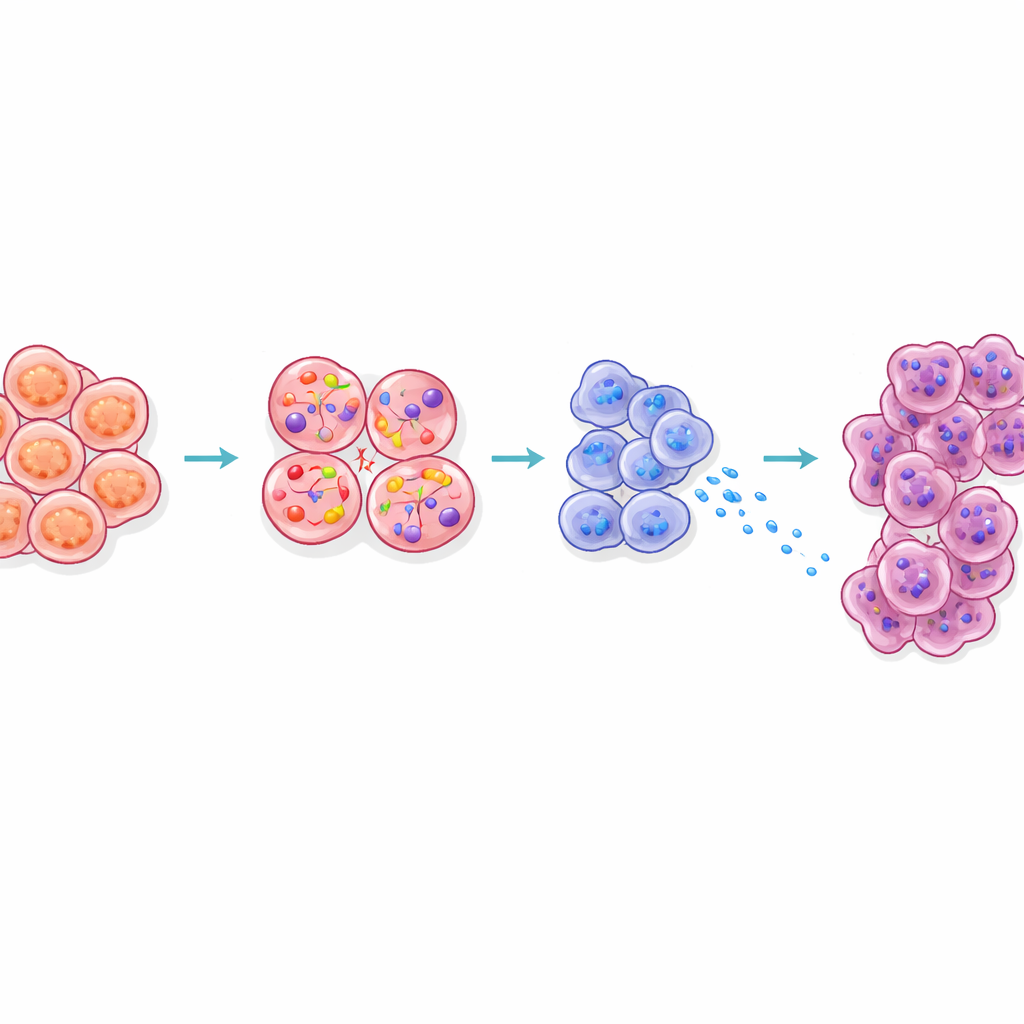
Как сигнал достигает и подготавливает соседние клетки
Исследование также изучило, как ХЦК из β-клеток перестраивает окружающую ткань. Ацинозные клетки, которые обычно секретируют пищеварительные ферменты, расположены непосредственно рядом с островками в поджелудочной. У ожиревших мышей ацинозные клетки вблизи островков демонстрировали сигнатуру стресса, вырабатывали больше пищеварительных ферментов и белков семейства Reg и переходили в состояния, известные как более восприимчивые к трансформации в рак. Блокирование ХЦК-сигналинга у ожиревших мышей снижало эти Reg-сигналы. Трехмерная визуализация дополнительно показала, что ранние предраковые очаги чаще возникали аномально близко к островкам у животных с ожирением. В совокупности эти результаты предполагают, что диффузия ХЦК из напряженных β-клеток создает «горячую зону» вокруг островков, где экзокринные клетки подготовлены к опухолевой трансформации.
Общие паттерны с человеческим диабетом и ключевой переключатель
Сравнив данные мышей с тканями поджелудочной людей с сахарным диабетом 2-го типа и без него, авторы обнаружили поразительные параллели: β-клетки доноров с диабетом соответствовали тем же стрессовым, менее зрелым состояниям, что и у ожиревших мышей. Затем они использовали регуляторный анализ, чтобы выяснить, что включает экспрессию ХЦК в β-клетках, и выявили стресс-индуцируемый путь, сосредоточенный вокруг белка cJun. Когда они блокировали верхний каскад JNK–cJun у ожиревших мышей или в клетках, напоминающих β-клетки, в культуре, уровни ХЦК падали, и наблюдали связывание cJun рядом с регуляторным участком гена CCK. Это указывает на то, что хронический стресс активирует JNK–cJun, который переводит β-клетки в режим продукции ХЦК.
Что это значит для людей в группе риска
Для неспециалиста основной вывод таков: под давлением ожирения и диабета клетки, производящие инсулин в поджелудочной, не просто дают сбой — они адаптируются так, что непреднамеренно стимулируют соседние клетки к образованию рака. Они делают это, включая синтез ХЦК — гормона, действующего как сигнал роста и стресса для соседних экзокринных клеток, создавая благоприятную почву для опухолей. Поскольку ХЦК, вырабатываемый в поджелудочной, не является необходимым для поддержания гомеостаза глюкозы, нацеливание на этот специфический источник гормона или на его стресс-активируемый переключатель теоретически может снизить риск рака поджелудочной у людей с ожирением или диабетом 2-го типа, не нарушая общего гормонального баланса. Работа переосмысливает рак поджелудочной как болезнь ошибочного общения между двумя сторонами органа и выделяет новые направления для ранней профилактики.
Цитирование: Garcia, C.C., Venkat, A., McQuaid, D.C. et al. Beta cell-derived cholecystokinin drives obesity-associated pancreatic adenocarcinoma development. Nat Commun 17, 3292 (2026). https://doi.org/10.1038/s41467-026-69821-2
Ключевые слова: рак поджелудочной железы, ожирение, β-клетки, холецистокинин, сахарный диабет 2 типа