Clear Sky Science · ru
Формирование композитного PIN‑домена SMG5‑SMG6 необходимо для NMD
Как клетки защищаются от дефектных сообщений
Клетки непрерывно считывают генетические сообщения (мРНК) для синтеза белков. Но в этих сообщениях иногда встречаются преждевременные стоп‑кодоны, которые приводят к образованию усечённых, потенциально вредных белков. Процесс, который уничтожает такие дефектные сообщения, называется нонсенс‑опосредованным распадом мРНК (NMD). В статье раскрывается, как два ключевых белка, SMG5 и SMG6, физически взаимодействуют, чтобы разрезать повреждённые сообщения, поясняя давнюю загадку механизма клеточного контроля качества.
Нахождение скрытого партнёрства
Многие годы было известно, что SMG6 способен непосредственно расщеплять РНК, тогда как SMG5 считался «каталитически мёртвым» и выступал главным образом в роли вспомогательного фактора или каркаса. Тем не менее эксперименты в клетках показали противоречивую картину: SMG6 не функционирует должным образом без SMG5, и NMD нарушается при отсутствии любого из них. Авторы использовали современные методы предсказания структуры (AlphaFold), биохимические анализы с очищенными белками и генетические тесты в линиях человеческих клеток, чтобы разрешить это противоречие. Их модели предсказали, что хвостовые участки SMG5 и SMG6, называемые PIN‑доменами, стыкуются друг с другом и формируют совместную структуру. Это композитное образование — названное «cPIN» — предложено в качестве истинного режущего механизма в NMD. 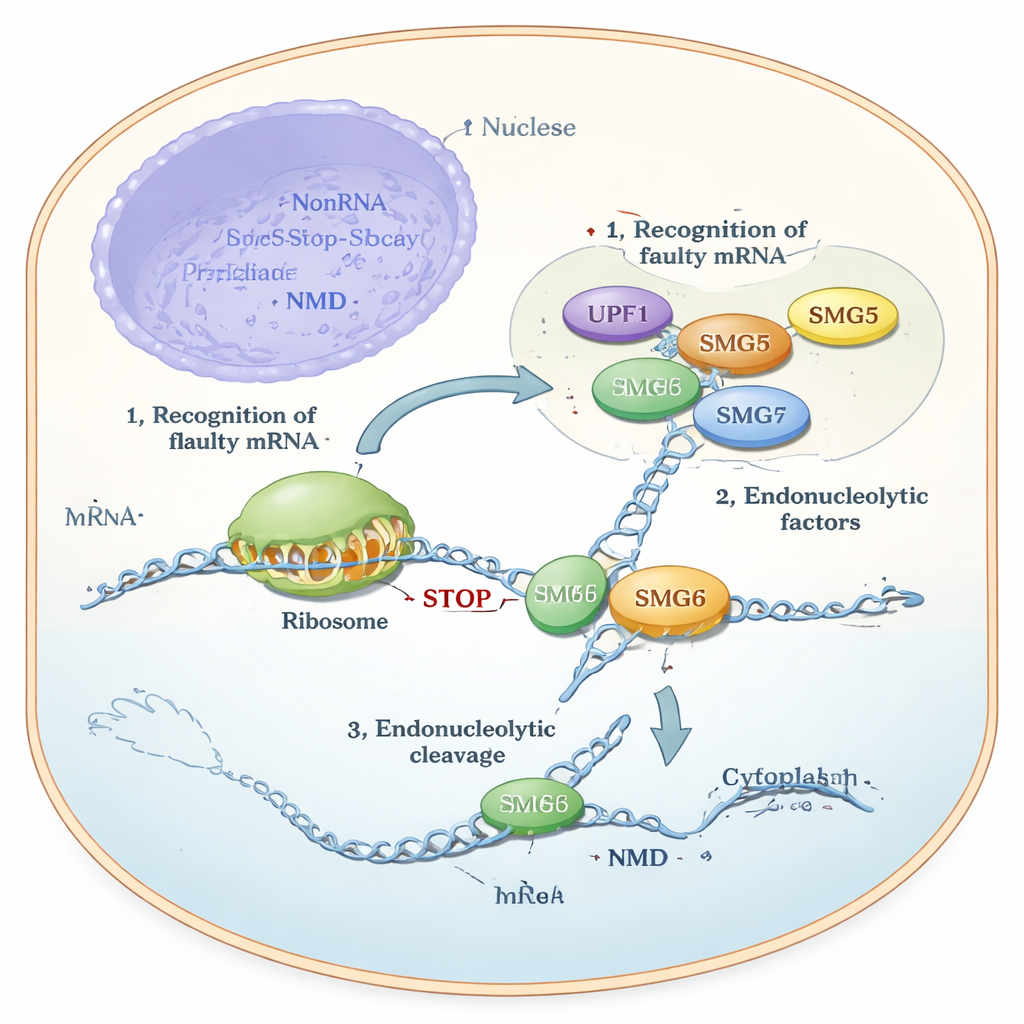
Воссоздание молекулярных ножниц в пробирке
Чтобы проверить предсказание, команда получила фрагменты человеческих SMG5 и SMG6 в бактериях и очистила их. По отдельности SMG6 демонстрировал лишь слабую способность рассекать синтетический РНК‑субстрат, а SMG5 в одиночку практически не проявлял активности. Но при смешивании двух фрагментов активность расщепления резко возрастала, даже в условиях, когда влияние контаминантных ферментов было маловероятно. Такой же эффект наблюдали на линейных и кольцевых РНК‑тестах, что указывает на то, что усиленное расщепление действительно исходило от пары SMG5–SMG6. Химическое кросслинкование и масс‑спектрометрия дополнительно показали, что оба белка находятся в близком контакте, поддерживая идею прямого, пусть и временного, партнёрства.
Довершение режущего узла
Структурные модели показали, как именно SMG5 усиливает SMG6. SMG6 вносит четыре кислые аминокислоты, которые удерживают ионы металлов в сердце каталитического центра, как это типично для этого семейства ферментов. Неожиданно модели поместили дополнительную кислую радикальную группу из SMG5 прямо рядом с ними, фактически расширяя каталитическую впадину. Другие положительно заряженные остатки SMG5, как предсказывали, захватывают остов РНК и помогают правильно её позиционировать для разрезания. Когда исследователи мутировали эти критические остатки в SMG5 или SMG6, композитный комплекс потерял значительную часть своей режущей активности in vitro. Те же мутации не смогли восстановить NMD в генетически модифицированных человеческих клетках с истощённым нормальным белком, что тесно связывает структурную модель с реальной клеточной функцией. 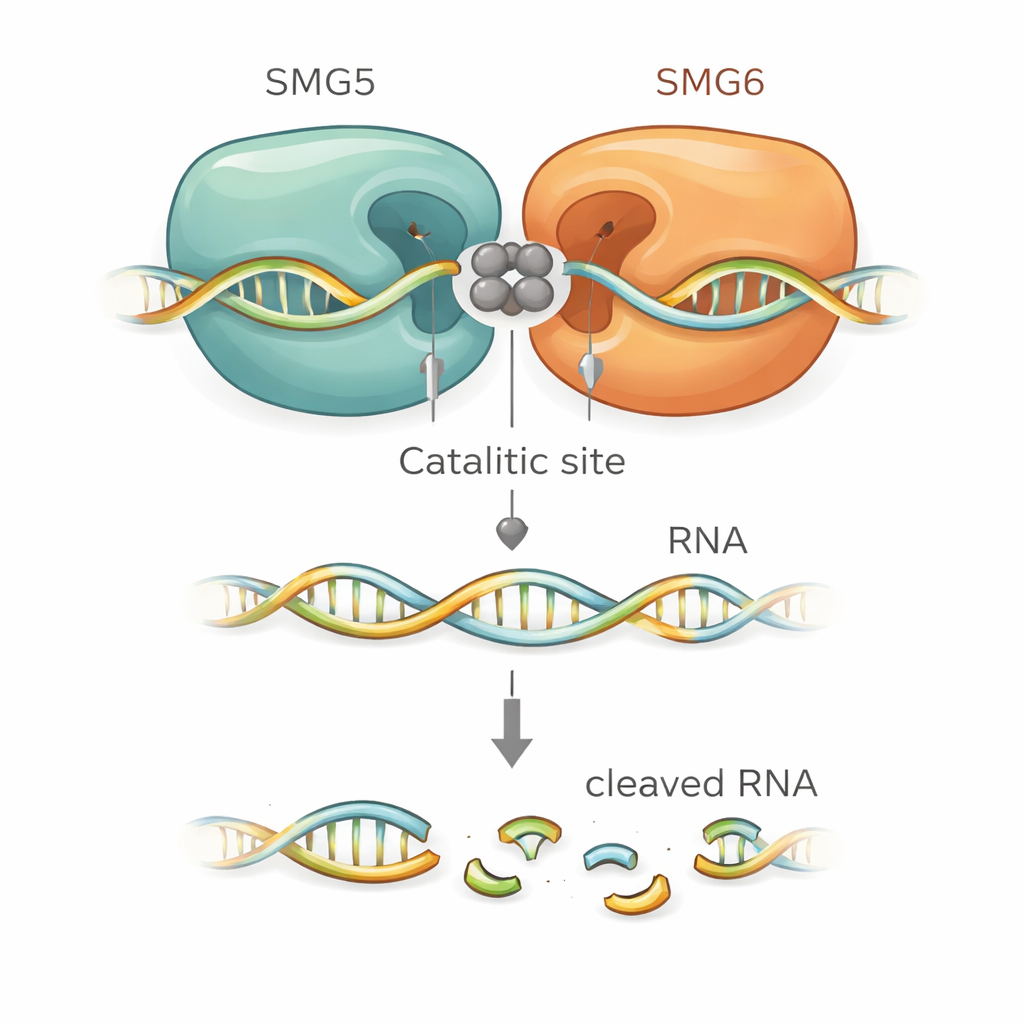
Доказательство, что оба партнёра необходимы в клетках
Поскольку полное удаление SMG5 или SMG6 приводит к гибели клеток, команда применила систему «дегрон», позволяющую пометить каждый белок так, чтобы он мог быть быстро уничтожен при добавлении малого молекулярного вещества. Сочетание быстрой деградации с РНК‑интерференцией позволило почти полностью удалить SMG5, SMG6 или центральный регулятор UPF1. Последующее геномное секвенирование РНК показало, что происходит с NMD при потере каждого фактора. Истощение SMG5 или UPF1 вызывало почти идентичные изменения в клеточных РНК, с сильным накоплением дефектных, чувствительных к NMD транскриптов. Удаление SMG6 давало очень похожий, хотя немного более мягкий, эффект. Эти данные показывают, что SMG5 и SMG6 не являются необязательными параллельными ветвями пути; напротив, они действуют вместе с UPF1 как ключевые компоненты одного основного маршрута распада.
Почему это важно для здоровья клеток
Проще говоря, исследование показывает, что SMG5 и SMG6 соединяются, образуя единые, мощные молекулярные «ножницы», которые разрезают дефектные генетические сообщения. SMG6 обеспечивает большую часть «лезвия», но SMG5 добавляет недостающий край и помогает удерживать РНК на месте, превращая слабый резак в эффективный. Этот композитный «cPIN» объясняет, почему клетки абсолютно нуждаются в обоих белках для поддержания чистоты своих РНК‑сообщений. Проясняя, как ключевой режущий шаг NMD включается только при распознавании дефектных сообщений, работа даёт более ясное представление о том, как клетки предотвращают накопление токсичных усечённых белков и тонко регулируют экспрессию генов.
Цитирование: Kurscheidt, K., Theunissen, S., Pasquali, N. et al. Composite SMG5-SMG6 PIN domain formation is essential for NMD. Nat Commun 17, 1934 (2026). https://doi.org/10.1038/s41467-026-69819-w
Ключевые слова: распад мРНК, обусловленный нонсенс‑кодонами, контроль качества РНК, SMG5 SMG6, надзор за мРНК, регуляция экспрессии генов