Clear Sky Science · ru
Неингибирующие гидролиз ацетиллизиновые аналоги для изучения ацетилирования белков in vitro и в клетках
Почему крошечные химические метки на белках важны
Внутри каждой клетки белки постоянно модифицируются малыми химическими метками, которые действуют как выключатели или регуляторы их активности. Одна из наиболее важных таких меток — ацетилирование, которое может менять поведение белка без изменения его генетической информации. Понять, что именно делает ацетилирование в одной конкретной позиции конкретного белка, оказалось непросто, потому что клетки могут снимать эти метки так же быстро, как и ставят их. В этом исследовании представлен хитрый химический «заместитель» ацетилирования, который не может быть удалён, что даёт учёным способ зафиксировать эти переключатели и проследить последствия.
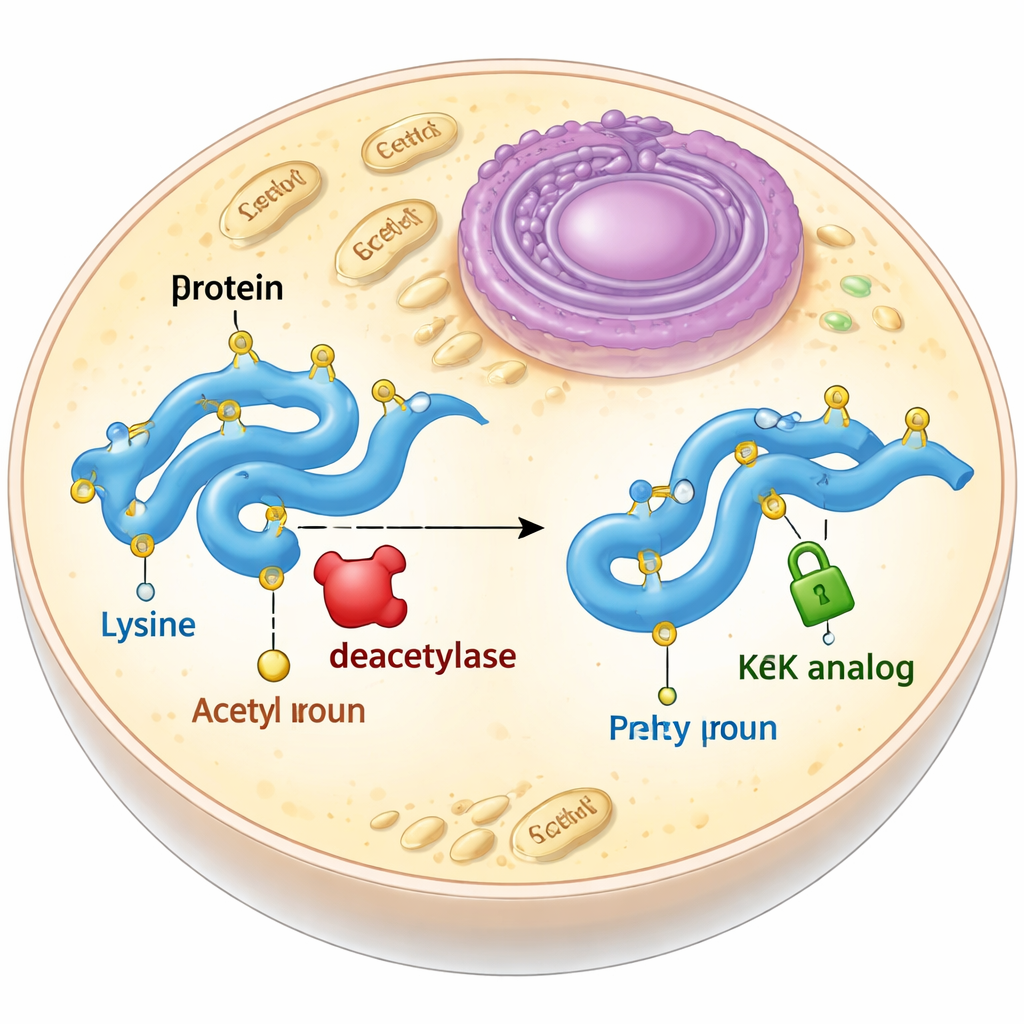
Стабильный заместитель для мимолёгкой метки
Ацетилирование обычно происходит на аминокислотном остатке лизина. Когда лизин ацетилирован, он теряет положительный заряд, а его боковая цепь становится немного длиннее. Биологи часто пытаются имитировать это, мутируя лизин в глутамин, который нейтрален, но короче, или вводя настоящий ацетиллизин с помощью расширения генетического кода. Обе стратегии имеют недостатки: глутамин не полностью воспроизводит пространственные изменения, вызванные ацетилированием, а настоящий ацетиллизин внутри клеток быстро снимается ферментами-деацетилазами. Авторы поставили задачу разработать и проверить аналоги ацетиллизина, которые сохраняют нужный размер и форму, но не могут быть удалены.
Тестирование новых химических мимиков на модельном белке
Команда сначала сосредоточилась на убиквитине — небольшом, хорошо изученном белке, который сам по себе часто модифицируется разными метками. С помощью современных методов генетической инженерии они ввели разные варианты лизина в одну позицию убиквитина: натуральный ацетиллизин, два неустранимых аналога TFAcK и кетолизин (KeK), а также распространённые заместители, такие как глутамин, аланин и аргинин. Затем они исследовали, как эти изменения влияют на структуру и функцию убиквитина. Высокопрецизионная ЯМР-производная показала, что ацетиллизин, TFAcK и KeK вызывают почти идентичные структурные изменения, особенно вокруг центральной спирали, тогда как глутамин и другие простые замены — нет. Функциональные тесты с ферментом HDM2 показали, что убиквитин с ацетиллизином, TFAcK или KeK ведёт себя схоже между собой и отличен от версии с глутамином, что подчёркивает: важны не только заряд, но и длина и объём боковой цепи.
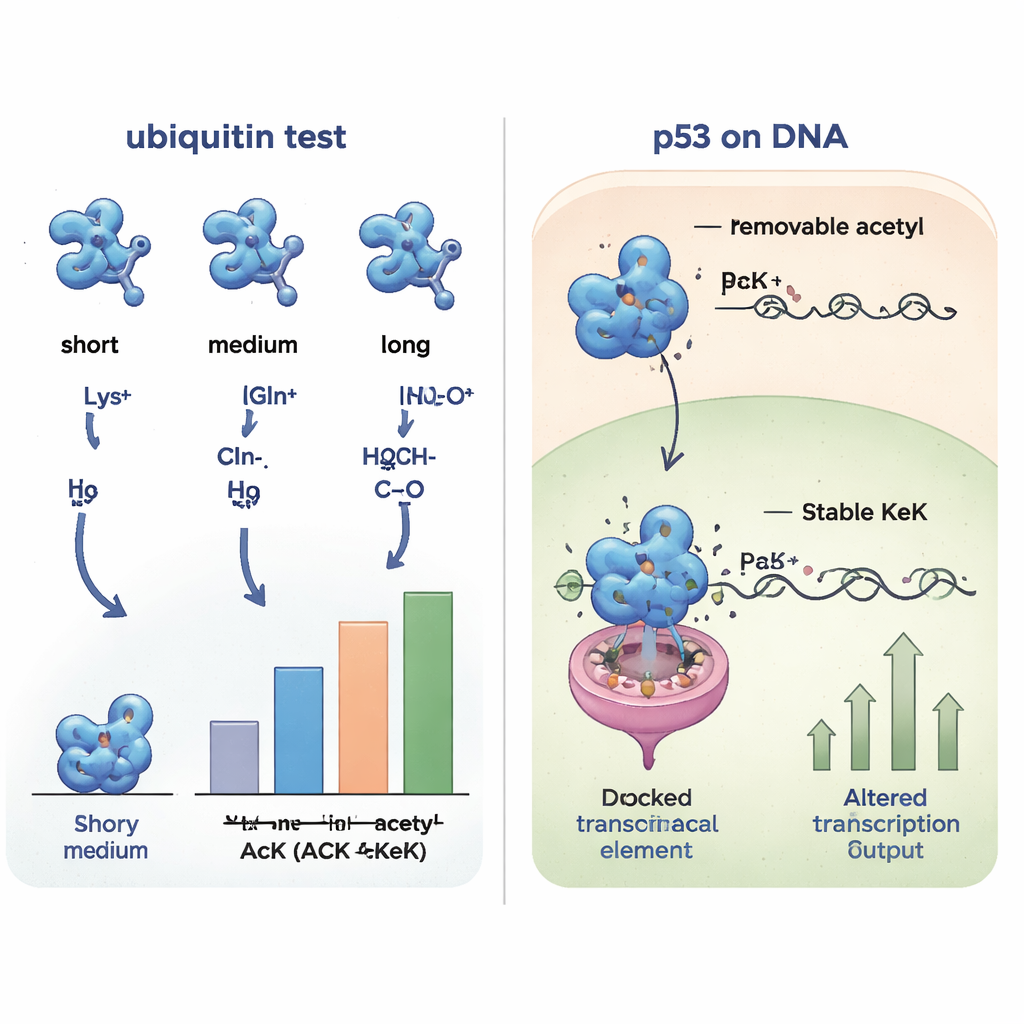
Изучение белковых взаимодействий по всей клетке
Поскольку небольшие структурные изменения могут менять набор партнёров белка, исследователи сравнили, как разные версии убиквитина связываются с белками из экстрактов человеческих клеток. Выводя белки-«партнёры» и идентифицируя их методом масс-спектрометрии, они обнаружили, что убиквитин с ацетиллизином, TFAcK или KeK имеет очень похожие профили взаимодействий, тогда как формы с глутамином или аланином образуют отдельную группу и выглядят иначе. Положительно заряженные варианты (лизин или аргинин) сформировали ещё одну группу. Эта систематическая сравнительная оценка показала, что неустранимые аналоги TFAcK и особенно KeK гораздо лучше имитируют и структуру, и поведение в связывании настоящего ацетиллизина, чем традиционная замена на глутамин.
Фиксация ацетилирования на супрессоре опухолей p53
Чтобы проверить, работают ли эти инструменты внутри живых клеток, авторы обратились к p53 — ключевому супрессору опухолей, часто называемому «стражем генома». Конкретные лизины в ДНК-связывающем домене p53 могут быть ацетилированы, что меняет набор генов, которые он включает, например те, что останавливают клеточный цикл или запускают гибель клетки. Команда модифицировала человеческие клетки так, чтобы p53 включал ацетиллизин, TFAcK или KeK в двух важных позициях (120 и 164) лишь при наличии соответствующей нестандартной аминокислоты. Все три могли быть встроены в p53, но детальные измерения показали, что в клетках ацетил- и TFAcK-группы в значительной степени удалялись деацетилазами, тогда как KeK оставался неизменным. При тестировании способности p53 активировать репортерный ген и естественный ген p21 варианты с KeK в этих позициях оказались гораздо менее активными, что соответствует эффекту «зафиксированного» ацетилирования, тогда как ацетиллизин и TFAcK вели себя ближе к нормальному p53 из‑за их деацетилирования.
Что это значит для изучения клеточных решений
В целом исследование показывает, что KeK — это достоверный и неустранимый заместитель ацетиллизина: он точно воспроизводит структурные изменения, предпочтения в связывании и функциональные последствия ацетилирования, но не может быть удалён клеточными ферментами. Для неспециалистов это означает, что у исследователей появляется способ «зафиксировать» обычно обратимый химический переключатель в одной позиции белка и проследить, как это влияет на процессы, такие как регуляция генов и судьба клетки. Это упростит отделение специфических ролей ацетилирования от других перекрывающихся модификаций и в конечном итоге может прояснить, как нарушение регуляции ацетилирования белков вносит вклад в заболевания, такие как рак.
Цитирование: Kienle, S.M., Sigg, M., Schneider, T. et al. Non-hydrolyzable acetyllysine analogs to study protein acetylation in vitro and in cells. Nat Commun 17, 1985 (2026). https://doi.org/10.1038/s41467-026-69782-6
Ключевые слова: ацетилирование белков, посттрансляционная модификация, убиквитин, p53, расширение генетического кода