Clear Sky Science · ru
Динамическая перестройка транскриптома в пересаженных человеческих нейропрогениторных клетках выявляет механизмы сохранения зрения в модели пигментного ретинита у крыс
Почему важно защищать угасающее зрение
Пигментный ретинит — это группа наследственных заболеваний, которые постепенно лишают людей зрения, часто начинаясь с ночной слепоты и прогрессируя до юридической слепоты. Поскольку сотни различных генетических мутаций могут вызывать это состояние, лечить каждую из них с помощью генной терапии сложно. В этом исследовании изучается более универсальный подход: трансплантация человеческих нейропрогениторных клеток — незрелых нервных клеток, выращенных в лаборатории — в глаз для защиты оставшихся светочувствительных клеток. Понимание того, как именно ведут себя эти пересаженные клетки и как они способствуют сохранению зрения, может сформировать будущие методы лечения не только при пигментном ретините, но и при других слепящих поражениях.
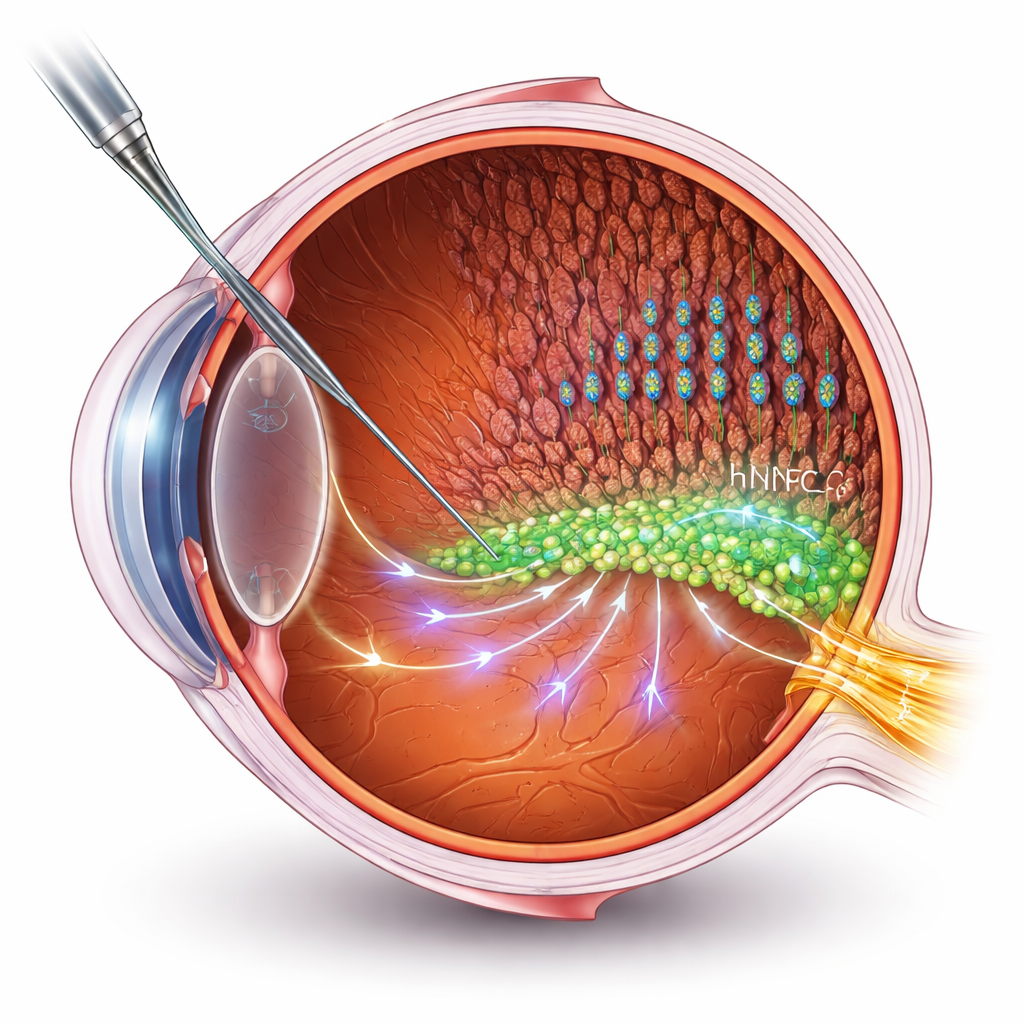
Помогать клеткам вместо их замены
Многие терапии со стволовыми клетками нацелены на замену погибших или повреждённых клеток. Но при запущенных заболеваниях сетчатки построение новых связей с мозгом представляет собой серьёзную техническую проблему. В этой работе исследователи выбрали иной путь: использование человеческих нейропрогениторных клеток (hNPCs) как «помощников», поддерживающих собственные клетки сетчатки пациента. Они пересадили hNPCs в субретинальное пространство хорошо известной модели пигментного ретинита у крыс, затем оценивали зрение с помощью электрических записей и поведенческих тестов. Лечёные животные сохраняли лучшую зрительную функцию и более целые слои фоторецепторов — палочек и колбочек, улавливающих свет — по сравнению с нелечеными, хотя дегенерация всё же постепенно продолжалась.
Как пересаженные клетки меняются в больном глазу
Чтобы выяснить, что происходит на молекулярном уровне, команда использовала секвенирование РНК одиночных клеток — метод, который определяет, какие гены активны в тысячах отдельных клеток. Они отслеживали пересаженные hNPCs в две временные точки, примерно на ранней и поздней стадиях после трансплантации. Вместо превращения в новые фоторецепторы большинство пересаженных клеток дифференцировались в астроцитоподобные поддерживающие клетки, меньшая доля проявляла маркеры олигодендроцитов или незрелых нейронов. Со временем эти клетки стабилизировались, приобретая черты, указывающие на их приспособленность к выживанию в стрессовой, дегенерирующей среде и на способность тесно взаимодействовать с соседними клетками сетчатки.
Защитные сигналы, метаболизм и уборка
hNPCs продуцировали богатый набор защитных белков, известных как трофические факторы. Среди них были MANF и MYDGF, связанные с выживанием клеток, снижением окислительного стресса и подавлением воспаления, а также другие факторы, такие как мидкин и плейтротрофин, которые поддерживают рост и миграцию нейрональных клеток. Эти молекулы, по-видимому, действовали как на сам трансплантат, так и на окружающую сетчатку. У лечёных крыс активность генов в палочках и колбочках была ближе к контролю, с улучшенной поддержкой визуальной сигнализации и клеточного обслуживания. Пересаженные клетки также усиливали пути, связанные с утилизацией клеточного мусора и настройкой метаболизма, что указывает на их роль в помощи фоторецепторам справляться с энергетическими потребностями и токсическими побочными продуктами, накапливающимися при болезни.
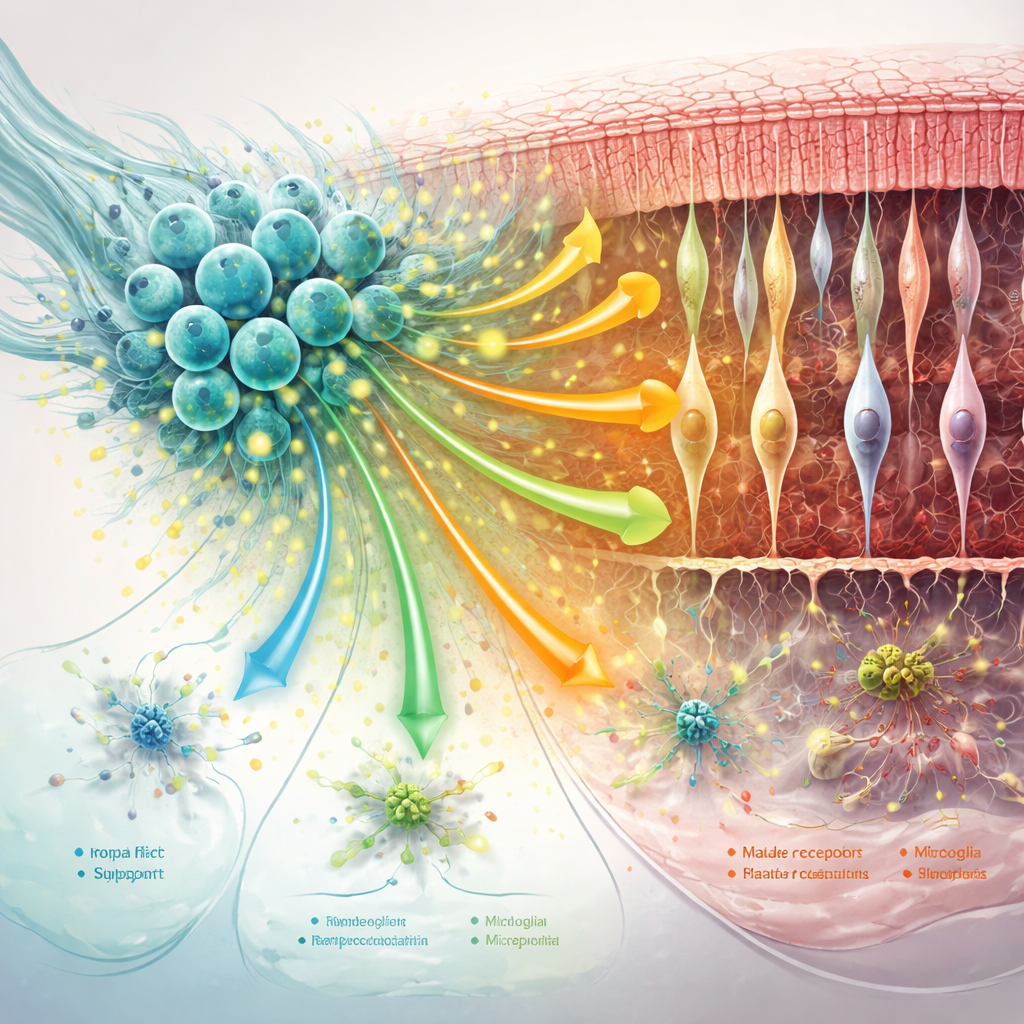
Успокаивающая поддержка и перестройка ретинального окружения
Сеть поддерживающих клеток сетчатки — глии Мюллера, микроглия и окружающий матрикс белков — играет большую роль в том, будет ли дегенерация усугубляться или замедляться. В исследовании показали, что лечение hNPCs снижало ключевые маркеры вредных «реактивных» изменений в глиях Мюллера и смещало микроглию от чрезмерно воспалительных состояний, особенно на ранних этапах. Одновременно усиливались сигналы коммуникации, способствующие стабилизации синапсов, сцеплению клеток и поддержанию каркаса вокруг фоторецепторов. По мере прогрессирования болезни часть этих преимуществ ослабевала: общение между клетками снижалось, некоторые защитные пути — в том числе сигналы, связанные с MANF — уменьшались, а поддерживающие клетки приобретали более стресс- и иммуноориентированные профили.
Что это значит для будущих терапий глаза
Для неспециалиста основная мысль такова: пересаженные человеческие нейропрогениторные клетки могут действовать как локальные «первые ответчики» в дегенерирующей сетчатке. Они не восстанавливают сетчатку с нуля, но выделяют защитные молекулы, регулируют метаболизм, успокаивают вредящее воспаление и помогают сохранять местную структуру, что в целом замедляет потерю зрения. Однако этот защитный эффект со временем ослабевает, поскольку среда становится более враждебной и «диалог» между пересаженными и донорскими клетками ухудшается. Авторы предполагают, что усиление ключевых факторов, таких как MANF, и улучшение состояния хостовой сетчатки — возможно, с помощью генетической модификации трансплантата или комбинированных методов лечения — могут быть необходимы, чтобы превратить временное облегчение в долговременное сохранение зрения.
Цитирование: Shahin, S., Bell, S., Lu, B. et al. Dynamic transcriptomic remodeling in grafted human neural progenitor cells uncovers mechanisms for vision preservation in a rat model of retinitis pigmentosa. Nat Commun 17, 2164 (2026). https://doi.org/10.1038/s41467-026-69776-4
Ключевые слова: пигментный ретинит, терапия стволовыми клетками, дегенерация сетчатки, нейропротекция, секвенирование РНК одиночных клеток