Clear Sky Science · ru
TCL1A опосредует дефекты метилирования ДНК при рецидивирующем пузырном заносе при патогенных вариантах NLRP7
Почему это важно для здоровья женщин
Некоторые беременности нарушаются очень рано и вместо развивающегося плода превращаются в массу аномальной плацентарной ткани. Это состояние, называемое пузырным заносом, может повторяться у некоторых женщин и иногда прогрессировать до рака. В этом исследовании анализируется одна из основных генетических причин этих редких, но тяжёлых беременностей и раскрывается, как единичный дефект защиты в яйцеклетке может разрушить химические «ярлыки», которые направляют нормальное развитие.
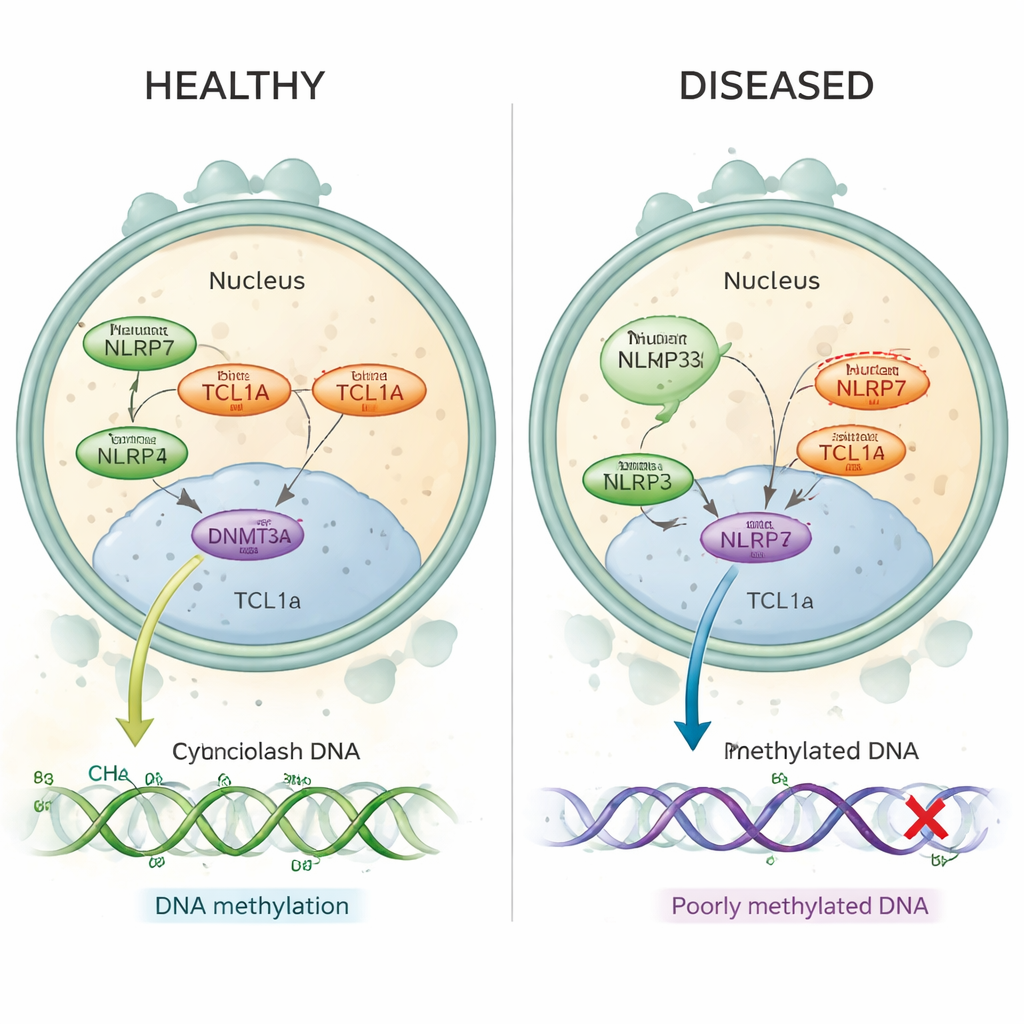
Проблема беременности, происходящая из яйцеклетки
Рецидивирующий пузырный занос — это расстройство, при котором у женщин многократно случаются молярные беременности, часто без нормальных беременностей между ними. Сейчас известно, что многие такие случаи вызваны вредными изменениями в гене NLRP7, который активен в яйцеклетке до оплодотворения и вскоре после него. У этих женщин ключевые участки ДНК, которые должны нести «отпечатки» от матери, лишены нормальных метильных меток — небольших химических тегов, помогающих включать или выключать гены в нужное время. До сих пор учёные не понимали, как белок, находящийся в цитоплазме яйцеклетки, как NLRP7, может контролировать метилирование, происходящее на ДНК внутри ядра.
Нахождение отсутствующего партнёра
Чтобы разгадать эту загадку, исследователи изучили выброшенные человеческие яйцеклетки и очень ранние эмбрионы из клиник репродукции. Они извлекли NLRP7 и его известных партнёров из этих клеток и идентифицировали другие белки, которые шли вместе с ним. Один из них выделялся: TCL1A, уже известный в онкогематологии как белок, способный проникать в ядро и вмешиваться в работу ферментов метилирования ДНК — DNMT3A и DNMT3B. TCL1A встречается в необычно больших количествах в человеческих яйцеклетках, что указывает на его важную роль там. Детальные тесты взаимодействия показали, что TCL1A прочно и специфично связывается с NLRP7, но не с близкородственными белками, и что этот комплекс встроен в более крупную яйцеклеточную структуру, называемую субкортикальным материнским комплексом.
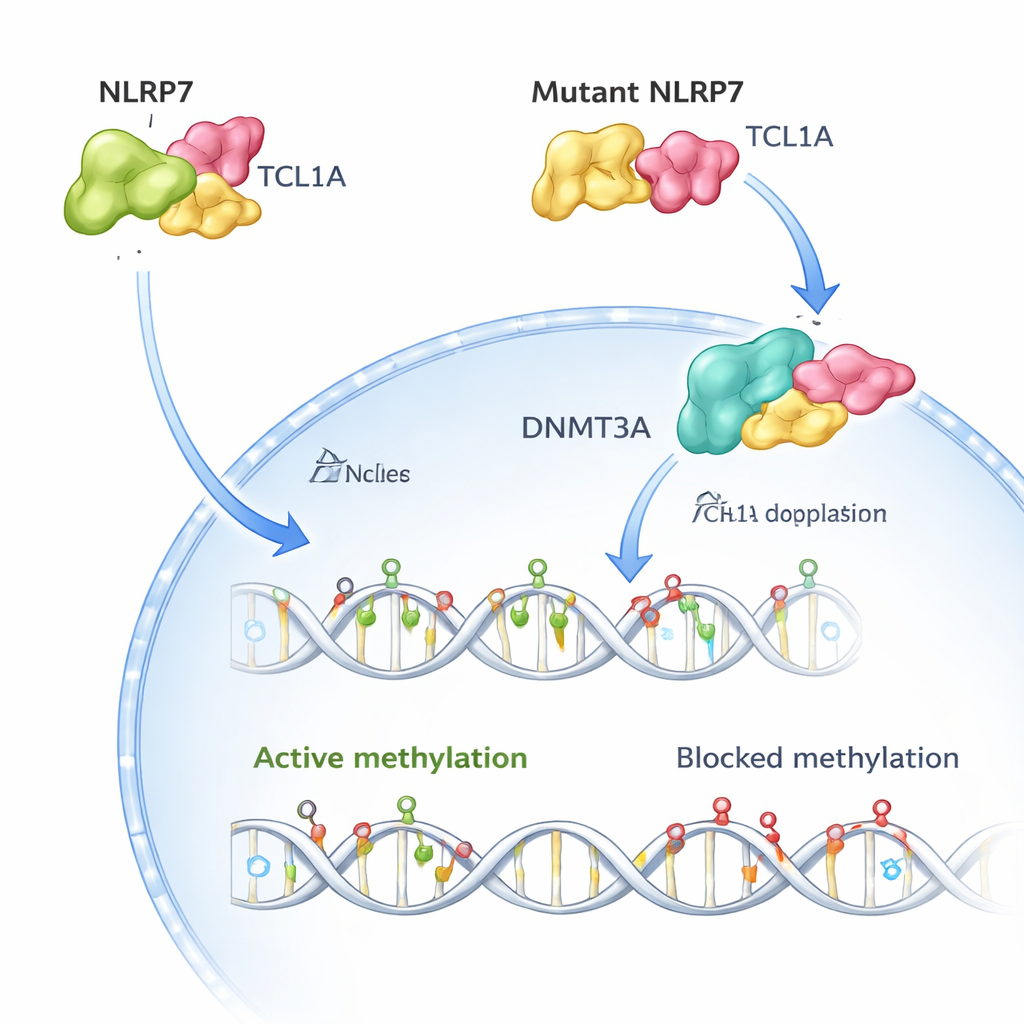
Видеть молекулярные объятия
Команда затем использовала криоэлектронную микроскопию, чтобы визуализировать трёхмерную структуру комплекса NLRP7–TCL1A. Они обнаружили, что два молекулы NLRP7 объединяются, и каждая удерживает димер TCL1A вдоль изогнутой поверхности, состоящей из повторяющихся мотивов. Такая организация объясняет, почему многие патогенные изменения в NLRP7 сосредоточены вдоль этой поверхности: изменение ключевых контактных точек ослабляет или разрушает связь с TCL1A. Когда исследователи воссоздали более 50 известных вариантов пациентов в клетках, большинство версий, связанных с рецидивирующими молярными беременностями, либо дестабилизировали NLRP7, либо резко снижали его способность связываться с TCL1A.
Как смещённые белки нарушают метки ДНК
В здоровых человеческих яйцеклетках и NLRP7, и TCL1A в основном находятся в цитоплазме, при этом только небольшая часть TCL1A достигает ядра. Авторы показывают, что NLRP7 фактически действует как привратник: когда он может удерживать TCL1A, TCL1A остаётся вне ядра. Когда NLRP7 мутирован и больше не может хорошо связываться, TCL1A просачивается в ядро. Там он присоединяется к DNMT3A — основному ферменту, который откладывает новые метильные метки в яйцеклетках — и подавляет его активность. В моделях стволовых клеток, которые обычно приобретают метилирование по мере созревания, чрезмерная экспрессия TCL1A вызывала драматическую потерю метилирования по всему геному, тогда как совместная экспрессия NLRP7 частично восстанавливала этот дефект. В совокупности эти результаты поддерживают простую картину: нормальный NLRP7 удерживает «тормоз» метилирования (TCL1A) в цитоплазме, чтобы DNMT3A мог правильно маркировать ДНК; дефектный NLRP7 позволяет этому тормозу попасть в ядро и блокировать процесс.
От механизма к диагностике
Помимо объяснения происхождения рецидивирующих молярных беременностей, исследование предлагает практический способ оценить, действительно ли недавно обнаруженное изменение NLRP7 у пациента является вредным. Авторы сравнивают три подхода — лабораторные тесты на связывание NLRP7–TCL1A, компьютерные прогнозы и стандартные генетические инструменты оценки — и показывают, что потеря связывания с TCL1A тесно коррелирует с вариантами, вызывающими заболевание. Они также выявляют ранее нераспознанный вредный вариант L766R в семьях с рецидивирующими заносами, подтвердив, что он как ослабляет белок, так и направляет TCL1A в ядро.
Что это значит простыми словами
Эта работа раскрывает молекулярную цепную реакцию, лежащую в основе редкого, но разрушительного нарушения беременности. По сути, яйцеклетки поражённых женщин несут сломанный «телохранитель» — белок NLRP7, который не удерживает своего партнёра TCL1A вне ядра. Попав внутрь, TCL1A мешает ферменту, который наносит жизненно важные химические метки на ДНК. Без этих меток ранняя плацента развивается аномально, и плод не формируется. Проследив этот путь шаг за шагом, исследование проясняет, почему определённые генетические изменения у матери могут многократно срывать беременности, и указывает путь к более точному генетическому консультированию и диагностике для женщин с рецидивирующими пузырными заносами.
Цитирование: Gao, Z., Liu, Q., Li, L. et al. TCL1A mediates DNA methylation defects in recurrent hydatidiform mole with NLRP7 pathogenic variants. Nat Commun 17, 2160 (2026). https://doi.org/10.1038/s41467-026-69744-y
Ключевые слова: метилирование ДНК, рецидивирующий пузырный занос, NLRP7, TCL1A, геномное отпечатывание