Clear Sky Science · ru
GCN5 способствует прогрессированию MASLD через путь сигнальной передачи LXRα/SREBP1c, опосредующий de novo липогенез
Почему эта история о печени важна
Метаболически обусловленное стеатотическое заболевание печени (MASLD), ранее называвшееся неалкогольной жировой болезнью печени, сейчас поражает примерно каждого четвертого человека в мире. Оно часто развивается бессимптомно, но может прогрессировать в фиброз, рак печени и серьёзные метаболические осложнения. В этом исследовании выявлен молекулярный «регулятор громкости», который способствует вредному накоплению жира в печени, и показано, что его приглушение может защищать печень и потенциально повысить безопасность существующих лекарственных стратегий для сердца.
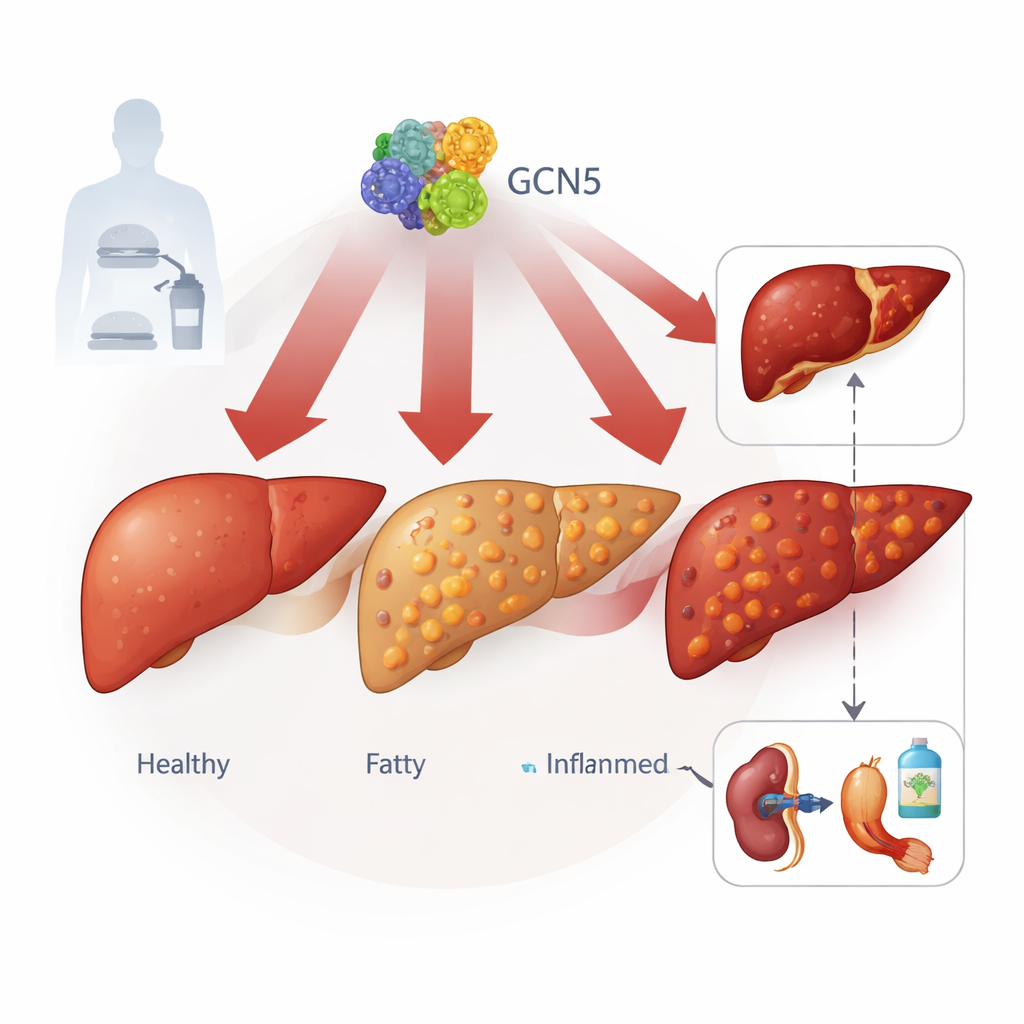
Скрытый переключатель внутри печёночных клеток
Авторы сосредоточились на белке GCN5, наиболее известном как регулятор упаковки ДНК. Изучив печёночную ткань более чем 100 человек — от здоровых до тяжёлых случаев MASLD, а также несколько мышиных моделей жировой болезни печени, они обнаружили, что уровни GCN5 в печёночных клетках постоянно повышаются по мере прогрессирования болезни. Родственный белок PCAF не демонстрировал такой закономерности, что указывает на особую роль GCN5. Высокий уровень GCN5 коррелировал с большим содержанием жира в печени, повышенными липидами в крови и более выраженными признаками повреждения печени, связывая этот молекулярный переключатель с клинической тяжестью заболевания.
Повышение и снижение GCN5 у животных
Чтобы проверить причинно-следственную связь, команда генетически увеличивала или удаляла GCN5 исключительно в печёночных клетках мышей. При повышении GCN5 мыши, получавшие высокожировую диету, развивали более тяжёлую, более жировую печень, более высокие уровни липидов в крови и больше повреждений печёночных клеток, хотя они не потребляли больше пищи и не набирали лишний вес. Печёночные клетки в культуре вели себя аналогично: избыток GCN5 приводил к увеличению числа и размера жировых капель. Напротив, мыши с удалённым GCN5 только в печени были надёжно защищены. В нескольких диетных моделях, имитирующих человеческую MASLD и её более воспалительную форму, эти животные накапливали меньше жира в печени, имели более низкие уровни липидов и ферментов печени в крови и развивали меньше воспаления и фиброза.
Как GCN5 побуждает печень синтезировать жир
Изучая метаболизм, исследователи измеряли множество жирных кислот и их строительных блоков в печени. Потеря GCN5 преимущественно снижала уровни жиров, которые печень синтезирует «с нуля» — процесс, известный как de novo липогенез, — оставляя при этом пищевые полиненасыщенные жиры главным образом без изменений. Экспрессия генов и эксперименты с изотопным трассированием показали, что GCN5 находится выше по потоку относительно ключевого регулятора липогенеза SREBP1c. Когда GCN5 активен, включаются гены, ответственные за синтез и модификацию жирных кислот, и внутренняя скорость образования жира в печени растёт. Удаление или блокада GCN5 притормаживали эту программу, сокращая поток углерода из сахаров в вновь синтезируемые печёночные жиры.
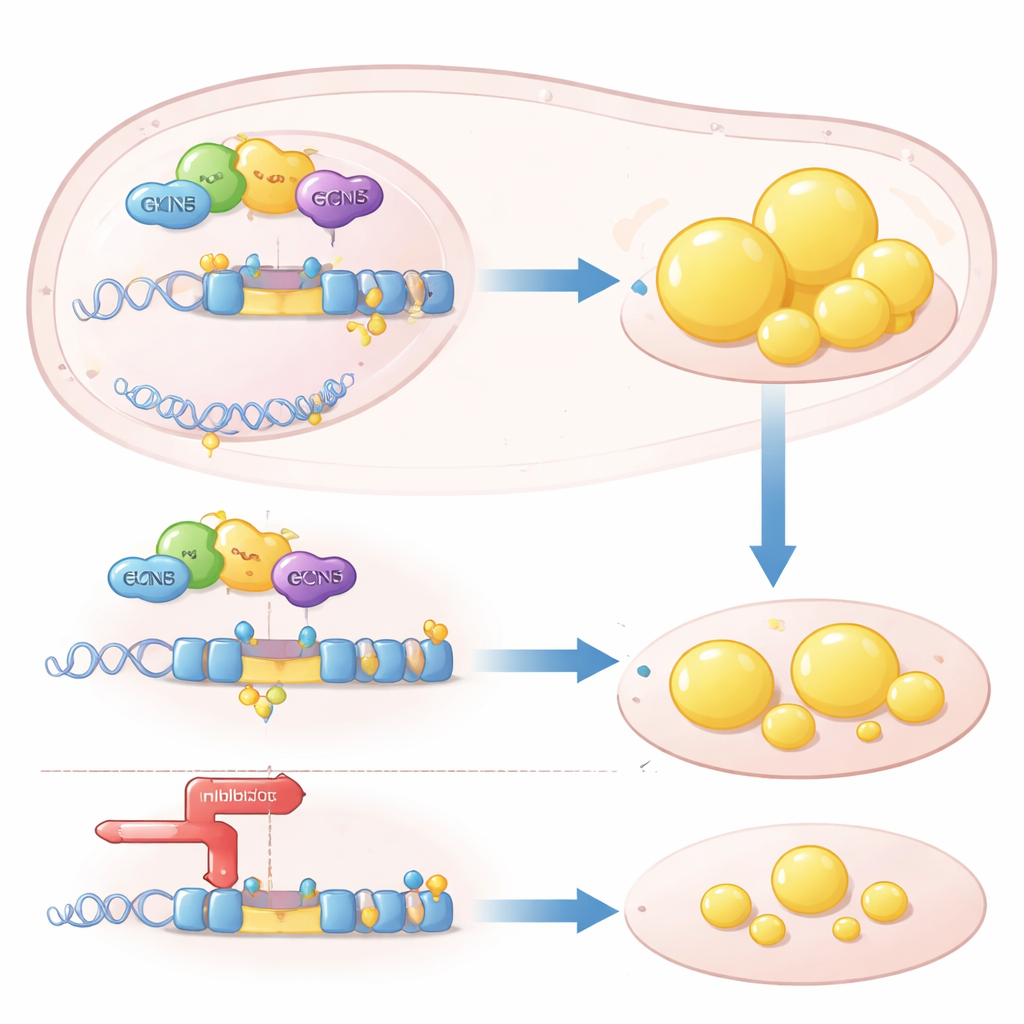
Эпигенетический рычаг на ключевом гене жира
Механистически GCN5 действует как «эпигенетический» рычаг: он химически модифицирует гистоны на ДНК, делая определённые гены более доступными для чтения. Авторы показали, что GCN5 привлекается к регуляторной области гена SREBP1c вместе с ядерным рецептором LXRα, который чувствует молекулы, связанные с холестерином. Оказавшись там, GCN5 добавляет ацетильные метки на гистон H3, разрыхляя хроматин и усиливая транскрипцию SREBP1c. Этот эффект был высокоизбирательным: GCN5 усиливал способность LXRα активировать SREBP1c, но не другой мишень LXR — ABCA1, участвующую в выведении холестерина из тканей. При отсутствии GCN5 LXRα больше не мог эффективно взаимодействовать с промотором SREBP1c, и программа синтеза жира тормозилась.
Кандидат в препараты и перспективная комбинация
Далее команда протестировала CPTH2, малую молекулу‑ингибитор GCN5, которая накапливается в печени. В мышиных моделях, уже получавших жирные диеты, CPTH2 уменьшал размер печени, её содержание жира и маркеры повреждения без очевидной токсичности или изменений в потреблении пищи. В культивируемых человеческих и мышиных печёночных клетках CPTH2 снижал число жировых капель и триглицеридов только при наличии GCN5, подтверждая специфичность его действия. Важно, что и в клетках, и у мышей, леченных активаторами LXR (разрабатываемыми для улучшения выведения холестерина и борьбы с атеросклерозом), CPTH2 выборочно блокировал нежелательное повышение синтеза жира, вызванного SREBP1c, при этом сохраняя гены, способствующие обратному транспорту холестерина. В комбинации с агонистом LXR у мышей на высокожировой диете CPTH2 дополнительно снижал вредные уровни липидов в крови и холестерина в печени и предотвращал дополнительное накопление жира в печени.
Что это значит для пациентов
Исследование позиционирует GCN5 как центральный фактор накопления жира в печени при MASLD, связывая диетные и гормональные сигналы с переключателем продукции жира SREBP1c. Поскольку GCN5, по-видимому, не обязателен для полезной ветви сигналинга LXR, отвечающей за выведение холестерина, препараты, ингибирующие GCN5 — такие как CPTH2 или более продвинутые аналоги — могут уменьшать печёночный жир и воспаление, сохраняя при этом сердечносберегающие эффекты терапии, направленной на холестерин. Для людей с риском как жировой болезни печени, так и сердечно‑сосудистых заболеваний таргетирование этого эпигенетического переключателя в будущем может предложить способ защитить печень без утраты преимуществ улучшения обращения с холестерином.
Цитирование: Xiao, HT., Song, P., Jin, J. et al. GCN5 drives MASLD progression through LXRα/SREBP1c signaling pathway–mediated de novo lipogenesis. Nat Commun 17, 2821 (2026). https://doi.org/10.1038/s41467-026-69736-y
Ключевые слова: жировая болезнь печени, эпигенетика, липидный обмен, обмен веществ в печени, ядерные рецепторы