Clear Sky Science · ru
Некелятный контроль в аллилировании α‑оксикетонов с использованием аллилэтранов группы‑14
Точная сборка молекулярных форм
Многие лекарства и природные вещества действуют лишь тогда, когда их атомы расположены в точно определённой трёхмерной форме. Химики поэтому тратят огромные усилия на изучение способов «пришивания» новых фрагментов к молекуле с одной или другой стороны. В этой статье описан новый подход присоединения аллил‑фрагментов — коротких цепочек из трёх углеродов — к распространённому классу соединений, открывающий доступ к зеркально‑симметричным структурам, которые до сих пор было очень трудно получить.
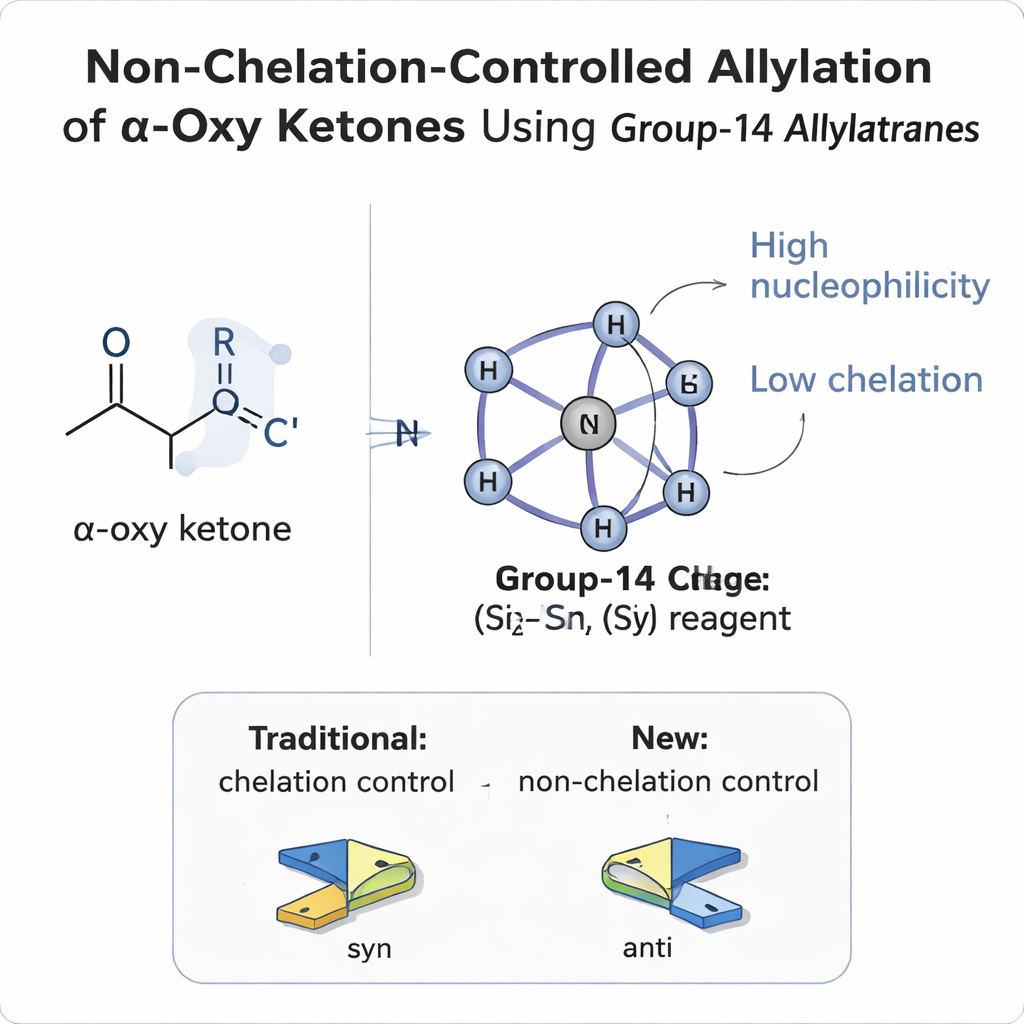
Почему трудно контролировать сторону атаки
Когда новый фрагмент добавляют к плоскому углеродно‑кислородному двойному звену (карбонилу), он может атаковать с любой из двух граней, как мяч, попадающий в монету сверху или снизу. Если на соседнем атоме углерода (α‑позиция) уже есть заместитель, результатом могут быть два различных трёхмерных продукта — диастереомеры. Десятилетиями химики опирались на простые модели — Фелкин–Анх, полярный Фелкин–Анх, Крам и модели с келяцией — чтобы предсказывать, какую сторону выберет реагент. В α‑оксикарбонилах, где соседний заместитель содержит кислород (например, эфир или эфиркарбонил), кислород обычно действует как «лапа», захватывающая металлические реагенты. Такая «келяция» фиксирует молекулу в одном конформационном состоянии и почти всегда даёт так называемые syn‑продукты, когда вновь образованные гидроксильные группы оказываются по одну сторону углеродной цепи.
Долговременная проблема с кислородными соседями
Хотя келяционный путь полезен, он одновременно ограничивает: он сильно смещает реакцию в сторону syn‑продуктов и делает получение противоположной anti‑конфигурации — при которой две гидроксильные группы ориентированы в разные стороны — очень затруднительным. Для α‑оксивальдегидов — молекул, где карбонильный углерод связан по крайней мере с одним атомом водорода — несколько хитроумных приёмов с использованием специальных силиконовых реагентов и тщательно подобранных кислот Льюиса позволяли получать anti‑продукты. Но для α‑оксикетонов, которые менее реакционноспособны и чаще встречаются в сложных целях синтеза, задача сложнее. Более сильные нуклеофилы обычно являются более кислотными по Льюису, что, в свою очередь, способствует той самой келяции, которой химики хотят избежать. Таким образом, баланс между «достаточно реактивным» и «не слишком липким» по отношению к кислороду остаётся ключевой нерешённой проблемой.
Клеточная реагентная структура, нарушающая правило
Авторы представляют новую семью реагентов — аллилэтраны, построенных вокруг элементов группы‑14 (кремний, германий и олово), удерживаемых в жёсткой, клеточной (cage‑подобной) структуре. В этих молекулах внутренний атом азота тянется через каркас, связываясь с центральным атомом и создавая сильно координированный, почти инкапсулированный центр. Эта конструкция даёт два ключевых эффекта. Во‑первых, она повышает нуклеофильность присоединённого аллил‑фрагмента, делая его охотнее образующим новую углеродно‑углеродную связь. Во‑вторых, она смягчает кислотность Льюиса центрального атома, поэтому он гораздо менее склонен к сильному связыванию с кислородными атомами субстрата. Квантово‑химические расчёты и данные ЯМР подтверждают, что заряд локализован на аллил‑фрагменте, в то время как электронная связь с кремниевым центром ослаблена, что объясняет, как реагент может быть одновременно мощным и не склонным к келяции.
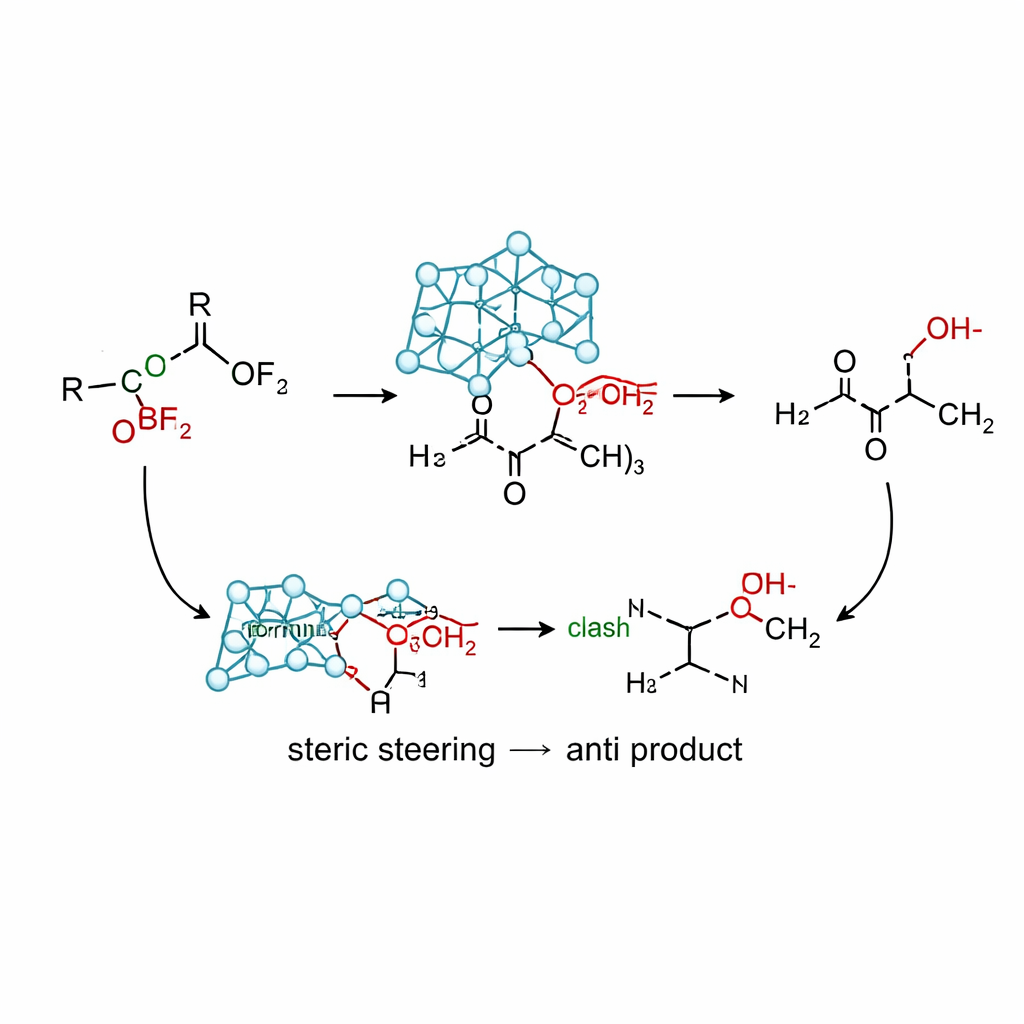
Как новая реакция работает на практике
Используя силиконовую версию реагента, аллилсилатран, совместно с мягкой кислотой Льюиса (трифторидом бора), команда разработала условия, дающие высокие выходы anti‑гомоаллильных спиртов из широкого круга α‑оксикетонов. Контрольные эксперименты показывают, что многие традиционные источники аллил‑фрагмента — на основе олова, индия, магния, лития и простых силанов — либо смещают реакцию в сторону syn‑продукта, дают смеси, либо разлагаются. Напротив, аллилсилатран стабильно обеспечивает соотношения anti/syn выше 95:5 для субстратов с метокси‑, изопропокси‑, фенокси‑, ацетокси‑, силокси‑ и аминокси‑заместителями, а также для различных ароматических колец и циклических кетонов. Вычисления указывают на некеляционный путь, при котором громоздкий атран‑каркас направляет подход аллил‑группы в конформацию, напоминающую модель Крама: кислородный заместитель располагается напротив карбонила, а стерическое отталкивание между клеткой и близлежащими фенильными кольцами предпочитает траекторию, ведущую к anti‑продукту.
Последствия для синтеза лекарств и природных продуктов
Метод также работает для более жёстких циклических систем, где объёмность аллилсилатрана поощряет атаку со менее затруднённых позиций, а также для специализированных производных, передающих замещённые аллил‑группы с аналогично высокой anti‑селективностью. Поскольку получающиеся anti‑1,2‑диолы с гомоаллильным фрагментом являются распространёнными мотивами в биологически активных молекулах, включая кандидатов на модуляторы ферментов, эта трансформация даёт химикам надёжный способ доступа к структурным вариантам, которые ранее требовали многопроходных обходных путей или были практически недостижимы. Важно, что те же субстраты можно направлять на получение либо syn, либо anti‑продуктов, переключаясь между келяционной оловянной системой и новой некеляционной силатранной системой, что обеспечивает точный контроль над молекулярной формой.
Что это значит простыми словами
По существу исследователи создали умный инструмент доставки аллил‑фрагмента, который поражает целевой углерод с «непредпочтительной» стороны, не попадая в ловушку рядом стоящих атомов кислорода. Тщательно разработав клетку вокруг кремния, они разъединили силу и «липкость»: реагент достаточно силён, чтобы установить новую связь, но не настолько «липок», чтобы захватывать окружающие атомы и нарушать желаемую геометрию. Для неспециалистов это означает, что у химиков теперь гораздо более надёжный контроль над лепкой трёхмерных молекулярных форм, лежащих в основе многих лекарств и природных продуктов, что расширяет пространство дизайна для будущих медикаментов и сложных синтетических молекул.
Цитирование: Tsutsui, Y., Shiga, K., Konishi, A. et al. Non-chelation control in allylations of α-oxy ketones using group-14 allylatranes. Nat Commun 17, 2019 (2026). https://doi.org/10.1038/s41467-026-69732-2
Ключевые слова: стереоселективное аллилирование, α‑оксикетоны, аллилсилатран, некеляционный контроль, гомоаллильные спирты