Clear Sky Science · ru
Регион N‑Myc MB0–MBI специфически и динамично взаимодействует с N-доменом киназы Aurora A
Почему это важно для лечения рака
Многие агрессивные детские опухоли зависят от белка N‑Myc, который поддерживает рост раковых клеток. Сам N‑Myc трудно блокировать лекарствами, потому что он ведёт себя скорее как гибкая спагетти‑нитка, чем как жесткая замочная скважина для ключа. В этом исследовании в беспрецедентных деталях показано, как N‑Myc охватывает другой белок — фермент Aurora kinase A (AurA), усиливая его активность и помогая клеткам опухоли выживать. Нанесение на карту этого взаимодействия раскрывает реалистичный путь для его разрушения малыми молекулами.
Гибкий нарушитель находит твёрдого партнёра
N‑Myc принадлежит к семейству MYC — главный регулятор роста, метаболизма и деления клеток. При его избыточной экспрессии эти регуляторы становятся мощными онкогенами, особенно в опухолях нервной системы, таких как высоко‑рисковая нейробластома у детей. В отличие от многих ферментов или рецепторов, N‑Myc сам по себе не сворачивается в фиксированную 3D‑форму; это «внутренне неупорядоченный» белок, который постоянно шевелится и меняет конформацию. Такая гибкость делает его адаптивным, но также чрезвычайно трудным для прямого лекарственного воздействия. AurA, напротив, — хорошо организованный фермент, участвующий в координации деления клетки. Ранее было показано, что AurA помогает стабилизировать N‑Myc в опухолевых клетках и что два белка физически взаимодействуют, но точная природа и значение контактных участков оставались неясными.
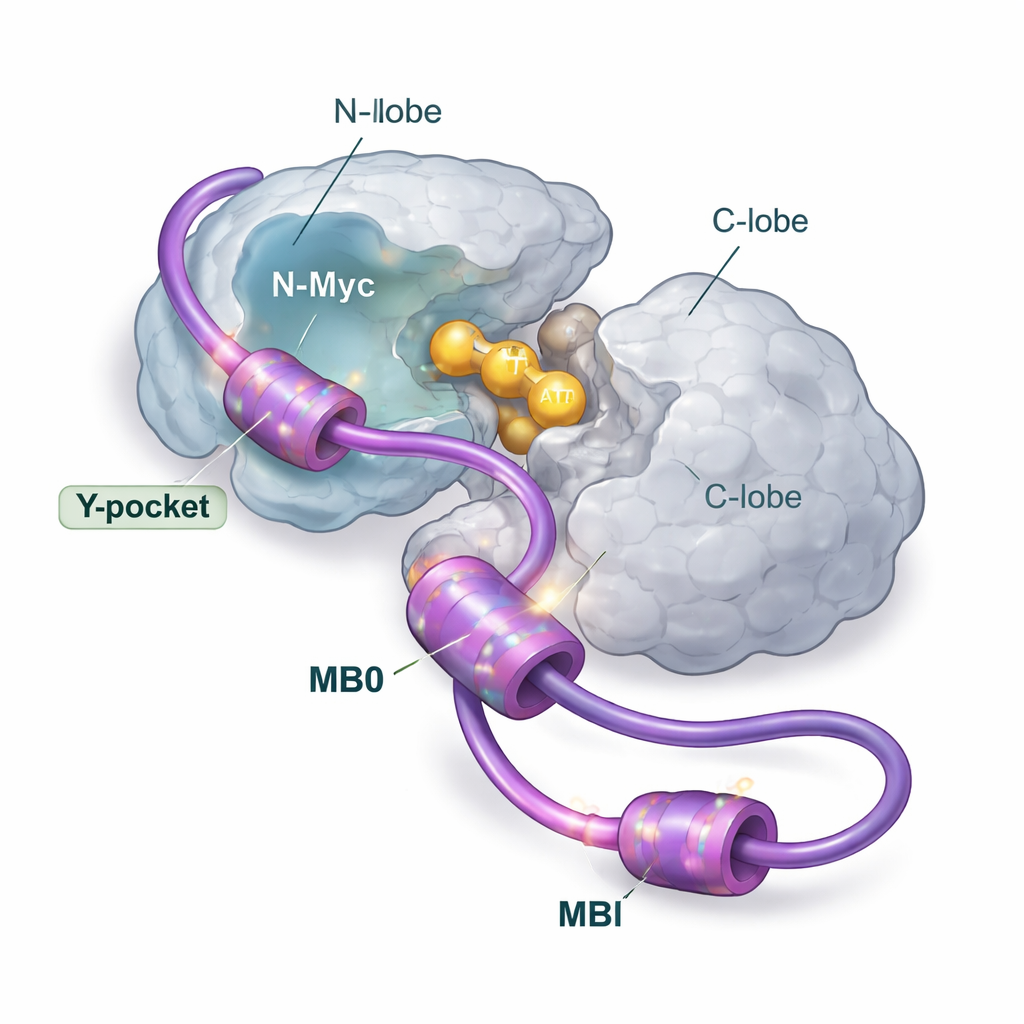
Несколько точек захвата, одна основная посадочная площадка
Используя широкий набор структурных и биофизических методов — включая ядерный магнитный резонанс, рассеяние рентгеновских лучей, масс‑спектрометрию, калориметрию и компьютерное моделирование — авторы детально рассмотрели, как N‑Myc и AurA связываются в растворе. Они сосредоточились на переднем конце N‑Myc, который содержит два консервативных региона, называемых MB0 и MBI. Эти короткие фрагменты богаты ароматическими остатками (например, фенилаланин, тирозин и триптофан), которые склонны прилипать к гидрофобным карманам на белковых партнёрах. Команда показывает, что N‑Myc в основном связывается с AurA в соотношении 1:1, причём MB0 и MBI выступают основными контактными зонами. Другой участок N‑Myc, привлекавший внимание предыдущих кристаллических структур, оказывается лишь второстепенным в присутствии полного региона MB0–MBI.
Динамическое рукопожатие, которое включает фермент
Вместо того чтобы фиксироваться в единственной жёсткой позе, N‑Myc остаётся во многом неупорядоченным даже при связывании с AurA. Данные указывают на «размытый» комплекс: несколько сегментов N‑Myc по очереди контактируют с разными участками N‑домена AurA, особенно с пазом, известным как Y‑карман, и с соседней петлёй, которая связывает сигналы с активным центром. Несмотря на эту рыхлость, эффект очевиден — связывание MB0 и MBI стабилизирует N‑домен AurA и увеличивает его киназную активность, то есть он эффективнее переносит фосфатные группы на свои мишени. Когда исследователи систематически заменяли ключевые ароматические остатки в MB0 и MBI на аланин, комплекс N‑Myc–AurA ослабевал, фермент меньше стабилизировался, и его активность падала. Это показывает, что специфические ароматические «якоря» в иначе гибкой цепочке N‑Myc необходимы для усиления AurA.
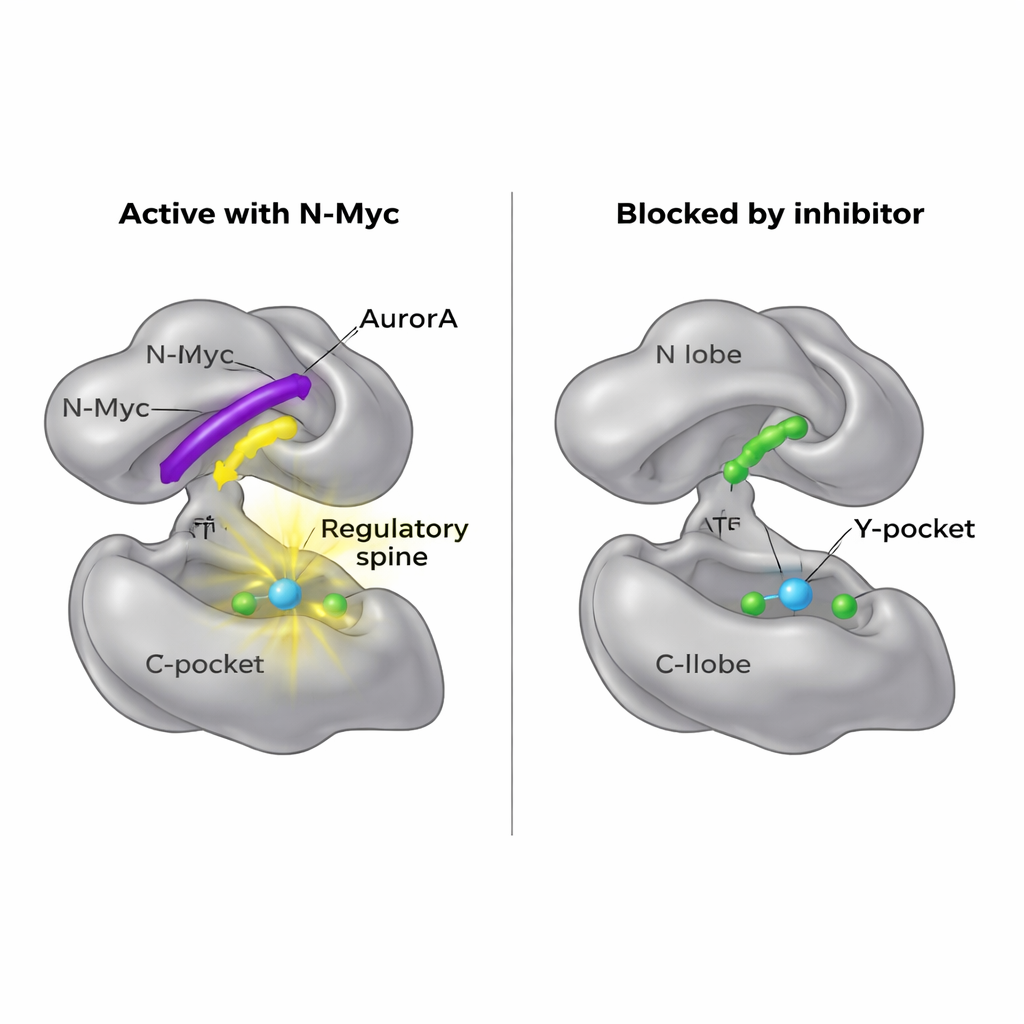
Открытие новой точки входа для лекарств
Поскольку сам N‑Myc трудно «задействовать» лекарствами, исследователи спросили, можно ли вместо этого блокировать его посадочную площадку на AurA. Их структурные карты показали, что MB0 и MBI занимают ту же общую область N‑домена, которую использует другой партнёр, белок TPX2, для активации AurA. Небольшая молекула AurkinA уже известна тем, что вталкивается в Y‑карман и вытесняет TPX2. В экспериментах связывания AurkinA эффективно конкурировала и с N‑Myc за N‑домен AurA, предотвращая прикрепление как фрагмента N‑Myc1–69, так и N‑Myc1–100. Этот результат демонстрирует, что поверхность N‑домена, и особенно Y‑карман, представляет собой «лекарственно‑пригодную» горячую точку, контролирующую не только классических регуляторов вроде TPX2, но и неупорядоченные онкопротеины, такие как N‑Myc.
Что это означает для будущих терапий
Эта работа перекладывает представление о партнёрстве N‑Myc–AurA как о динамичном, многоконтактном объятии, сосредоточенном на N‑домене AurA, а не о единой жёсткой зоне связывания. Для неспециалистов ключевой вывод в том, что даже бесформенный онкобелок, такой как N‑Myc, можно атаковать косвенно, нацеливаясь на твёрдое посадочное пятно на его партнёрном ферменте. Показав, что существующие соединения, связывающиеся с N‑доменом, могут вытеснить N‑Myc из AurA, исследование прокладывает понятный путь к препаратам, которые избирательно нарушают это взаимодействие. Такие агенты могли бы ослабить критическую поддержку N‑Myc в высоко‑рисковых детских опухолях и, при дальнейшем развитии, предложить новый лечебный путь для раков, долго считавшихся «нелекаруемыми».
Цитирование: Hultman, J., Morad, V., Tanner, E. et al. The N-Myc MB0-MBI region interacts specifically and dynamically with the N-lobe of Aurora kinase A. Nat Commun 17, 2016 (2026). https://doi.org/10.1038/s41467-026-69725-1
Ключевые слова: N‑Myc, Aurora kinase A, внутренне неупорядоченные белки, нейробластома, ингибиторы белок–белкового взаимодействия